实验室用50 mL浓盐酸跟足量的氯酸钾固体共热制取氯气,该反应的化学方程式为KClO3+6HCl(浓) ===3Cl2↑+KCl+3H2O。
(1)浓盐酸在此反应中所具有的性质是__________ (填写编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(2)若产生0.3 mol Cl2,求反应中转移的电子数__________ 。
(3)若反应中HCl的利用率为50%,当反应结束时,生成氯气0.15 mol,则浓盐酸的物质的量浓度为_________ 。
(1)浓盐酸在此反应中所具有的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(2)若产生0.3 mol Cl2,求反应中转移的电子数
(3)若反应中HCl的利用率为50%,当反应结束时,生成氯气0.15 mol,则浓盐酸的物质的量浓度为
更新时间:2017-12-07 07:24:06
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】已知金属钠和金属铝共7.3g,放入足量的水中充分反应无金属剩余,共收集到标准状况下的气体5.6L。
(1)写出钠与水反应的化学方程式,并用双线桥分析该反应电子转移方向和数目__________ ;
(2)求出混合物中金属钠和金属铝的物质的量之比。__________
(3)若反应后溶液的体积为100mL,求所得溶液中剩余NaOH的物质的量浓度。__________
(1)写出钠与水反应的化学方程式,并用双线桥分析该反应电子转移方向和数目
(2)求出混合物中金属钠和金属铝的物质的量之比。
(3)若反应后溶液的体积为100mL,求所得溶液中剩余NaOH的物质的量浓度。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】在工业生产中要制取某种物质,除了要考虑反应进行的可能性,还要考虑原料来源、成本高低和设备要求等因素,以选取最适当的方法。例如,工业上制取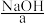 一般不采用
一般不采用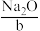 与
与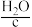 反应的方法(Na2O作为原料,来源少、成本高),而主要采用电解饱和食盐水的方法,过去也曾采用
反应的方法(Na2O作为原料,来源少、成本高),而主要采用电解饱和食盐水的方法,过去也曾采用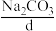 与
与 且2反应的方法。
且2反应的方法。
回答下列问题:
(1)Na与水反应的离子方程式为________ 。
(2)电解饱和食盐水的化学方程式为2NaCl+2H2O 2NaOH+H2↑+Cl2↑:
2NaOH+H2↑+Cl2↑:
①该反应中的还原剂为_______ (填化学式,下同),被氧化的物质为________ 。
②用单线桥法表示该反应中电子转移的方向和数目:_______ 。
③每生成0.2gH2,同时生成Cl2的质量为________  。
。
(3)d和e反应可制得a:
①碳酸钠的俗称为________ 。
②从碳酸钠组成的阴离子来看,其属于_______ 盐。
③将Na2CO3溶液加入澄清石灰水中,发生反应的离子方程式为_______ 。
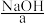 一般不采用
一般不采用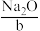 与
与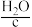 反应的方法(Na2O作为原料,来源少、成本高),而主要采用电解饱和食盐水的方法,过去也曾采用
反应的方法(Na2O作为原料,来源少、成本高),而主要采用电解饱和食盐水的方法,过去也曾采用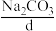 与
与 且2反应的方法。
且2反应的方法。回答下列问题:
(1)Na与水反应的离子方程式为
(2)电解饱和食盐水的化学方程式为2NaCl+2H2O
 2NaOH+H2↑+Cl2↑:
2NaOH+H2↑+Cl2↑:①该反应中的还原剂为
②用单线桥法表示该反应中电子转移的方向和数目:
③每生成0.2gH2,同时生成Cl2的质量为
 。
。(3)d和e反应可制得a:
①碳酸钠的俗称为
②从碳酸钠组成的阴离子来看,其属于
③将Na2CO3溶液加入澄清石灰水中,发生反应的离子方程式为
您最近一年使用:0次
【推荐3】近来,《饮用天然矿泉水》新标准引起热议,其中备受争议的溴酸盐是一种致癌物,新标准中溴酸盐极值为0.01mg/L。已知在酸性条件下有以下反应:
①2 +I2===2
+I2===2 +Br2
+Br2
②2 +10Br-+12H+===I2+5Br2+6H2O
+10Br-+12H+===I2+5Br2+6H2O
③5Br-+ +6H+===3Br2+3H2O
+6H+===3Br2+3H2O
请回答下列问题:
(1)有同学根据反应①得出氧化性:I2>Br2的结论,请说明该结论错误的理由是:_________ 。
(2)反应②中: →l2发生的是
→l2发生的是__________ 反应(氧化、还原)。
现向含6mol的KI的硫酸溶液中逐滴滴加KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量有如图的关系:
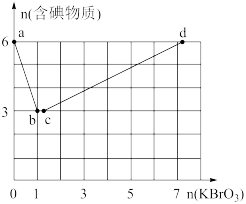
(3)完成a→b阶段的反应方程式,并标出电子转移的方向和数目:I-+BrO3-+H+→ ,________ 。
(4)b→c阶段只有一种元素化合价发生了改变,反应中氧化产物和还原产物的物质的量之比为______ 。
(5)a→b、b→c、c→d阶段的还原剂分别是______ 、_______ 、______ ,依次发生的这些反应,说明有关物质(l2、Br2、I-、Br-)还原性由强到弱的顺序是________ 。
①2
 +I2===2
+I2===2 +Br2
+Br2②2
 +10Br-+12H+===I2+5Br2+6H2O
+10Br-+12H+===I2+5Br2+6H2O③5Br-+
 +6H+===3Br2+3H2O
+6H+===3Br2+3H2O请回答下列问题:
(1)有同学根据反应①得出氧化性:I2>Br2的结论,请说明该结论错误的理由是:
(2)反应②中:
 →l2发生的是
→l2发生的是现向含6mol的KI的硫酸溶液中逐滴滴加KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量有如图的关系:

(3)完成a→b阶段的反应方程式,并标出电子转移的方向和数目:I-+BrO3-+H+→ ,
(4)b→c阶段只有一种元素化合价发生了改变,反应中氧化产物和还原产物的物质的量之比为
(5)a→b、b→c、c→d阶段的还原剂分别是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】中国首款完全自主知识产权民用客机C919的钛合金用量达9.3%。制备海绵钛的化学方程式为TiCl4+2Mg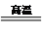 2MgCl2+Ti
2MgCl2+Ti
(1)该反应中,作为还原剂的物质是____ ,Ti元素的化合价__ (填“升高”或“降低”)
(2)若反应中消耗了2 mol Mg,则生成___ molTi。转移电子的物质的量为____ mol
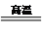 2MgCl2+Ti
2MgCl2+Ti(1)该反应中,作为还原剂的物质是
(2)若反应中消耗了2 mol Mg,则生成
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】含氮废水进入水体而对环境造成的污染越来越严重,环境专家认为可以用金属铝将水体中的NO3-还原为N2,从而消除污染。其反应的离子方程式是:
6NO3-+ 10Al + 18H2O → 3N2↑+ 10Al(OH)3+ 6OH-
(1)现在要除去1m3含氮元素0.3mol的废水中的NO3-(设氮元素都以NO3-的形式存在,下同),则至少需要消耗金属铝__________ g。
(2)有人认为金属镁比铝能更快消除氮的污染,其反应原理和金属铝相同。
①写出镁和含氮废水反应的离子方程式:___________________________________
②已知金属镁是从海水中提取的MgCl2,通过电解制得的。若要除去1m3含氮元素0.3mol的废水中的NO3-,则至少需要含0.5%(质量分数)MgCl2的海水_________ kg。
6NO3-+ 10Al + 18H2O → 3N2↑+ 10Al(OH)3+ 6OH-
(1)现在要除去1m3含氮元素0.3mol的废水中的NO3-(设氮元素都以NO3-的形式存在,下同),则至少需要消耗金属铝
(2)有人认为金属镁比铝能更快消除氮的污染,其反应原理和金属铝相同。
①写出镁和含氮废水反应的离子方程式:
②已知金属镁是从海水中提取的MgCl2,通过电解制得的。若要除去1m3含氮元素0.3mol的废水中的NO3-,则至少需要含0.5%(质量分数)MgCl2的海水
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】亚硝酸钠有咸味,有毒,暴露于空气中会与氧气反应生成硝酸钠。
已知: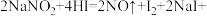 _______。
_______。
(1)上述方程式中横线处应填的是_______ 。
(2)上述反应的还原剂为_______ (填化学式);若反应中有 (标准状况下)气体生成则反应中转移电子的物质的量为
(标准状况下)气体生成则反应中转移电子的物质的量为_______  。
。
(3)在酸性条件下,高锰酸钾可将 氧化为
氧化为 ,所得溶液中锰元素仅以
,所得溶液中锰元素仅以 形式存在,写出此反应的离子方程式:
形式存在,写出此反应的离子方程式:_______ 。
(4) 加热到320℃以上会分解生成二氧化氮、一氧化氮和氧化钠,写出此反应的化学方程式
加热到320℃以上会分解生成二氧化氮、一氧化氮和氧化钠,写出此反应的化学方程式_______ 。反应中被氧化的元素和被还原的元素的物质的量之比为_______ 。
(5)某厂废液中,含有2%~5%的 ,直接排放会造成污染,
,直接排放会造成污染, 能使
能使 转化为
转化为 ,则反应中氧化剂和还原剂的质量之比为
,则反应中氧化剂和还原剂的质量之比为_______ 。
已知:
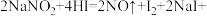 _______。
_______。(1)上述方程式中横线处应填的是
(2)上述反应的还原剂为
 (标准状况下)气体生成则反应中转移电子的物质的量为
(标准状况下)气体生成则反应中转移电子的物质的量为 。
。(3)在酸性条件下,高锰酸钾可将
 氧化为
氧化为 ,所得溶液中锰元素仅以
,所得溶液中锰元素仅以 形式存在,写出此反应的离子方程式:
形式存在,写出此反应的离子方程式:(4)
 加热到320℃以上会分解生成二氧化氮、一氧化氮和氧化钠,写出此反应的化学方程式
加热到320℃以上会分解生成二氧化氮、一氧化氮和氧化钠,写出此反应的化学方程式(5)某厂废液中,含有2%~5%的
 ,直接排放会造成污染,
,直接排放会造成污染, 能使
能使 转化为
转化为 ,则反应中氧化剂和还原剂的质量之比为
,则反应中氧化剂和还原剂的质量之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)19 g某二价金属的氯化物ACl2中含有0.4 mol Cl-,金属A的相对原子质量是___________ 。
(2)根据反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,可知当有2.5 mol FeS2参加反应时,被氧化的硫元素的物质的量为___________ mol。
(1)19 g某二价金属的氯化物ACl2中含有0.4 mol Cl-,金属A的相对原子质量是
(2)根据反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,可知当有2.5 mol FeS2参加反应时,被氧化的硫元素的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】氯的单质及其化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂。
(1)常温下,可用氯酸钾固体与浓盐酸反应制备Cl2,写出反应的化学方程式___ ,若氧化产物比还原产物多1mol,则被氧化HCl的物质的量为___ mol。
(2)Cl2O为淡棕黄色气体,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为___ 。
(3)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力,Cl2O的有效氯含量为___ 。(计算结果保留两位小数)
(1)常温下,可用氯酸钾固体与浓盐酸反应制备Cl2,写出反应的化学方程式
(2)Cl2O为淡棕黄色气体,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为
(3)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力,Cl2O的有效氯含量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】钾是活泼的碱金属,钾和氧有氧化钾(K2O)、过氧化钾(K2O2)和超氧化钾(KO2)等多种化合物。
⑴钾和硝酸钾反应可制得氧化钾:K+KNO3→K2O+N2(未配平),每生成9.4gK2O消耗的还原剂有___________ g
⑵超氧化钾和过氧化钾都能与二氧化碳反应均生成氧气和K2CO3,在医院、矿井、潜水、高空飞行中用作供氧剂。写出超氧化钾与二氧化碳反应的化学方程式______________________ ,为了维持气压稳定,可以使用超氧化钾和过氧化钾的混合物使吸收的CO2与生成的O2体积相同(同温同压),则它们的物质的量之比为n(KO2) :n(K2O2)=____________
⑶KO2加热至600℃部分分解得到产物A。6.30g产物A充分吸收二氧化碳生成碳酸钾并产生氧气1.12L(标准状况),试确定产物A中钾氧两种原子个数之比_______ 。如果产物A只含有两种化合物,写出所有可能的化学式并计算A中两种化合物的物质的量之比_______ 。
⑴钾和硝酸钾反应可制得氧化钾:K+KNO3→K2O+N2(未配平),每生成9.4gK2O消耗的还原剂有
⑵超氧化钾和过氧化钾都能与二氧化碳反应均生成氧气和K2CO3,在医院、矿井、潜水、高空飞行中用作供氧剂。写出超氧化钾与二氧化碳反应的化学方程式
⑶KO2加热至600℃部分分解得到产物A。6.30g产物A充分吸收二氧化碳生成碳酸钾并产生氧气1.12L(标准状况),试确定产物A中钾氧两种原子个数之比
您最近一年使用:0次



