某温度时,测得0.01 mol/L的NaOH溶液的pH为11,在此温度下,将pH=12的强碱与pH=2的强酸溶液混合,所得混合溶液的pH=10,则强碱与强酸的体积比为( )
| A.1∶9 | B.9∶1 | C.1∶11 | D.11∶1 |
更新时间:2018-01-03 15:33:40
|
相似题推荐
单选题
|
较难
(0.4)
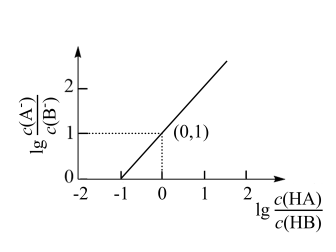
【推荐1】常温下,向20mL0.1000mol·L-1NaB溶液中滴加等浓度的弱酸HA溶液,所得混合溶液中lg 与1g
与1g 的关系如图所示。已知Ka(HA)=1.77×10-4。下列说法正确的是
的关系如图所示。已知Ka(HA)=1.77×10-4。下列说法正确的是
 与1g
与1g 的关系如图所示。已知Ka(HA)=1.77×10-4。下列说法正确的是
的关系如图所示。已知Ka(HA)=1.77×10-4。下列说法正确的是
| A.Ka(HB)>Ka(HA) |
B.pH=4时,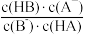 的值比pH=3的大 的值比pH=3的大 |
| C.滴入20mLHA溶液后存在关系:c(A-)>c(HB) |
| D.pH=7时,混合溶液中一定存在关系:c(Na+)=c(B-) |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
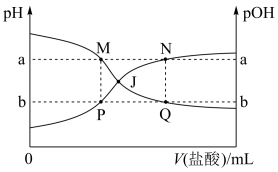
【推荐2】25℃时,用HCl气体调节0.1mol⋅L⁻¹氨水的pH,体系中粒子浓度的对数(lgc)、反应物的物质的量之比 与溶液pH的关系如图所示。若忽略通入气体后溶液体积的变化,下列有关说法错误的是
与溶液pH的关系如图所示。若忽略通入气体后溶液体积的变化,下列有关说法错误的是
 与溶液pH的关系如图所示。若忽略通入气体后溶液体积的变化,下列有关说法错误的是
与溶液pH的关系如图所示。若忽略通入气体后溶液体积的变化,下列有关说法错误的是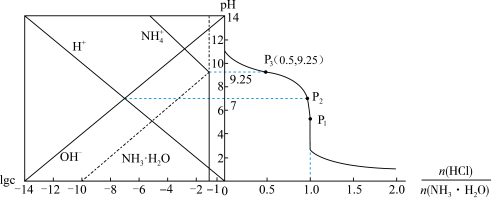
| A.P1点溶液中:c(Cl⁻)>c(NH3⋅H2O) |
B.P2点溶液中:c(NH )=c(Cl-) )=c(Cl-) |
| C.25℃时,NH4Cl的水解平衡常数的数量级为10-9 |
D. =0.5时,c(NH3⋅H2O)+c(NH =0.5时,c(NH3⋅H2O)+c(NH )=2c(Cl-) )=2c(Cl-) |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】常温下,下列各组离子一定能在指定溶液中大量共存的是
A.投入足量漂白粉后的溶液中:Fe2+、H+、Cl-、 |
B.0.1 mol/L FeCl3溶液中:Na+、Ba2+、 、SCN- 、SCN- |
C.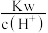 =1×10-13 mol/L的溶液中: =1×10-13 mol/L的溶液中: 、Ca2+、Cl-、 、Ca2+、Cl-、 |
D.水电离的c(OH-)=1×10-13 mol/L的溶液中:K+、Na+、 、 、 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】常温下,甲溶液的pH = 4,乙溶液的pH = 5,甲溶液与乙溶液中由水电离的c(H+)之比不可能是( )
| A.2∶1 | B.10∶1 | C.1∶10 | D.1∶105 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】常温下用0.10 mol·L-1NaOH溶液分别滴定20.00mL浓度均为0.10mol • L-1的CH3COOH(Ka=1.75×10-5)溶液和HCN (Ka=4.9×10-10)溶液所得滴定曲线。下列说法正确的是

| A.曲线I和曲线Ⅱ分别代表的是CH3COOH和HCN |
| B.点③和点⑤所示溶液中:c(CN—) = c(CH3COO—) |
| C.点①和点②所示溶液中 c(CH3COO—)-c(CN—) =c(HCN)-c(CH3COOH) |
| D.在点②和③之间(不包括端点)存在以下关系:c(Na+)>c(A—)>c(H+)>c(OH—)(A—代表溶液中的酸根离子) |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】室温下,下列有关两种溶液的说法不正确 的是
| 序号 | ① | ② |
| pH | 12 | 12 |
| 溶液 | 氨水 | 氢氧化钠溶液 |
| A.①②两溶液中c(OH-)相等 |
| B.①②两溶液中水的电离程度相同 |
| C.①②两溶液分别加水稀释10倍,稀释后溶液的pH:①<② |
| D.等体积的①②两溶液分别与0.01mol·L-1的盐酸完全中和,消耗盐酸的体积:①>② |
您最近半年使用:0次