Cu、Ni、V为制造合金及合成催化剂的重要元素。 请回答:
(1)基态铜原子的电子排布式是_________________ 。基态铜原子价电子层排布依据的原理,可用于解释下列事实的是___________ 。
A.Fe2+易被氧化为Fe3+ B.铜丝灼烧时焰色呈绿色
C.N的第一电离能大于O的第一电离能 D.NaCl的熔点比KCl的高
(2)[Cu(NH3)4]SO4是一种重要的配合物。与SO42-互为等电子体的分子的化学式为__________ (任写一种)。NH3与CH4的VSPER构型相同,其中NH3的键角较小,原因是____________ 。Ni(CO)4中σ键和π键的数目之比为_________ 。
(3)钒的某种配合物有增强胰岛素和降糖作用,其分子结构如图所示。
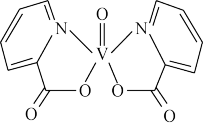
① 基态V元素的价层电子轨道表示式______________________ ,分子中非金属元素电负性由大到小的顺序为________ 。
② 该物质的晶体中除配位键外,所含微粒间作用力的类型还有___________ (填序号)。
a.金属键 b.极性键 c.非极性键 d.范德华力 e.氢键
③ 1mol分子中含有配位键的数目是______ ,分子中采取sp2杂化的原子有_______ 。
(1)基态铜原子的电子排布式是
A.Fe2+易被氧化为Fe3+ B.铜丝灼烧时焰色呈绿色
C.N的第一电离能大于O的第一电离能 D.NaCl的熔点比KCl的高
(2)[Cu(NH3)4]SO4是一种重要的配合物。与SO42-互为等电子体的分子的化学式为
(3)钒的某种配合物有增强胰岛素和降糖作用,其分子结构如图所示。

① 基态V元素的价层电子轨道表示式
② 该物质的晶体中除配位键外,所含微粒间作用力的类型还有
a.金属键 b.极性键 c.非极性键 d.范德华力 e.氢键
③ 1mol分子中含有配位键的数目是
更新时间:2018-03-20 18:05:14
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、E、F五种元素的原子序数依次递增。已知:F位于周期表中第四周期IB族,其余的均为短周期主族元素,X、E同主族,E的氧化物是光导纤维的主要成分,X是形成化合物种类最多的元素之一,基态Z原子核外p轨道的未成对电子数为2。请回答下列问题:
(1)基态Y原子价层电子排布式为____ 。原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ ,表示,则与之相反的用-
,表示,则与之相反的用- 表示,这称为电子的自旋量子数。对于基态的Y原子,其价电子的自旋量子数代数和为
表示,这称为电子的自旋量子数。对于基态的Y原子,其价电子的自旋量子数代数和为____ 。
(2)X、Y、E三种元素的第一电离能由小到大的顺序为____ (填元素符号,下同);电负性由小到大的顺序为____ 。
(3)X、Z和氢元素按原子数目比为1:1:2形成常温下呈气态的物质,其分子中键角约为____ ,其中X原子的杂化轨道类型为____ 。
(4)F2+与NH3能形成[F(NH3)4]2+离子,[F(NH3)4]2+中的配位原子为____ (填元素符号)。若[F(NH3)4]2+离子中2个NH3被2个Cl-替代可以得到2种不同的结构,则[F(NH3)4]2+离子的空间结构名称是____ 。(填“平面四方形”或“正四面体”)。
(5)F2Z的晶胞中(结构如图所示)所包含的F离子数目为____ 。若其晶体密度为ρ g·cm-3,F离子的半径为r1 pm,Z离子的半径为r2 pm,阿伏加德罗常数的值为NA,则该晶胞中原子的空间利用率(即原子的体积占晶胞体积的百分率)为____ 。(用含ρ、r1、r2、NA的代数式表示,列式即可,不需化简)。

(1)基态Y原子价层电子排布式为
 ,表示,则与之相反的用-
,表示,则与之相反的用- 表示,这称为电子的自旋量子数。对于基态的Y原子,其价电子的自旋量子数代数和为
表示,这称为电子的自旋量子数。对于基态的Y原子,其价电子的自旋量子数代数和为(2)X、Y、E三种元素的第一电离能由小到大的顺序为
(3)X、Z和氢元素按原子数目比为1:1:2形成常温下呈气态的物质,其分子中键角约为
(4)F2+与NH3能形成[F(NH3)4]2+离子,[F(NH3)4]2+中的配位原子为
(5)F2Z的晶胞中(结构如图所示)所包含的F离子数目为

您最近一年使用:0次
【推荐2】2019年1月3日上午,嫦娥四号探测器翩然落月,首次实现人类飞行器在月球背面的软着陆。所搭载的“玉兔二号”月球车,通过砷化镓(GaAs)太阳能电池提供能量进行工作。回答下列问题:
(1)基态Ga原子价电子轨道表示式为___________ ,核外电子占据最高能级的电子云形状为___________ ;基态As原子最高能层上有___________ 个电子。
(2)镓失去电子的逐级电离能(单位:kJ•mol-1)的数值依次为577、1985、2962、6192,由此可推知镓的主要化合价为___________ ,砷的第一电离能比镓___________ (填“大”或“小”)。
(3)第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为___________ 。
(4)砷化镓可由(CH3)3Ga和AsH3在700℃制得,(CH3)3Ga中C原子的杂化方式为___________ ,AsH3分子的空间构型为___________ 。
(5)相同压强下,AsH3的沸点___________ NH3(填“大于”或“小于”),原因为___________ 。
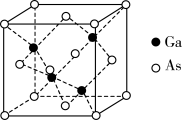
(6)GaAs为原子晶体,其晶胞结构如图所示,Ga与As以___________ (填“共价键”或“离子键”)键合。设阿伏加德罗常数的值为NA,该晶胞边长为a pm则GaAs晶体的密度为___________ g•cm-3(列出计算式即可)。
(1)基态Ga原子价电子轨道表示式为
(2)镓失去电子的逐级电离能(单位:kJ•mol-1)的数值依次为577、1985、2962、6192,由此可推知镓的主要化合价为
(3)第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为
(4)砷化镓可由(CH3)3Ga和AsH3在700℃制得,(CH3)3Ga中C原子的杂化方式为
(5)相同压强下,AsH3的沸点
(6)GaAs为原子晶体,其晶胞结构如图所示,Ga与As以

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】氮化镓(GaN)结构与金刚石类似,是一种半导体材料,因其具有良好的电学特性,广泛的应用于电子行业,近年智能手机的快速充电器中就使用了氮化镓材料。
(1)基态N原子的电子排布式为___________ ;基态Ga原子核外电子能量最高的电子占据的能级为___________ 。
(2)GaN、GaP、GaAs熔点如下表所示,分析其变化原因___________ 。
(3)GaN可在高温下由金属Ga和NH3反应制取。N原子和H原子可以形成多种微粒,如:NH3、NH 、NH
、NH 、N2H4、N2H
、N2H4、N2H 、N2H
、N2H 等。在N2H
等。在N2H 中,N原子的杂化方式为
中,N原子的杂化方式为___________ 。与N2H 互为等电子体的物质是
互为等电子体的物质是___________ (写出一种);在N2H 中存在的化学键类型有
中存在的化学键类型有___________ 。
a.极性键 b.非极性键 c.离子键 d.配位键
(4)GaN的晶胞结构如图所示:其中与Ga原子最近的N原子所构成的空间结构为___________ ;若GaN晶体的密度为6.1 g/cm3,阿伏加德罗常数为NA,则距离最近的两个N原子间的距离为___________ nm(写出表达式即可)。

(1)基态N原子的电子排布式为
(2)GaN、GaP、GaAs熔点如下表所示,分析其变化原因
| 晶体 | GaN | GaP | GaAs |
| 熔点/℃ | 1700 | 1480 | 1238 |
(3)GaN可在高温下由金属Ga和NH3反应制取。N原子和H原子可以形成多种微粒,如:NH3、NH
 、NH
、NH 、N2H4、N2H
、N2H4、N2H 、N2H
、N2H 等。在N2H
等。在N2H 中,N原子的杂化方式为
中,N原子的杂化方式为 互为等电子体的物质是
互为等电子体的物质是 中存在的化学键类型有
中存在的化学键类型有a.极性键 b.非极性键 c.离子键 d.配位键
(4)GaN的晶胞结构如图所示:其中与Ga原子最近的N原子所构成的空间结构为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】新材料的研制与应用始终是科技发展的主要方向之一。
(1)某太阳能吸热涂层以镍或镍合金空心球为吸收剂,基态镍原子的价层电子排布式是____ 。
(2)硼及其化合物广泛应用于永磁材料、超导材料等领域,硼可以与氟气反应生成BF3气体,BF3分子的立体构型为___________ 。
(3)石墨的晶体结构如图所示,如图虚线勾勒出的是其晶胞。则石墨晶胞含碳原子个数___________ 。碳的两种同素异形体中键长较短的是___________ (填“石墨”或“金刚石”)。

(4)石墨烯(图甲〕是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(图乙)

图乙中,1号C的杂化方式是___________ ,该C与相邻C形成的键角___________ (填“>”“<”或“=”)图甲中1号C与相邻C形成的键角。
(5)有机太阳能固体电池材料含有高纯度C60,其分子结构如图,1molC分子中π键的数目为___________ 。C60能溶于二硫化碳而不溶于水的原因是___________ 。C60的晶胞与干冰的晶胞相似,已知该晶胞的密度为ρg·cm-3,则两个最近C60分子间的距离为___________ nm(列出计算式,已知阿伏伽德罗常数的值为NA)。

(1)某太阳能吸热涂层以镍或镍合金空心球为吸收剂,基态镍原子的价层电子排布式是
(2)硼及其化合物广泛应用于永磁材料、超导材料等领域,硼可以与氟气反应生成BF3气体,BF3分子的立体构型为
(3)石墨的晶体结构如图所示,如图虚线勾勒出的是其晶胞。则石墨晶胞含碳原子个数

(4)石墨烯(图甲〕是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(图乙)

图乙中,1号C的杂化方式是
(5)有机太阳能固体电池材料含有高纯度C60,其分子结构如图,1molC分子中π键的数目为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】铁及其化合物在生产生活及科研中应用广泛。
(1)聚合硫酸铁的化学式为[ ]m,是常用的水处理剂。基态铁原子的核外电子排布式为
]m,是常用的水处理剂。基态铁原子的核外电子排布式为___________ ,聚合硫酸铁中铁元素阳离子有_________ 个未成对电子。
(2)Fe3+、Co3+与N3-、CN-等可形成络合离子。
①K3[Fe(CN)6]可用于检验Fe2+,配体CN-中碳原子杂化轨道类型为_______ ,1mol [Fe(CN)6]3-离子中含有σ键的数目为__________ 。
②已知N3-与CS2为等电子体,则N3-的空间构型为_________ 。
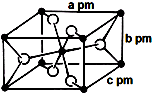
(3)氟化亚铁晶胞属于四方晶系,其长方体结构如图所示,根据图中所示数据计算该晶体密度ρ=_________ g·cm-3。(列出计算式即可)(1pm=10-12m)
(1)聚合硫酸铁的化学式为[
 ]m,是常用的水处理剂。基态铁原子的核外电子排布式为
]m,是常用的水处理剂。基态铁原子的核外电子排布式为(2)Fe3+、Co3+与N3-、CN-等可形成络合离子。
①K3[Fe(CN)6]可用于检验Fe2+,配体CN-中碳原子杂化轨道类型为
②已知N3-与CS2为等电子体,则N3-的空间构型为
(3)氟化亚铁晶胞属于四方晶系,其长方体结构如图所示,根据图中所示数据计算该晶体密度ρ=

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】A、B、C、D是四种短周期主族元素, E位于第四周期。 A的最外层电子数是次外层电子数的2倍, C+与A4-具有相同的电子层结构, D的氧化物为光导纤维的主要成分。 B的简单氢化物的水溶液呈碱性, E与 B同主族。
请完成下列问题:
(1)D元素在周期表中的位置:__________________ 。
(2)B的最简单氢化物化学式为_______ ;D的氢化物稳定性比B的_____ (填“强”或“弱”)。
(3)A与D之间形成的化学键属于___________ (填“离子键”、“极性共价键” 或 “非极性共价键”);C最高价氧化物对应的水化物溶液呈_______ (填“酸性” 、“碱性”或“两性”)。
(4)B、C、D三种元素的原子半径由大到小顺序为_______________ (用元素符号表示)。
(5) E 与锗、硒的第一电离能由小到大的顺序为_____________ (用元素符号表示) 。与A的氧化物(AO)互为等电子体的有______ (写一种即可)。
(6)C的最高价氧化物的水化物与D的氧化物反应的离子方程式:________________ 。
请完成下列问题:
(1)D元素在周期表中的位置:
(2)B的最简单氢化物化学式为
(3)A与D之间形成的化学键属于
(4)B、C、D三种元素的原子半径由大到小顺序为
(5) E 与锗、硒的第一电离能由小到大的顺序为
(6)C的最高价氧化物的水化物与D的氧化物反应的离子方程式:
您最近一年使用:0次
【推荐1】完成下列问题。
(1)在配合物[Cu(NH3)4]SO4中,___________ 是中心离子,提供电子对形成配位键的原子是___________ 。
(2)基态Cr原子的核外电子排布式为___________ 。
(3)下列羧酸:①CF3COOH ②CH3COOH ③CH2FCOOH ④CH2ClCOOH ⑤CH3CH2COOH,酸性由强到弱的顺序为___________ (填标号)。
(4)石墨晶体中横向与纵向的导电性不同,这说明晶体性质表现___________ 。
a.自范性 b.各向异性 c.各向同性
(5)基态硫原子占据最高能级的电子云轮廓图形状为___________ 。
(6)下列有关超分子的说法正确的是_______ 。。
A.超分子是由两个或两个以上分子通过分子间相互作用形成的分子聚集体
B.细胞膜中的磷脂分子的双层膜结构、冠醚与金属离子的聚集体都能看作超分子
C.分离C60和C70时,先是杯酚和C70形成超分子
(7)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,乙图为甲图的俯视图,若A点坐标为(0,0,0),B点坐标为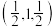 ,则D点坐标为
,则D点坐标为_______ 。

(1)在配合物[Cu(NH3)4]SO4中,
(2)基态Cr原子的核外电子排布式为
(3)下列羧酸:①CF3COOH ②CH3COOH ③CH2FCOOH ④CH2ClCOOH ⑤CH3CH2COOH,酸性由强到弱的顺序为
(4)石墨晶体中横向与纵向的导电性不同,这说明晶体性质表现
a.自范性 b.各向异性 c.各向同性
(5)基态硫原子占据最高能级的电子云轮廓图形状为
(6)下列有关超分子的说法正确的是
A.超分子是由两个或两个以上分子通过分子间相互作用形成的分子聚集体
B.细胞膜中的磷脂分子的双层膜结构、冠醚与金属离子的聚集体都能看作超分子
C.分离C60和C70时,先是杯酚和C70形成超分子
(7)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,乙图为甲图的俯视图,若A点坐标为(0,0,0),B点坐标为
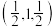 ,则D点坐标为
,则D点坐标为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】硼及其化合物广泛应用于开发新型储氢材料、超导材料、复合材料等高新材料领域。回答下列问题:
(1)硼单质有晶体硼和无定形硼两种,区分二者最可靠的方法为___ 。
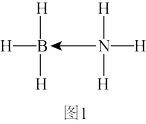
(2)氨硼烷(NH3BH3)是一种新型储氢材料,其分子中与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),结构式如图1。氨硼烷分子含元素中电负性最小的元素是____ (填元素符号,下同)。
(3)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。
①1molNH4BF4含有___ mol配位键。
②NH4BF4中BF 的空间构型为
的空间构型为___ 。
(4)硼酸(H3BO3)是一种结构为片层状的白色晶体。层内的H3BO3分子间通过氢键相连(如图2),H3BO3分子中B的杂化轨道类型为___ ,0.6molH3BO3晶体中有___ mol氢键。硼酸晶体在冷水中溶解度很小,但在热水中溶解度很大原因是___ 。
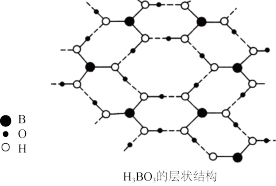
图2
(5)硼氢化钠是一种常用的还原剂,其晶胞结构如图3。
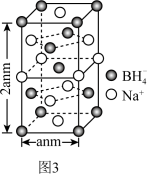
①该晶体中BH 的配位数为
的配位数为___ 。
②设NA为阿伏加德罗常数的值,则硼氢化钠晶体的密度ρ=___ (用含a、NA的最简式表示)g·cm-3。
(1)硼单质有晶体硼和无定形硼两种,区分二者最可靠的方法为
(2)氨硼烷(NH3BH3)是一种新型储氢材料,其分子中与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),结构式如图1。氨硼烷分子含元素中电负性最小的元素是

(3)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。
①1molNH4BF4含有
②NH4BF4中BF
 的空间构型为
的空间构型为(4)硼酸(H3BO3)是一种结构为片层状的白色晶体。层内的H3BO3分子间通过氢键相连(如图2),H3BO3分子中B的杂化轨道类型为

图2
(5)硼氢化钠是一种常用的还原剂,其晶胞结构如图3。

①该晶体中BH
 的配位数为
的配位数为②设NA为阿伏加德罗常数的值,则硼氢化钠晶体的密度ρ=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铜单质及其化合物在很多领域中都有重要的用途。请回答以下问题:
(1)超细铜粉可用作导电材料、催化剂等,其制备方法如下:

①NH4CuSO3中金属阳离子的核外电子排布式为______ 。N、O、S三种元素的第一电离能大小顺序为__________________ (填元素符号)。
②SO42-的空间构型为________ 。
(2)某学生用硫酸铜溶液与氨水做了一组实验,CuSO4溶液中加氨水生成蓝色沉淀,再加氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶体,请解释加入乙醇后析出晶体的原因_________ ;在该晶体中存在的化学键的种类有_________ 。
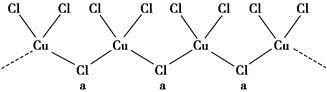
(3)氯和钾与不同价态的铜可生成两种化合物,其阴离子均为无限长链结构(如图所示),a位置上Cl原子的杂化轨道类型为________ 。已知其中一种化合物的化学式为KCuCl3,则另一种化合物的化学式为____________ 。
用晶体的X射线衍射法可以测得阿伏加德罗常数的值。对金属铜的测定得到以下结果:铜晶胞为面心立方最密堆积,边长为361 pm。又知铜的密度为9.00 g·cm-3,则铜原子的直径约为__________ pm,阿伏加德罗常数的值为________ [已知Ar(Cu)=63.5]。
(1)超细铜粉可用作导电材料、催化剂等,其制备方法如下:

①NH4CuSO3中金属阳离子的核外电子排布式为
②SO42-的空间构型为
(2)某学生用硫酸铜溶液与氨水做了一组实验,CuSO4溶液中加氨水生成蓝色沉淀,再加氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶体,请解释加入乙醇后析出晶体的原因
(3)氯和钾与不同价态的铜可生成两种化合物,其阴离子均为无限长链结构(如图所示),a位置上Cl原子的杂化轨道类型为

用晶体的X射线衍射法可以测得阿伏加德罗常数的值。对金属铜的测定得到以下结果:铜晶胞为面心立方最密堆积,边长为361 pm。又知铜的密度为9.00 g·cm-3,则铜原子的直径约为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大,其中基态A原子价电子排布式为nsnnpn;化合物B2E为离子化合物,E原子核外的M层中只有两对成对电子;C元素基态原子没有不成对电子;D单质常用于制作太阳能电池和集成电路芯片;F原子最外层只有1个电子,其余各内层轨道均充满电子。请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):
(1)C的同周期相邻元素的第一电离能由小到大的顺序为______
(2)氢化物A2H4分子中A原子采取______ 杂化
(3)元素F在周期表的位置为______ ,E的气态氢化物通入二价阳离子F2+的水溶液反应的离子方程式为______
(4)元素A和D可形成一种无机非金属材料,其晶体具有很高的硬度和熔点,其化合物中所含的化学键类型为______ (从原子轨道重叠方式看),A、D的最高价氧化物的熔沸点大小顺序_________ ;原因________ 。
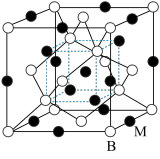
(5)B与同主族原子半径最小的元素M形成的晶胞结构所示的立方晶胞,则其化学式为______ 。设阿伏加 德罗常数为NA,距离最近的两个B、M原子的核间距为a nm,则该化合物的晶胞密度为(用含a和NA的代数式表示)______ g/cm3
(1)C的同周期相邻元素的第一电离能由小到大的顺序为
(2)氢化物A2H4分子中A原子采取
(3)元素F在周期表的位置为
(4)元素A和D可形成一种无机非金属材料,其晶体具有很高的硬度和熔点,其化合物中所含的化学键类型为
(5)B与同主族原子半径最小的元素M形成的晶胞结构所示的立方晶胞,则其化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】2019年4月23日,中国人民军成立70周年。提到海军就不得不提航空母舰,我国正在建造第三艘航空母舰。航母的龙骨要耐冲击,甲板要耐高温,外壳要耐腐蚀.
(1)镍铬钢抗腐蚀性能强,基态C r 原子价层电子的电子排布式为_______________ 。
(2)航母甲板涂有一层耐高温的材料聚硅氧烷(结构如图甲所示)。基态Si原子电子占据最高能级的电子云轮廓图为_______ 形:H、C、O、Si 四种元素中的电负性最高的是______ 。
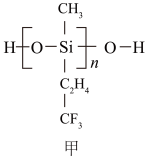
(3)海洋是元素的摇篮,海水中含有大量卤族元素。
①钛卤化物的熔点如下表所示:
解释表中卤化物之间熔点差异的原因是________________________ 。
②OF2的空间构型为___________ ,其中O原子杂化方式为__________ 杂化。
③氯元素可以形成多种含氧酸,其酸性由弱到强的顺序为:HClO <HClO2<HClO3<HClO4。试解释其酸性强弱的原因是_______________ 。
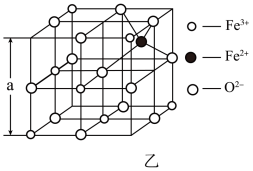
(4)海底金属软泥是在海洋底覆盖着的一层红棕色沉积物,蕴藏大着极的资源,含有硅、氧、锰、锌等。如图是从铁氧体离子晶体Fe3O4中取出的能体现其晶体结构的一个立方体。
①晶体中的氧离子是否构成了面心立方最密堆积?________ (填“是”或“否”);
②已知:Fe3O4晶体的密度为5. 18g•cm -3, 根据该图计算a________ nrn (写出计算式即可,阿伏加 德罗常数的值为N A)
(1)镍铬钢抗腐蚀性能强,基态C r 原子价层电子的电子排布式为
(2)航母甲板涂有一层耐高温的材料聚硅氧烷(结构如图甲所示)。基态Si原子电子占据最高能级的电子云轮廓图为
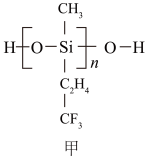
(3)海洋是元素的摇篮,海水中含有大量卤族元素。
①钛卤化物的熔点如下表所示:
| TiF4 | TiCl4 | TiBr4 | TiI4 | |
| 熔点/℃ | 377 | -24 | 38 | 150 |
解释表中卤化物之间熔点差异的原因是
②OF2的空间构型为
③氯元素可以形成多种含氧酸,其酸性由弱到强的顺序为:HClO <HClO2<HClO3<HClO4。试解释其酸性强弱的原因是
(4)海底金属软泥是在海洋底覆盖着的一层红棕色沉积物,蕴藏大着极的资源,含有硅、氧、锰、锌等。如图是从铁氧体离子晶体Fe3O4中取出的能体现其晶体结构的一个立方体。
①晶体中的氧离子是否构成了面心立方最密堆积?
②已知:Fe3O4晶体的密度为5. 18g•cm -3, 根据该图计算a

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】碱土金属指II A族的铍(Be)、镁(Mg)、钙(Ca)、锶(Sr)、钡(Ba)等元素,它们的单质及其化合物有着广泛的用途。
(1)Be基态原子的轨道表示式为_________________________ ;
镁和铝的第二电离能:I2(Mg)_____ I2(Al) (填“>”“ <”或“=”)。
(2)在500~600℃气相中,氯化铍以二聚体Be2Cl4, (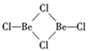 )的形式存在,在1000 ℃,氯化铍则以BeCl2形式存在。
)的形式存在,在1000 ℃,氯化铍则以BeCl2形式存在。
①在二聚体Be2Cl4中Be的杂化方式为___________ ,1mol Be2Cl4中含有_________ mol 配位键。
②MgCl2的熔、沸点比BeCl2高的原因是____________________ 。
(3)根据巴索洛规则:一般来讲,盐中阴、阳离子半径相差较大时,其溶解度较大。则在水中溶解度 S(SrF2)____ S(BaF2) (填“>” “<””或“=”)。
(4)石灰氮(CaCN2)—种碱性肥料,可用作除草剂、杀菌剂、杀虫剂等。
①CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O和________ (填化学式),写出CN22-的电子式___________ 。
②CaCN2与水反应生成CaCO3和NH3两种物质,则1mol CaCN2与水反应的过程中,反应物断裂的σ键总数_______________ 。
(5) Mg2+与Ni2+、 O2-形成晶体的晶胞结构如图所示(Ni2+未画出),则该晶体的化学式为_________ 。已知该晶胞参数a pm.则该晶体的密度为_________ g·cm-3(用a和NA表示)。
(1)Be基态原子的轨道表示式为
镁和铝的第二电离能:I2(Mg)
(2)在500~600℃气相中,氯化铍以二聚体Be2Cl4, (
 )的形式存在,在1000 ℃,氯化铍则以BeCl2形式存在。
)的形式存在,在1000 ℃,氯化铍则以BeCl2形式存在。①在二聚体Be2Cl4中Be的杂化方式为
②MgCl2的熔、沸点比BeCl2高的原因是
(3)根据巴索洛规则:一般来讲,盐中阴、阳离子半径相差较大时,其溶解度较大。则在水中溶解度 S(SrF2)
(4)石灰氮(CaCN2)—种碱性肥料,可用作除草剂、杀菌剂、杀虫剂等。
①CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O和
②CaCN2与水反应生成CaCO3和NH3两种物质,则1mol CaCN2与水反应的过程中,反应物断裂的σ键总数
(5) Mg2+与Ni2+、 O2-形成晶体的晶胞结构如图所示(Ni2+未画出),则该晶体的化学式为

您最近一年使用:0次



