硼及其化合物广泛应用于开发新型储氢材料、超导材料、复合材料等高新材料领域。回答下列问题:
(1)硼单质有晶体硼和无定形硼两种,区分二者最可靠的方法为___ 。
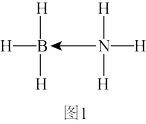
(2)氨硼烷(NH3BH3)是一种新型储氢材料,其分子中与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),结构式如图1。氨硼烷分子含元素中电负性最小的元素是____ (填元素符号,下同)。
(3)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。
①1molNH4BF4含有___ mol配位键。
②NH4BF4中BF 的空间构型为
的空间构型为___ 。
(4)硼酸(H3BO3)是一种结构为片层状的白色晶体。层内的H3BO3分子间通过氢键相连(如图2),H3BO3分子中B的杂化轨道类型为___ ,0.6molH3BO3晶体中有___ mol氢键。硼酸晶体在冷水中溶解度很小,但在热水中溶解度很大原因是___ 。
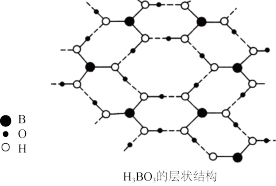
图2
(5)硼氢化钠是一种常用的还原剂,其晶胞结构如图3。
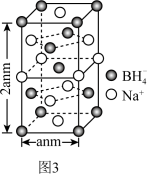
①该晶体中BH 的配位数为
的配位数为___ 。
②设NA为阿伏加德罗常数的值,则硼氢化钠晶体的密度ρ=___ (用含a、NA的最简式表示)g·cm-3。
(1)硼单质有晶体硼和无定形硼两种,区分二者最可靠的方法为
(2)氨硼烷(NH3BH3)是一种新型储氢材料,其分子中与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),结构式如图1。氨硼烷分子含元素中电负性最小的元素是

(3)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。
①1molNH4BF4含有
②NH4BF4中BF
 的空间构型为
的空间构型为(4)硼酸(H3BO3)是一种结构为片层状的白色晶体。层内的H3BO3分子间通过氢键相连(如图2),H3BO3分子中B的杂化轨道类型为

图2
(5)硼氢化钠是一种常用的还原剂,其晶胞结构如图3。

①该晶体中BH
 的配位数为
的配位数为②设NA为阿伏加德罗常数的值,则硼氢化钠晶体的密度ρ=
更新时间:2021-11-26 12:16:34
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E五种元素的原子序数依次递增。已知:
①A原子有3个能级且各能级电子数相等;
②B原子的核外L层电子数为奇数;
③C原子最外层p能级上有2个未成对电子;
④D原子外围电子排布式为 (m≠n);
(m≠n);
⑤E的基态原子的M能层全充满,N能层没有成对电子,只有一个未成对电子。
请回答下列问题:
(1)基态D原子中,电子占据的最高能层符号为_______ ,电子占据的最高能级在空间共有_______ 种不同方向的轨道,它在元素周期表中属于_______ 区元素。
(2)A、B、C、D四种元素电负性由大到小的顺序为_______ 。(填元素符号)。
(3)A、B、D的最高价氧化物对应的水化物的酸性由弱到强的顺序为_______ 。
(4)前四种元素中,电负性最大与最小的两种元素形成的化合物是_______ 。
(5)E的单质能与B的最高价氧化物对应的水化物的稀溶液发生反应,若反应过程中转移0.3mol电子,则需要消耗E单质的质量是_______ 。
①A原子有3个能级且各能级电子数相等;
②B原子的核外L层电子数为奇数;
③C原子最外层p能级上有2个未成对电子;
④D原子外围电子排布式为
 (m≠n);
(m≠n);⑤E的基态原子的M能层全充满,N能层没有成对电子,只有一个未成对电子。
请回答下列问题:
(1)基态D原子中,电子占据的最高能层符号为
(2)A、B、C、D四种元素电负性由大到小的顺序为
(3)A、B、D的最高价氧化物对应的水化物的酸性由弱到强的顺序为
(4)前四种元素中,电负性最大与最小的两种元素形成的化合物是
(5)E的单质能与B的最高价氧化物对应的水化物的稀溶液发生反应,若反应过程中转移0.3mol电子,则需要消耗E单质的质量是
您最近一年使用:0次
【推荐2】丁二酮肟(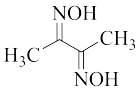 )可与
)可与 反应,生成鲜红色的沉淀丁二酮肟镍,这个反应可用来鉴定
反应,生成鲜红色的沉淀丁二酮肟镍,这个反应可用来鉴定 的存在。请回答下列问题:
的存在。请回答下列问题:
(1)Ni在元素周期表中的位置为___________ 。
(2)基态氧原子的核外电子的运动状态有___________ 种。
(3)丁二酮肟(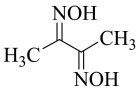 )中涉及元素的电负性由大到小的顺序为
)中涉及元素的电负性由大到小的顺序为___________ ;与氮同周期的硼在成键时,能将一个 电子激发进入
电子激发进入 能级参与形成化学键,请写出该激发态原子的价电子轨道表示式:
能级参与形成化学键,请写出该激发态原子的价电子轨道表示式:___________ ,该过程形成的原子光谱为___________ (填“吸收”或“发射”)光谱。
(4)与Ni同周期的铜、锌两种元素位于元素周期表的___________ 区,两元素的第一电离能 、第二电离能
、第二电离能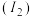 数据如表所示:
数据如表所示:
铜的 小于锌,
小于锌, 却大于锌的主要原因是
却大于锌的主要原因是___________ 。
 )可与
)可与 反应,生成鲜红色的沉淀丁二酮肟镍,这个反应可用来鉴定
反应,生成鲜红色的沉淀丁二酮肟镍,这个反应可用来鉴定 的存在。请回答下列问题:
的存在。请回答下列问题:(1)Ni在元素周期表中的位置为
(2)基态氧原子的核外电子的运动状态有
(3)丁二酮肟(
 )中涉及元素的电负性由大到小的顺序为
)中涉及元素的电负性由大到小的顺序为 电子激发进入
电子激发进入 能级参与形成化学键,请写出该激发态原子的价电子轨道表示式:
能级参与形成化学键,请写出该激发态原子的价电子轨道表示式:(4)与Ni同周期的铜、锌两种元素位于元素周期表的
 、第二电离能
、第二电离能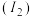 数据如表所示:
数据如表所示:电离能 |  |  |
| 铜 | 746 | 1958 |
| 锌 | 906 | 1733 |
 小于锌,
小于锌, 却大于锌的主要原因是
却大于锌的主要原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】向CoCl2溶液中滴加过量的氨水得到含有[Co(NH3)6]Cl2的溶液。
(1)基态Co2+的电子排布式为___________ 。
(2)O、N、H的电负性由大到小的顺序是___________ 。
(3)下列状态的氮中,电离最外层一个电子所需能量最小的是___________ (填序号)。
a.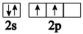 b.
b.  c.
c.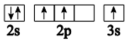
(4)[Co(NH3)6]Cl2 的晶胞结构示意图如下。

①在下图虚线框内画出[Co(NH3)6]2+中一个NH3的结构式___________ 。
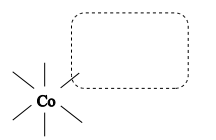
②比较H- N-H键角: NH3___________ [Co(NH3)6]2+ (填“>”“<”或“=”) ,原因是___________ 。
③该立方晶胞的边长为a pm,阿伏加德罗常数为NA, [Co(NH3)6]Cl2的摩尔质量为M g/mol,则该晶体的密度为____________ g/cm3。
(1)基态Co2+的电子排布式为
(2)O、N、H的电负性由大到小的顺序是
(3)下列状态的氮中,电离最外层一个电子所需能量最小的是
a.
 b.
b.  c.
c.
(4)[Co(NH3)6]Cl2 的晶胞结构示意图如下。

①在下图虚线框内画出[Co(NH3)6]2+中一个NH3的结构式

②比较H- N-H键角: NH3
③该立方晶胞的边长为a pm,阿伏加德罗常数为NA, [Co(NH3)6]Cl2的摩尔质量为M g/mol,则该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】下表为长式周期表的一部分,其中的编号代表对应的元素。
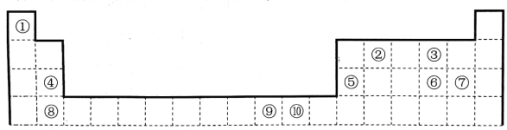
请回答下列问题:
(1)元素⑨的基态原子的价电子排布式为_________________ 。
(2)这10种元素,其中电负性最大的是________ (填元素符号)。
(3)元素②的一种氢化物(分子中含有6个原子) 是重要的化工原料,常把该氢化物的产 量作为衡量石油化工发展水平的标志。有关该氢化物分子的说法正确的是________ 。
A.6个原子不在同一平面上 B.属于含有极性键的非极性分子
C.只含有4个sp2-s的δ键和1个P-P的π键 D.该氢化物分子中C原子采用sp2杂化
(4)下图所示为血红蛋白和肌红蛋白的活性部分(血红素) 的结构式。此结构片段中含有的化学键有________ (填序号)。

A.离子键 B.金属键 C.极性键 D.非极性键 E.配位键 G. δ键 H.Π键
(5)下表为原子序数依次增大的短周期元素A~F的第一到第五电离能数据。

请回答:表中的D、E、F可能是哪三种元素__________ (填元素符号);若A、B、C为原子序数依次增大的同周期相邻元素,表中显示B比A和C 的第一电离能都略大,其原因是__________ 。

请回答下列问题:
(1)元素⑨的基态原子的价电子排布式为
(2)这10种元素,其中电负性最大的是
(3)元素②的一种氢化物(分子中含有6个原子) 是重要的化工原料,常把该氢化物的产 量作为衡量石油化工发展水平的标志。有关该氢化物分子的说法正确的是
A.6个原子不在同一平面上 B.属于含有极性键的非极性分子
C.只含有4个sp2-s的δ键和1个P-P的π键 D.该氢化物分子中C原子采用sp2杂化
(4)下图所示为血红蛋白和肌红蛋白的活性部分(血红素) 的结构式。此结构片段中含有的化学键有

A.离子键 B.金属键 C.极性键 D.非极性键 E.配位键 G. δ键 H.Π键
(5)下表为原子序数依次增大的短周期元素A~F的第一到第五电离能数据。

请回答:表中的D、E、F可能是哪三种元素
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】钛被誉为“21世纪的金属”,可呈现多种化合价。其中以+4价的Ti最为稳定。
(1)基态Ti原子的价电子轨道表示式为_______________ 。
(2)已知电离能:I2(Ti)=1310kJ/mol,I2(K)=3051kJ/mol。I2(Ti)<I2(K),其原因为________ 。
(3)钛某配合物可用于催化环烯烃聚合,其结如图所示:
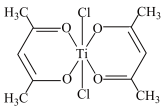
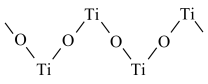
①钛的配位数为_____ ,碳原子的杂化类型_____ 。
②该配合物中存在的化学键有___________ (填字母标号)。
a.离子键 b.配位键 c.金属键 d.共价键 e.氢键
(4)已知TiO2与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如上图所示,该阳离子化学式为________ ,阴离子SO42—的空间构型为____ 。
(5)钛与卤素形成的化合物熔沸点如下表所示:
分析 TiCl4、TiBr4、TiI4的熔点和沸点呈现一定变化规律的原因是:_____ 。
(6)已知TiN晶体的晶胞结构如下图所示,若该晶胞的密度ρg/cm3,阿伏加 德罗常数值为NA,则晶胞中Ti原子与N原子的最近距离为________ pm.(用含ρ、NA的代数式表示)
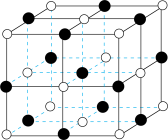
(1)基态Ti原子的价电子轨道表示式为
(2)已知电离能:I2(Ti)=1310kJ/mol,I2(K)=3051kJ/mol。I2(Ti)<I2(K),其原因为
(3)钛某配合物可用于催化环烯烃聚合,其结如图所示:


①钛的配位数为
②该配合物中存在的化学键有
a.离子键 b.配位键 c.金属键 d.共价键 e.氢键
(4)已知TiO2与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如上图所示,该阳离子化学式为
(5)钛与卤素形成的化合物熔沸点如下表所示:
| TiCl4 | TiBr4 | TiI4 | |
| 熔点/℃ | ﹣24.1 | 38.3 | 155 |
| 沸点/℃ | 136.5 | 233.5 | 377 |
分析 TiCl4、TiBr4、TiI4的熔点和沸点呈现一定变化规律的原因是:
(6)已知TiN晶体的晶胞结构如下图所示,若该晶胞的密度ρg/cm3,阿伏加 德罗常数值为NA,则晶胞中Ti原子与N原子的最近距离为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】铜是人体不可缺少的微量元素之一,但铜摄入过量又会导致中毒。
(1)基态Cu原子的价层电子排布式为________
(2)向CuSO4溶液中逐滴加入氨水,经历沉淀析出、沉淀溶解过程。当沉淀完全溶解后,再向其中加入乙醇,可得到深蓝色晶体[Cu(NH3)4]SO4· H2O。该晶体的阴离子立体构型为________ 。氨(NH3)和膦(PH3) 均为三角锥形分子,其中,H-N-H键角为107°,H-P-H键角为93.6°,试分析PH3的键角小于NH3的原因_______ 。氨的沸点_______ (填“高于”或“低于”)膦,请解释原因________ 。
(3) D-青霉胺(β, β-二甲基半胱氨酸)的结构如图所示,可作为药物用于治疗或控制铜中毒病症,其中的碳原子的杂化方式为______ ; 其组成元素中,第二周期的三种元素的电负性由大到小的顺序为_________ 。第一电离能(I1)由大到小的顺序为________________ 。

(4)晶体Cu的晶胞结构如图所示,若晶胞参数为a nm,则晶体密度为_____ g.cm-3 (NA代表阿伏加 德罗常数的值)。
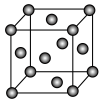
(1)基态Cu原子的价层电子排布式为
(2)向CuSO4溶液中逐滴加入氨水,经历沉淀析出、沉淀溶解过程。当沉淀完全溶解后,再向其中加入乙醇,可得到深蓝色晶体[Cu(NH3)4]SO4· H2O。该晶体的阴离子立体构型为
(3) D-青霉胺(β, β-二甲基半胱氨酸)的结构如图所示,可作为药物用于治疗或控制铜中毒病症,其中的碳原子的杂化方式为

(4)晶体Cu的晶胞结构如图所示,若晶胞参数为a nm,则晶体密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】镁、铜等金属离子是人体内多种酶的辅因子。工业上从海水中提取镁时,先制备无水氯化镁,然后将其熔融电解,得到金属镁。
(1)以MgCl2为原料用熔融盐电解法制备镁时,常加入NaCl、KCl或CaCl2等金属氯化物,其主要作用除了降低熔点之外还有___________ 。
(2)已知MgO的晶体结构属于NaCl型。某同学画出的MgO晶胞结构示意图如下图所示,请改正图中错误:___________ 。___________ 。
(4)Mg是第三周期元素,该周期部分元素氟化物的熔点见下表:
解释表中氟化物熔点差异的原因:___________ 。
(5)人工模拟是当前研究的热点。有研究表明,化合物X可用于研究模拟酶,当其结合 或Cu(I)(I表示化合价为+1)时,分别形成a和b:
或Cu(I)(I表示化合价为+1)时,分别形成a和b:___________ 键的特性。
②微粒间的相互作用包括化学键和分子间相互作用,比较a和b中微粒间相互作用力的差异___________ 。
(1)以MgCl2为原料用熔融盐电解法制备镁时,常加入NaCl、KCl或CaCl2等金属氯化物,其主要作用除了降低熔点之外还有
(2)已知MgO的晶体结构属于NaCl型。某同学画出的MgO晶胞结构示意图如下图所示,请改正图中错误:
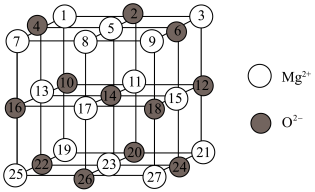
(4)Mg是第三周期元素,该周期部分元素氟化物的熔点见下表:

| 氧化物 | NaF | MgF2 | SiF4 |
| 熔点/K | 1266 | 1534 | 183 |
(5)人工模拟是当前研究的热点。有研究表明,化合物X可用于研究模拟酶,当其结合
 或Cu(I)(I表示化合价为+1)时,分别形成a和b:
或Cu(I)(I表示化合价为+1)时,分别形成a和b: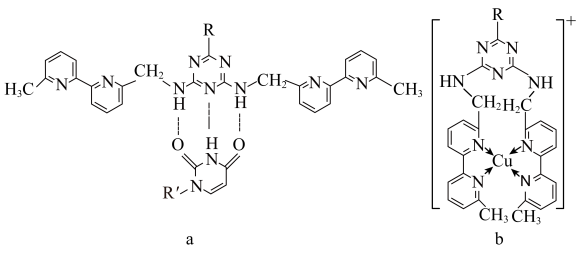
②微粒间的相互作用包括化学键和分子间相互作用,比较a和b中微粒间相互作用力的差异
您最近一年使用:0次
【推荐2】2019年诺贝尔化学奖授予三位开发锂离子电池的科学家。锂离子电池是指以锂离子嵌入化合物为正极材料的电池。研究锂离子电池的电极材料、电解液具有重要的现实意义。请回答下列问题。
(1)锂离子电池的正极材料大多采用橄榄石型的LiMPO4(M=Fe、Co等元素)。
① Li+能量最低的激发态的轨道表示式为___________ ;
② 在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是___________ ;
③ Co3+的一种配离子[Co(N3)(NH3)5]2+中,Co3+的配位数是___________ 。CoO的熔点是1935 ℃,CoS的熔点是1135 ℃,试分析CoO的熔点较高的原因___________ 。
(2)锂离子电池的电解液有LiBF4等,碳酸亚乙酯( )用作该电解液的添加剂。
)用作该电解液的添加剂。
① LiBF4中阴离子的立体构型为___________ ;
② 碳酸亚乙酯分子中σ键和π键的个数比是___________ 。
(3)硫化锂是目前正在研发的锂离子电池的新型固体电解质,为立方晶系晶体,其晶胞参数为a pm。该晶胞中离子的分数坐标为:
硫离子:(0,0,0);( ,
, ,0);(
,0);( ,0,
,0, );(0,
);(0, ,
, );……
);……
锂离子:( ,
, ,
, );(
);( ,
, ,
, );(
);( ,
, ,
, );(
);( ,
, ,
, );……
);……
①在图上画出硫化锂晶胞沿x轴投影的俯视图___________ ;
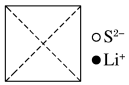
②硫离子的配位数为___________ ;
③设NA为阿伏加德罗常数的值,硫化锂的晶体密度为___________ g·cm-3(列出计算表达式)。
(1)锂离子电池的正极材料大多采用橄榄石型的LiMPO4(M=Fe、Co等元素)。
① Li+能量最低的激发态的轨道表示式为
② 在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是
③ Co3+的一种配离子[Co(N3)(NH3)5]2+中,Co3+的配位数是
(2)锂离子电池的电解液有LiBF4等,碳酸亚乙酯(
 )用作该电解液的添加剂。
)用作该电解液的添加剂。① LiBF4中阴离子的立体构型为
② 碳酸亚乙酯分子中σ键和π键的个数比是
(3)硫化锂是目前正在研发的锂离子电池的新型固体电解质,为立方晶系晶体,其晶胞参数为a pm。该晶胞中离子的分数坐标为:
硫离子:(0,0,0);(
 ,
, ,0);(
,0);( ,0,
,0, );(0,
);(0, ,
, );……
);……锂离子:(
 ,
, ,
, );(
);( ,
, ,
, );(
);( ,
, ,
, );(
);( ,
, ,
, );……
);……①在图上画出硫化锂晶胞沿x轴投影的俯视图

②硫离子的配位数为
③设NA为阿伏加德罗常数的值,硫化锂的晶体密度为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下图是元素周期农中的前四周期,①~⑨为相应的元素,请从中选择合适的元素回答问题:

(1)根据元素原子的外围电子排布特征,元素周期表可划分为五个区域,①元素位于周期表的_______ 区。
(2)②、⑥两元素形成的化合物的空间构型为_______ ,其中心原子的杂化轨道类型为_______ 。
(3)③、④、⑤的电离能由大到小为_______ (填元素符号,下同),电负性由大到小为_______
(4)写出元素⑧基态原子的电子排布式_______ ;⑧的二价阳离子与过量的④的简单氢化物的水溶液作用生成深蓝色的配离子,该配离子的化学式为_______ 。
(5)元素⑨的氢氧化物不溶于水,但可溶于氨水中,该离子与 间结合的作用力为_______(填正确选项)。
间结合的作用力为_______(填正确选项)。
(6)元素⑦与 可形成的
可形成的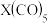 型化合物,该化合物常温下呈液态,熔点为
型化合物,该化合物常温下呈液态,熔点为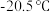 ,沸点为
,沸点为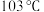 ,易溶于非极性溶剂,据此可判断该化合物晶体属于
,易溶于非极性溶剂,据此可判断该化合物晶体属于_______ 晶体(填晶体类型)。金属⑦的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。面心立方晶胞和体心立方晶胞中实际含有的原子个数之比为_______ ,空间利用率较高的是_______ 堆积方式(填面心立方或体心立方),面心立方晶胞中原子的配位数是_______ 。


(1)根据元素原子的外围电子排布特征,元素周期表可划分为五个区域,①元素位于周期表的
(2)②、⑥两元素形成的化合物的空间构型为
(3)③、④、⑤的电离能由大到小为
(4)写出元素⑧基态原子的电子排布式
(5)元素⑨的氢氧化物不溶于水,但可溶于氨水中,该离子与
 间结合的作用力为_______(填正确选项)。
间结合的作用力为_______(填正确选项)。| A.共价键 | B.离子键 | C.配位键 | D.分子间作用力 |
 可形成的
可形成的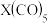 型化合物,该化合物常温下呈液态,熔点为
型化合物,该化合物常温下呈液态,熔点为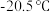 ,沸点为
,沸点为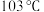 ,易溶于非极性溶剂,据此可判断该化合物晶体属于
,易溶于非极性溶剂,据此可判断该化合物晶体属于
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】钛及其化合物被广泛应用于飞机、火箭、卫星、舰艇、医疗以及石油化工等领域。回答下列问题:
(1)基态Ti原子的核外电子排布式为___________ 。
(2)钛与卤素形成的化合物TiX4熔点如下表:
解释TiX4熔点差异的原因___________ 。
(3) TiCl4能与甲胺(CH3NH2)形成稳定的配合物[TiCl4(CH3NH2)2]。
①甲胺中N原子的杂化方式为___________ 。
②CH3NH2中H-N-H键角比[TiCl4(CH3NH2)2]中H-N-H键角小,从结构角度解释原因___________ 。
(4)TiO2的化学性质非常稳定,广泛用于涂料、橡胶和造纸等工业。
①向TiCl4中加入大量的水,可制得TiO2∙xH2O,该反应的化学方程式为___________ ,所得TiO2∙xH2O经焙烧得到TiO2。
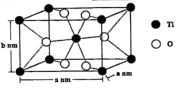
②金红石型TiO2的晶胞为长方体,晶胞参数如图所示。TiO2的摩尔质量为80 g∙mol-1,阿伏加德罗常数为NA,该晶体的密度为___________ g∙cm-3。
(5)Ti(SO4)2是有机合成中常见的催化剂。测定Ti(SO4)2溶液物质的量浓度的方法为:
ⅰ.取5mL待测液于烧杯中,加入足量铝粉,充分反应;
ⅱ.将所得混合物过滤、洗涤,将滤液和洗涤液合并,转移到锥形瓶中,加水稀释到25mL;
ⅲ.向锥形瓶中滴加2滴KSCN溶液;
ⅳ.用cmol/LFe2(SO4)3溶液滴定,滴定终点时消耗Fe2(SO4)3溶液VmL。
已知: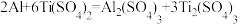
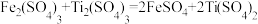
①滴定终点时的现象为___________ 。
②待测液中Ti(SO4)2的浓度为___________  。
。
(1)基态Ti原子的核外电子排布式为
(2)钛与卤素形成的化合物TiX4熔点如下表:
| TiX4 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | -24 | 38.3 | 153 |
(3) TiCl4能与甲胺(CH3NH2)形成稳定的配合物[TiCl4(CH3NH2)2]。
①甲胺中N原子的杂化方式为
②CH3NH2中H-N-H键角比[TiCl4(CH3NH2)2]中H-N-H键角小,从结构角度解释原因
(4)TiO2的化学性质非常稳定,广泛用于涂料、橡胶和造纸等工业。
①向TiCl4中加入大量的水,可制得TiO2∙xH2O,该反应的化学方程式为
②金红石型TiO2的晶胞为长方体,晶胞参数如图所示。TiO2的摩尔质量为80 g∙mol-1,阿伏加德罗常数为NA,该晶体的密度为

(5)Ti(SO4)2是有机合成中常见的催化剂。测定Ti(SO4)2溶液物质的量浓度的方法为:
ⅰ.取5mL待测液于烧杯中,加入足量铝粉,充分反应;
ⅱ.将所得混合物过滤、洗涤,将滤液和洗涤液合并,转移到锥形瓶中,加水稀释到25mL;
ⅲ.向锥形瓶中滴加2滴KSCN溶液;
ⅳ.用cmol/LFe2(SO4)3溶液滴定,滴定终点时消耗Fe2(SO4)3溶液VmL。
已知:
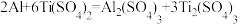
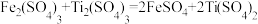
①滴定终点时的现象为
②待测液中Ti(SO4)2的浓度为
 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】锂、铁、铜、锌元素在很多领域有重要应用,回答下列问题:
(1)基态锂原子的电子占据的轨道形状有_____ 种。
(2)基态铁原子的价电子排布式为_____ ,排布时能量最高的电子所占能级的原子轨道有_____ 个伸展方向。
(3)铜的第二电离能_____ (填“”大于“小于”“等于”)锌的第二电离能,原因是_____ 。
(4)LiPF6、LiAsF6和LiCl等可作为聚乙二醇锂离子电池的电极材料。电池放电时,Li+沿聚乙二醇分子中的碳氧链向正极迁移的过程如图所示(图中阴离子未画出)。
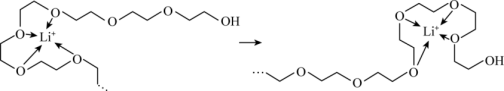
相同条件下,电极材料_____ (填“LiPF6”或“LiAsF6”)中的Li+迁移较快,原因是:_____ 。(从晶体性质角度解释)
(5)[Zn[(NH3)4]2+中,提供电子对形成配位键的原子是_____ ,中心离子的配位数为_____ 。
(6)一种锌的配合物结构简式如图所示,结构中的碳原子有_____ 种杂化方式,其中标注“★”的碳原子为杂化_____ 。

(7)FeO晶体结构与NaCl相似,其中Fe2+的排列方式如图所示。

①Fe2+的配位数为_____ 。
②已知FeO的晶胞参数是a0=0.44nm,则晶胞密度为____ g•cm-3(用含NA的代数式表示,不必化简)。
(1)基态锂原子的电子占据的轨道形状有
(2)基态铁原子的价电子排布式为
(3)铜的第二电离能
(4)LiPF6、LiAsF6和LiCl等可作为聚乙二醇锂离子电池的电极材料。电池放电时,Li+沿聚乙二醇分子中的碳氧链向正极迁移的过程如图所示(图中阴离子未画出)。

相同条件下,电极材料
(5)[Zn[(NH3)4]2+中,提供电子对形成配位键的原子是
(6)一种锌的配合物结构简式如图所示,结构中的碳原子有

(7)FeO晶体结构与NaCl相似,其中Fe2+的排列方式如图所示。

①Fe2+的配位数为
②已知FeO的晶胞参数是a0=0.44nm,则晶胞密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】2021年10月18日《自然•化学》发表我国科学家研究成果,发现AgCrS2(AMX2家族成员之一,A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题:
(1)基态硫原子核外最多有___________ 个电子顺时针旋转。基态铬原子有___________ 种电子运动状态。
(2)氧族元素有氧、硫、硒、碲等元素。这四种元素中,电负性最大的是___________ (填元素符号)。科学家用亚硒酸盐和硫酸盐跟踪固氮酶,研究反应机理。SeO 中硒的杂化轨道类型是
中硒的杂化轨道类型是___________ ,TeO 的空间结构模型为
的空间结构模型为___________ 。H2O、H2S、H2Se、H2Te的键角由大到小的顺序为___________ 。
(3)配合物[Cr(OH)3(H2O)(en)](en为H2NCH2CH2NH2)的中心离子配位数为___________ (Cr与O、N均形成了配位键),1mol该配合物中含___________ molσ键。
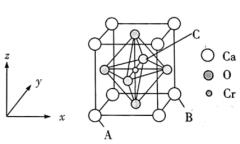
(4)复合材料氧铬酸钙的立方晶胞如图所示。已知A、B的原子坐标分别为(0,0,0)、(1,1,0),则C的原子坐标为___________ ,1个钙原子与___________ 个氧原子等距离且最近,已知钙和氧的最近距离为apm,则该晶体的密度为___________ g/cm3 (列出计算式即可)
(1)基态硫原子核外最多有
(2)氧族元素有氧、硫、硒、碲等元素。这四种元素中,电负性最大的是
 中硒的杂化轨道类型是
中硒的杂化轨道类型是 的空间结构模型为
的空间结构模型为(3)配合物[Cr(OH)3(H2O)(en)](en为H2NCH2CH2NH2)的中心离子配位数为
(4)复合材料氧铬酸钙的立方晶胞如图所示。已知A、B的原子坐标分别为(0,0,0)、(1,1,0),则C的原子坐标为

您最近一年使用:0次



