2019年4月23日,中国人民军成立70周年。提到海军就不得不提航空母舰,我国正在建造第三艘航空母舰。航母的龙骨要耐冲击,甲板要耐高温,外壳要耐腐蚀.
(1)镍铬钢抗腐蚀性能强,基态C r 原子价层电子的电子排布式为_______________ 。
(2)航母甲板涂有一层耐高温的材料聚硅氧烷(结构如图甲所示)。基态Si原子电子占据最高能级的电子云轮廓图为_______ 形:H、C、O、Si 四种元素中的电负性最高的是______ 。
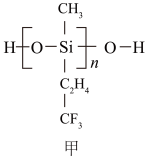
(3)海洋是元素的摇篮,海水中含有大量卤族元素。
①钛卤化物的熔点如下表所示:
解释表中卤化物之间熔点差异的原因是________________________ 。
②OF2的空间构型为___________ ,其中O原子杂化方式为__________ 杂化。
③氯元素可以形成多种含氧酸,其酸性由弱到强的顺序为:HClO <HClO2<HClO3<HClO4。试解释其酸性强弱的原因是_______________ 。
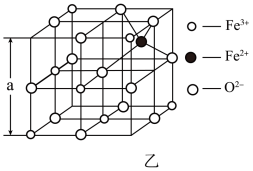
(4)海底金属软泥是在海洋底覆盖着的一层红棕色沉积物,蕴藏大着极的资源,含有硅、氧、锰、锌等。如图是从铁氧体离子晶体Fe3O4中取出的能体现其晶体结构的一个立方体。
①晶体中的氧离子是否构成了面心立方最密堆积?________ (填“是”或“否”);
②已知:Fe3O4晶体的密度为5. 18g•cm -3, 根据该图计算a________ nrn (写出计算式即可,阿伏加 德罗常数的值为N A)
(1)镍铬钢抗腐蚀性能强,基态C r 原子价层电子的电子排布式为
(2)航母甲板涂有一层耐高温的材料聚硅氧烷(结构如图甲所示)。基态Si原子电子占据最高能级的电子云轮廓图为
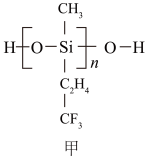
(3)海洋是元素的摇篮,海水中含有大量卤族元素。
①钛卤化物的熔点如下表所示:
| TiF4 | TiCl4 | TiBr4 | TiI4 | |
| 熔点/℃ | 377 | -24 | 38 | 150 |
解释表中卤化物之间熔点差异的原因是
②OF2的空间构型为
③氯元素可以形成多种含氧酸,其酸性由弱到强的顺序为:HClO <HClO2<HClO3<HClO4。试解释其酸性强弱的原因是
(4)海底金属软泥是在海洋底覆盖着的一层红棕色沉积物,蕴藏大着极的资源,含有硅、氧、锰、锌等。如图是从铁氧体离子晶体Fe3O4中取出的能体现其晶体结构的一个立方体。
①晶体中的氧离子是否构成了面心立方最密堆积?
②已知:Fe3O4晶体的密度为5. 18g•cm -3, 根据该图计算a

更新时间:2020-05-18 18:00:30
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
【推荐1】硅晶体常用作太阳能电池材料。
(1)硅在元素周期表中的位置为___________ ,硅的基态原子的电子排布式为___________ 。
(2)GaAlAs也可作太阳能电池材料,同周期元素As(ⅤA族)的第一电离能___________ Se(ⅥA族)的第一电离能(填“>”“<”或“=”),原因是___________ 。基态Ga原子核外电子占据的最高能级为___________ 。
(3)很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物Ⅰ可与氧化汞生成化合物Ⅱ。

①化合物Ⅲ也是一种汞解毒剂,下列说法正确的有___________ 。
A.在Ⅰ中S原子采取 杂化 B.在Ⅱ中O元素的电负性最大
杂化 B.在Ⅱ中O元素的电负性最大
C.在Ⅲ中C-C-C键角是180° D.在Ⅳ中硫氧键的键能均相等
②汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。化合物Ⅰ与化合物Ⅲ相比,水溶性较好的是___________ 。
③化合物Ⅳ(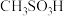 )是一种强酸,写出其电离方程式
)是一种强酸,写出其电离方程式___________ 。
(1)硅在元素周期表中的位置为
(2)GaAlAs也可作太阳能电池材料,同周期元素As(ⅤA族)的第一电离能
(3)很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物Ⅰ可与氧化汞生成化合物Ⅱ。

①化合物Ⅲ也是一种汞解毒剂,下列说法正确的有
A.在Ⅰ中S原子采取
 杂化 B.在Ⅱ中O元素的电负性最大
杂化 B.在Ⅱ中O元素的电负性最大C.在Ⅲ中C-C-C键角是180° D.在Ⅳ中硫氧键的键能均相等
②汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。化合物Ⅰ与化合物Ⅲ相比,水溶性较好的是
③化合物Ⅳ(
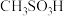 )是一种强酸,写出其电离方程式
)是一种强酸,写出其电离方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】钛被誉为“21世纪的金属”,可呈现多种化合价。其中以+4价的Ti最为稳定。回答下列问题:
(1)基态Ti原子的价电子排布式为___________ ,核外不同空间运动状态的电子数为___________ 种。
(2)已知电离能:I2(Ti)=1310kJ·mol-1,I2(K)=3051kJ·mol-1,I2(Ti)<I2(K),其原因为___________ 。
(3)钛某配合物可用于催化环烯烃聚合,其结构如图所示:

①钛的配位数为___________ ,碳原子的杂化类型有___________ 种。
②该配合物中存在的化学键有___________ (填字母)。
a.离子键 b.配位键 c.金属键 d.共价键 e.氢键
(4)钛与卤素形成的化合物熔、沸点如下表所示:
分析TiCl4、TiBr4、TiI4的熔点和沸点呈现一定变化规律的原因是___________ 。
(5)已知TiN晶体的晶胞结构如下图所示,若该晶胞的密度为ρg·cm-3,阿伏加德罗常数值为NA,则晶胞中Ti原子与N原子的最近距离为___________ pm。(用含ρ、NA的代数式表示)

(1)基态Ti原子的价电子排布式为
(2)已知电离能:I2(Ti)=1310kJ·mol-1,I2(K)=3051kJ·mol-1,I2(Ti)<I2(K),其原因为
(3)钛某配合物可用于催化环烯烃聚合,其结构如图所示:

①钛的配位数为
②该配合物中存在的化学键有
a.离子键 b.配位键 c.金属键 d.共价键 e.氢键
(4)钛与卤素形成的化合物熔、沸点如下表所示:
| TiCl4 | TiBr4 | TiI4 | |
| 熔点/℃ | -24.1 | 38.3 | 155 |
| 沸点/℃ | 136.5 | 233.5 | 377 |
分析TiCl4、TiBr4、TiI4的熔点和沸点呈现一定变化规律的原因是
(5)已知TiN晶体的晶胞结构如下图所示,若该晶胞的密度为ρg·cm-3,阿伏加德罗常数值为NA,则晶胞中Ti原子与N原子的最近距离为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】中国科学家在国际上首次实现了 到淀粉的合成,不依赖植物光合作用,原料只需
到淀粉的合成,不依赖植物光合作用,原料只需 、
、 比和电,相关成果发表在《科学》上。回答下列问题:
比和电,相关成果发表在《科学》上。回答下列问题:
(1) 的空间结构为
的空间结构为_______ 形,基态碳原子的价电子排布式为_______ 。
(2)淀粉遇碘变蓝。单质碘易溶于KI溶液,原因是_______ 。(用离子方程式表示)。
(3)淀粉在一定条件下可水解成葡萄糖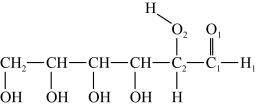 ,葡萄糖分子中键角
,葡萄糖分子中键角
_______ 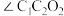 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(4)①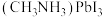 ,的晶胞结构如图所示:
,的晶胞结构如图所示:

其中B代表 。则
。则_______ 代表 ,原子分数坐标A为
,原子分数坐标A为 ,B为
,B为 ,则C的原子分数坐标为
,则C的原子分数坐标为_______ 。
②已知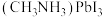 的摩尔质量为M
的摩尔质量为M  ,
, 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为_______  。该晶胞沿体对角线方向的投影图为
。该晶胞沿体对角线方向的投影图为_______ (填选项字母)。
a. b.
b. 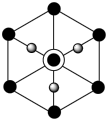 c.
c.  d.
d.
 到淀粉的合成,不依赖植物光合作用,原料只需
到淀粉的合成,不依赖植物光合作用,原料只需 、
、 比和电,相关成果发表在《科学》上。回答下列问题:
比和电,相关成果发表在《科学》上。回答下列问题:(1)
 的空间结构为
的空间结构为(2)淀粉遇碘变蓝。单质碘易溶于KI溶液,原因是
(3)淀粉在一定条件下可水解成葡萄糖
 ,葡萄糖分子中键角
,葡萄糖分子中键角
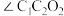 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(4)①
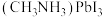 ,的晶胞结构如图所示:
,的晶胞结构如图所示:
其中B代表
 。则
。则 ,原子分数坐标A为
,原子分数坐标A为 ,B为
,B为 ,则C的原子分数坐标为
,则C的原子分数坐标为②已知
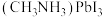 的摩尔质量为M
的摩尔质量为M  ,
, 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为 。该晶胞沿体对角线方向的投影图为
。该晶胞沿体对角线方向的投影图为a.
 b.
b.  c.
c.  d.
d.
您最近一年使用:0次
【推荐1】一种从工业锌置换渣(主要含 等)中回收锗、铅的工艺流程如图:
等)中回收锗、铅的工艺流程如图: 能溶于强酸的浓溶液或强碱溶液;
能溶于强酸的浓溶液或强碱溶液; 可溶于热盐酸中:
可溶于热盐酸中: ;常温下,
;常温下,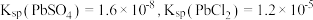 。
。
(1)“还原浸出”时, 的存在可促进
的存在可促进 浸出。
浸出。
① 的空间结构为
的空间结构为___________ 。
②该反应中氧化剂与还原剂的物质的量之比为___________ 。
(2)“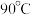 酸浸”所用盐酸的浓度不宜过大或过小,浓度不宜过大的主要原因是
酸浸”所用盐酸的浓度不宜过大或过小,浓度不宜过大的主要原因是___________ 。
(3)“碱溶”时, 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(4)“降温析铅”过程中,体系温度冷却至常温,且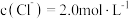 。为防止
。为防止 中混有
中混有 杂质,应控制溶液中
杂质,应控制溶液中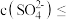
___________ 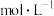 (保留两位有效数字)。
(保留两位有效数字)。
(5)“转化”的意义在于可重复利用___________ (填物质名称)。
(6)通过掺杂硅可将锗单质转化为不同掺杂比例的硅锗合金,锗及硅锗合金的立方晶胞如图所示。 周围与其最近的
周围与其最近的 的个数为
的个数为___________ 。
②若硅锗合金i的晶胞边长为 ,设
,设 为阿伏加德罗常数的值,则硅锗合金i晶体的密度为
为阿伏加德罗常数的值,则硅锗合金i晶体的密度为___________  (列计算式)。
(列计算式)。
③硅锗合金ii沿晶胞对角面取得的截图为___________ (填标号)。
 等)中回收锗、铅的工艺流程如图:
等)中回收锗、铅的工艺流程如图: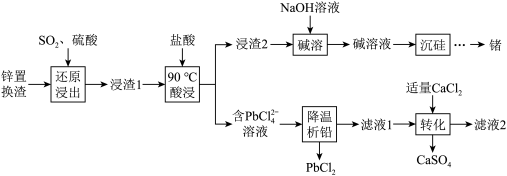
 能溶于强酸的浓溶液或强碱溶液;
能溶于强酸的浓溶液或强碱溶液; 可溶于热盐酸中:
可溶于热盐酸中: ;常温下,
;常温下,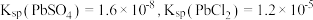 。
。(1)“还原浸出”时,
 的存在可促进
的存在可促进 浸出。
浸出。①
 的空间结构为
的空间结构为②该反应中氧化剂与还原剂的物质的量之比为
(2)“
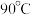 酸浸”所用盐酸的浓度不宜过大或过小,浓度不宜过大的主要原因是
酸浸”所用盐酸的浓度不宜过大或过小,浓度不宜过大的主要原因是(3)“碱溶”时,
 发生反应的离子方程式为
发生反应的离子方程式为(4)“降温析铅”过程中,体系温度冷却至常温,且
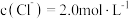 。为防止
。为防止 中混有
中混有 杂质,应控制溶液中
杂质,应控制溶液中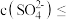
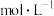 (保留两位有效数字)。
(保留两位有效数字)。(5)“转化”的意义在于可重复利用
(6)通过掺杂硅可将锗单质转化为不同掺杂比例的硅锗合金,锗及硅锗合金的立方晶胞如图所示。
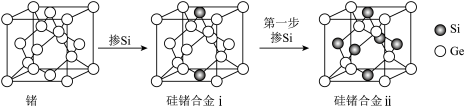
 周围与其最近的
周围与其最近的 的个数为
的个数为②若硅锗合金i的晶胞边长为
 ,设
,设 为阿伏加德罗常数的值,则硅锗合金i晶体的密度为
为阿伏加德罗常数的值,则硅锗合金i晶体的密度为 (列计算式)。
(列计算式)。③硅锗合金ii沿晶胞对角面取得的截图为
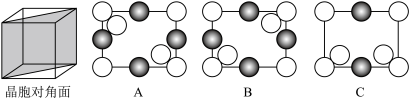
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】为了纪念元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。回答下列问题:
(1)Ag与Cu在同一族,则Ag在周期表中_______ (填“s”、“p”、“d”或“ds”)区。[Ag(NH3)2]+中Ag+空的5s轨道和5p轨道以sp杂化成键,则该配离子的空间构型是_______ 。
(2)表中是Fe和Cu的部分电离能数据:请解释I2(Cu)大于I2(Fe)的主要原因:_______ 。
(3)亚铁氰化钾是食盐中常用的抗结剂,其化学式为K4[Fe(CN)6]。
①CN-的电子式是_______ ;该配离子中配位原子是_______ 。
②该配合物中存在的作用力类型有_______ (填字母)。
A.金属键 B.离子键 C.共价键 D.配位键 E.氢键 F.范德华力
(4)MnO的熔点(1660℃)比MnS的熔点(1610℃)高,其主要原因是_______ 。
(5)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓、硫化镉、硫化锌及铜锢硒薄膜电池等。
①第一电离能:As_______ Se(填“>”、“<”或“=”)。
②硫化锌的晶胞中(结构如图所示),硫离子的配位数是_______ 。
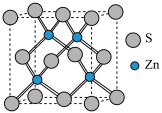
③二氧化硒分子的空间构型为_______ 。
(1)Ag与Cu在同一族,则Ag在周期表中
(2)表中是Fe和Cu的部分电离能数据:请解释I2(Cu)大于I2(Fe)的主要原因:
| 元素 | Fe | Cu |
| 第一电离能I1/kJ·mol-1 | 759 | 746 |
| 第二电离能I2/kJ·mol-1 | 1561 | 1958 |
①CN-的电子式是
②该配合物中存在的作用力类型有
A.金属键 B.离子键 C.共价键 D.配位键 E.氢键 F.范德华力
(4)MnO的熔点(1660℃)比MnS的熔点(1610℃)高,其主要原因是
(5)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓、硫化镉、硫化锌及铜锢硒薄膜电池等。
①第一电离能:As
②硫化锌的晶胞中(结构如图所示),硫离子的配位数是

③二氧化硒分子的空间构型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】实验研究表明,Cu2+本身是无色离子,其化合物或化合物溶液能显现出各种颜色的主要原因是Cu2+形成化合物时,形成了配位键,其配合物显现出各种不同的颜色。如无水硫酸铜中, 不易与Cu2+形成配位键,故无水硫酸铜为白色粉末,无水硫酸铜遇到水蒸气后,H2O与Cu2+形成蓝色的[Cu(H2O)4]2+,白色粉末逐渐变为蓝色。回答下列问题:
不易与Cu2+形成配位键,故无水硫酸铜为白色粉末,无水硫酸铜遇到水蒸气后,H2O与Cu2+形成蓝色的[Cu(H2O)4]2+,白色粉末逐渐变为蓝色。回答下列问题:
(1)基态 Cu2+核外电子排布式为___________ ;铜元素位于元素周期表的___________ 区。
(2)H2O分子中O原子的杂化方式为___________ 杂化;水分子的空间构型为___________ ;根据电负性分析水中氧元素为-2价而氢元素为+1价的原因是___________ 。
(3)1mol[Cu(H2O)4]2+含有___________  共价键,中心原子配位数为
共价键,中心原子配位数为___________ 。
(4)光学原理中,黄色与蓝色的光混合后呈现出绿色。仔细阅读题干信息,推测CuCl2∙2H2O晶体为绿色的原因可能是___________ 。
(5)金属铜的晶胞结构如图所示,已知金属铜的密度为 ,NA表示阿伏加德罗常数的值,则距离最近的两个铜原子之间的距离为
,NA表示阿伏加德罗常数的值,则距离最近的两个铜原子之间的距离为___________  (列出算式即可,不需要化简)。
(列出算式即可,不需要化简)。

 不易与Cu2+形成配位键,故无水硫酸铜为白色粉末,无水硫酸铜遇到水蒸气后,H2O与Cu2+形成蓝色的[Cu(H2O)4]2+,白色粉末逐渐变为蓝色。回答下列问题:
不易与Cu2+形成配位键,故无水硫酸铜为白色粉末,无水硫酸铜遇到水蒸气后,H2O与Cu2+形成蓝色的[Cu(H2O)4]2+,白色粉末逐渐变为蓝色。回答下列问题:(1)基态 Cu2+核外电子排布式为
(2)H2O分子中O原子的杂化方式为
(3)1mol[Cu(H2O)4]2+含有
 共价键,中心原子配位数为
共价键,中心原子配位数为(4)光学原理中,黄色与蓝色的光混合后呈现出绿色。仔细阅读题干信息,推测CuCl2∙2H2O晶体为绿色的原因可能是
(5)金属铜的晶胞结构如图所示,已知金属铜的密度为
 ,NA表示阿伏加德罗常数的值,则距离最近的两个铜原子之间的距离为
,NA表示阿伏加德罗常数的值,则距离最近的两个铜原子之间的距离为 (列出算式即可,不需要化简)。
(列出算式即可,不需要化简)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】(1)Na和O形成的一种只含有离子键的离子化合物的晶胞结构下如下图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为____________ 。

(2)某离子晶体晶胞结构如图所示,X( )位于立方体的顶点,Y(○)位于立方体的中心。试分析:
)位于立方体的顶点,Y(○)位于立方体的中心。试分析:
①晶体中每个Y同时吸引____ 个X。
②该晶体的化学式为_____ 。
③设该晶体的摩尔质量为M g·mol-1,晶体的密度为ρg·cm-3,阿伏伽德罗常数的值为NA,则晶体中两个距离最近的X之间的距离为_________ nm(用含M、ρ、NA的式子表示距离)

(2)某离子晶体晶胞结构如图所示,X(
 )位于立方体的顶点,Y(○)位于立方体的中心。试分析:
)位于立方体的顶点,Y(○)位于立方体的中心。试分析: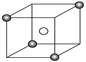
①晶体中每个Y同时吸引
②该晶体的化学式为
③设该晶体的摩尔质量为M g·mol-1,晶体的密度为ρg·cm-3,阿伏伽德罗常数的值为NA,则晶体中两个距离最近的X之间的距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】LiBH4-MgH2-AlH3是一种具有良好释氢性能的三元复合储氢材料。回答下列问题:
(1)下列说法正确的是______ (填标号)。
A.该材料中,五种元素的基态原子都没有成对的p电子
B.该材料中,五种元素的电负性最大的是H
C.Li已无电子可发生跃迁,故Li灼烧时火焰为无色
D.MgH2熔点高于AlH3,原因是Mg2+半径比Al3+小,与H-形成的化学键更强
(2)BH 的空间构型为
的空间构型为______ ,其中B原子的轨道杂化方式为______ 。
(3)LiBH4晶体中含有的微粒间作用力有______ (填标号)。
A.离子键 B.π键 C.氢键 D.配位键
(4)氢化镁(h-MgH2)是一种单层的二维材料,二维晶胞俯视图如图1。
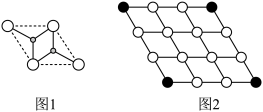
①h-MgH2中,Mg的配位数为______ 。
②3×3×1的h-MgH2晶胞中,涂黑处的Mg被Mn替换,形成掺杂h-MgH2(晶胞如图2所示,H已省略)的化学式为______ 。
(1)下列说法正确的是
A.该材料中,五种元素的基态原子都没有成对的p电子
B.该材料中,五种元素的电负性最大的是H
C.Li已无电子可发生跃迁,故Li灼烧时火焰为无色
D.MgH2熔点高于AlH3,原因是Mg2+半径比Al3+小,与H-形成的化学键更强
(2)BH
 的空间构型为
的空间构型为(3)LiBH4晶体中含有的微粒间作用力有
A.离子键 B.π键 C.氢键 D.配位键
(4)氢化镁(h-MgH2)是一种单层的二维材料,二维晶胞俯视图如图1。

①h-MgH2中,Mg的配位数为
②3×3×1的h-MgH2晶胞中,涂黑处的Mg被Mn替换,形成掺杂h-MgH2(晶胞如图2所示,H已省略)的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)原子形成化合物时,电子云间的相互作用对物质的结构和性质会产生影响。碳原子有4个价电子,在形成化合物时价电子均参与成键,但杂化方式不一定相同。在乙烷、乙烯、乙炔和苯四种分子中,碳原子采取 杂化的是
杂化的是_______ (写结构简式),。试写出一种有机物分子的结构简式,要求同时含有三种不同杂化方式的碳原子:_______ 。
(2)金属钛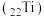 号称航空材料。回答下列问题:
号称航空材料。回答下列问题:
①纳米 是一种应用广泛的催化剂,纳米
是一种应用广泛的催化剂,纳米 催化的一个实例如图所示。
催化的一个实例如图所示。 杂化方式的碳原子个数为
杂化方式的碳原子个数为_______ ,化合物乙中采取 杂化的原子的第一电离能由小到大的顺序为
杂化的原子的第一电离能由小到大的顺序为_______ 。
②有一种氮化钛晶体的晶胞如图所示,该晶体的化学式为_______ ,该晶体中 原子周围距离最近且相等的
原子周围距离最近且相等的 原子的个数为
原子的个数为_______ 。已知晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶胞边长为
,则晶胞边长为_______ (用含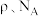 的式子表示)
的式子表示) 。
。
(1)原子形成化合物时,电子云间的相互作用对物质的结构和性质会产生影响。碳原子有4个价电子,在形成化合物时价电子均参与成键,但杂化方式不一定相同。在乙烷、乙烯、乙炔和苯四种分子中,碳原子采取
 杂化的是
杂化的是(2)金属钛
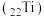 号称航空材料。回答下列问题:
号称航空材料。回答下列问题:①纳米
 是一种应用广泛的催化剂,纳米
是一种应用广泛的催化剂,纳米 催化的一个实例如图所示。
催化的一个实例如图所示。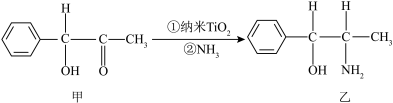
 杂化方式的碳原子个数为
杂化方式的碳原子个数为 杂化的原子的第一电离能由小到大的顺序为
杂化的原子的第一电离能由小到大的顺序为②有一种氮化钛晶体的晶胞如图所示,该晶体的化学式为
 原子周围距离最近且相等的
原子周围距离最近且相等的 原子的个数为
原子的个数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶胞边长为
,则晶胞边长为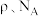 的式子表示)
的式子表示) 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】氮、磷、砷、锑为元素周期表中原子序数依次增大的同族元素。
(1)除 外,科学家还先后研究出了
外,科学家还先后研究出了 、
、 、
、 、高聚氮等氮的单质。
、高聚氮等氮的单质。 为正四面体结构,高聚氮具有空间网状结构,如图所示。
为正四面体结构,高聚氮具有空间网状结构,如图所示。

① 分子是一种
分子是一种_______ (填“极性”或“非极性”)分子。
② 的沸点
的沸点_______ (填“>”、“<”或“=”)高聚氮的沸点,原因是_______ 。
(2)热稳定性:
_______  (填“>”“<”),判断依据是
(填“>”“<”),判断依据是_______ 。
(3) 链状分子中所有原子都满足8电子稳定结构,则其分子中
链状分子中所有原子都满足8电子稳定结构,则其分子中 键与
键与 键之比为
键之比为_______ ,C原子的杂化类型为_______ 。
(1)除
 外,科学家还先后研究出了
外,科学家还先后研究出了 、
、 、
、 、高聚氮等氮的单质。
、高聚氮等氮的单质。 为正四面体结构,高聚氮具有空间网状结构,如图所示。
为正四面体结构,高聚氮具有空间网状结构,如图所示。
①
 分子是一种
分子是一种②
 的沸点
的沸点(2)热稳定性:

 (填“>”“<”),判断依据是
(填“>”“<”),判断依据是(3)
 链状分子中所有原子都满足8电子稳定结构,则其分子中
链状分子中所有原子都满足8电子稳定结构,则其分子中 键与
键与 键之比为
键之比为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用。请回答下列问题。
(1)砷原子核外电子排布式为________________________________________ 。
(2)K3[Fe(CN)6]晶体中Fe3+与CN-之间的键型为_________________ ,该化学键能够形成的原因是_______________________________________________________________ 。
(3)已知:
分析上表中四种物质的相关数据,请回答:
①CH4和SiH4比较,NH3和PH3比较,沸点高低的原因是__________ 。
②CH4和SiH4比较,NH3和PH3比较,分解温度高低的原因是_________ 。
(1)砷原子核外电子排布式为
(2)K3[Fe(CN)6]晶体中Fe3+与CN-之间的键型为
(3)已知:
| CH4 | SiH4 | NH3 | PH3 | |
| 沸点(K) | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度(K) | 873 | 773 | 1073 | 713.2 |
分析上表中四种物质的相关数据,请回答:
①CH4和SiH4比较,NH3和PH3比较,沸点高低的原因是
②CH4和SiH4比较,NH3和PH3比较,分解温度高低的原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】按要求回答下列问题。
(1)氮化镓(GaN)已成为固态射频功率应用领域无可争议的冠军,它在雷达,5G无线领域等方面应用广泛。GaN是坚硬的高熔点材料,熔点约为1700℃,晶体GaN的熔点高于晶体GaAs(熔点1238℃)熔点的原因是_______ 。
(2)下图为钛酸钡晶体的晶胞结构,该晶体经X射线分析得出,重复单元为立方体,顶点位置被Ti4+所占据,体心位置被Ba2+所占据,棱心位置被O2-所占据。写出该晶体的化学式:_______ 。

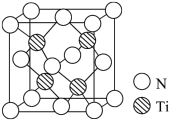
(3)Li2S是目前正在开发的锂离子电池的新型固体电解质,其晶胞结构如下图所示,已知晶胞参数a=588 pm。设NA为阿伏加德罗常数的值,Li2S的晶胞密度为_______ (列出计算式)g·cm-3。
(4)NaCl晶体的晶胞结构如下图所示:
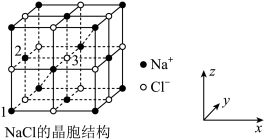
①晶胞中距离1个Na+最近的Cl-有_______ 个,晶胞边长为apm,则相邻Cl-之间的最短距离为_______ pm。(用含a的表达式表示)
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,NaCl晶胞中原子1的坐标为(0,0,0),则原子2的坐标分别为_______ 。
(1)氮化镓(GaN)已成为固态射频功率应用领域无可争议的冠军,它在雷达,5G无线领域等方面应用广泛。GaN是坚硬的高熔点材料,熔点约为1700℃,晶体GaN的熔点高于晶体GaAs(熔点1238℃)熔点的原因是
(2)下图为钛酸钡晶体的晶胞结构,该晶体经X射线分析得出,重复单元为立方体,顶点位置被Ti4+所占据,体心位置被Ba2+所占据,棱心位置被O2-所占据。写出该晶体的化学式:

(3)Li2S是目前正在开发的锂离子电池的新型固体电解质,其晶胞结构如下图所示,已知晶胞参数a=588 pm。设NA为阿伏加德罗常数的值,Li2S的晶胞密度为

(4)NaCl晶体的晶胞结构如下图所示:

①晶胞中距离1个Na+最近的Cl-有
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,NaCl晶胞中原子1的坐标为(0,0,0),则原子2的坐标分别为
您最近一年使用:0次



