现有六种元素,其中A、B、C、D、E为短周期主要族元素,F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)某同学根据上述信息,推断A基态原子的核外最子排布为 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了___________ 。
(2)B元素的电负性_____ (填“大于”、“小于”或“等于”)C元素的电负性。
(3)C与D形成的化合物所含有的化学键类型为_____________ 。
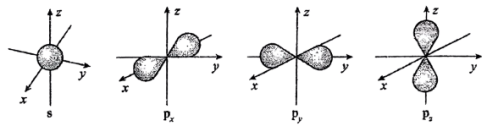
(4)E基态原子中能量最高的电子,其电子云在空间有__________ 个方向。
(5)下列关于F原子的价层电子排布图正确的是___________ 。
a. b.
b.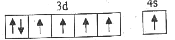
c.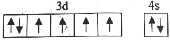 d.
d.
(6)基态F3+离子核外电子排布式为_____________ 。过量单质F与B的最高价氧化物的水化物的稀溶液完全反应,生成BC气体,该反应的离子方程式为____________ 。
(7)元素铜与镍的第二电离能分别为:ICu=1959kJ·mol-1,INi=1753kJ·mol-1,ICu>INi原因是__________________ 。
| A元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
| B元素原子的核外p电子数比s电子数少1 |
| C元素基态原子p轨道有两个未成对电子 |
| D原子的第一至第四电离能分别是: Ⅰ1=738kJ·mol-1;Ⅰ2=1451kJ·mol-1;Ⅰ3=7733kJ·mol-1;Ⅰ4=10540kJ·mol-1; |
| E原子核外所有p轨道全满或半满 |
| F在周期表的第8纵列 |
 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了(2)B元素的电负性
(3)C与D形成的化合物所含有的化学键类型为
(4)E基态原子中能量最高的电子,其电子云在空间有
(5)下列关于F原子的价层电子排布图正确的是
a.
 b.
b.
c.
 d.
d.
(6)基态F3+离子核外电子排布式为
(7)元素铜与镍的第二电离能分别为:ICu=1959kJ·mol-1,INi=1753kJ·mol-1,ICu>INi原因是
更新时间:2018-03-09 16:00:45
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】锗 是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态 原子的核外电子排布式为
原子的核外电子排布式为
______ ,有______ 个未成对电子。
(2)光催化还原 制备
制备 的反应中,带状纳米
的反应中,带状纳米 是该反应的良好催化剂。
是该反应的良好催化剂。 、
、 、
、 电负性由大至小的顺序是
电负性由大至小的顺序是______ 。
(3) 单晶具有金刚石型结构,其中
单晶具有金刚石型结构,其中 原子的杂化方式为
原子的杂化方式为______ ,微粒之间存在的作用力是______ 。
 是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:(1)基态
 原子的核外电子排布式为
原子的核外电子排布式为
(2)光催化还原
 制备
制备 的反应中,带状纳米
的反应中,带状纳米 是该反应的良好催化剂。
是该反应的良好催化剂。 、
、 、
、 电负性由大至小的顺序是
电负性由大至小的顺序是(3)
 单晶具有金刚石型结构,其中
单晶具有金刚石型结构,其中 原子的杂化方式为
原子的杂化方式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】《自然》杂志曾报道我国科学家通过测量 中
中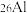 和
和 两种核素的比例确定“北京人”生存年代的研究结果,这种测量方法叫“铝铍测年法”。自然界一共存在三种硅的稳定同位素,分别是
两种核素的比例确定“北京人”生存年代的研究结果,这种测量方法叫“铝铍测年法”。自然界一共存在三种硅的稳定同位素,分别是 。
。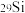 和
和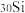 。完成下列填空:
。完成下列填空:
(1)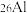 和
和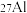 ___________。
___________。
(2)Si原子的结构示意图为___________ 。
(3)基态Si原子能量最高的能层和该能层中电子排布式分别为___________。
(4) 的中子数为
的中子数为___________ ;一个 原子的质量为
原子的质量为___________ g。(用 表示)
表示)
(5)计算硅元素的近似相对原子质量的计算式为: %
% %
% %,其中
%,其中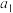 %。
%。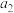 %……指各同位素的
%……指各同位素的___________ 。
(6) 空间结构与
空间结构与 相似,
相似, 分子中存在的化学键
分子中存在的化学键___________ , 空间构型
空间构型___________ 。
A.离子键 B.共价键 C.金属键
(7)向盐酸中逐滴滴加硅酸钠溶液,当pH达到6~7时得到一种乳白色、半透明的分散系,其分散质为粒径在 的
的 粒子。该分散系属于
粒子。该分散系属于___________ 。
A.溶液 B.悬浊液 C.胶体
 中
中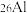 和
和 两种核素的比例确定“北京人”生存年代的研究结果,这种测量方法叫“铝铍测年法”。自然界一共存在三种硅的稳定同位素,分别是
两种核素的比例确定“北京人”生存年代的研究结果,这种测量方法叫“铝铍测年法”。自然界一共存在三种硅的稳定同位素,分别是 。
。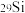 和
和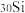 。完成下列填空:
。完成下列填空:(1)
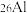 和
和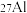 ___________。
___________。| A.是不同核素,具有相同的物理性质 | B.是同一种核素 |
| C.具有相同的中子数 | D.具有相同的化学性质 |
(3)基态Si原子能量最高的能层和该能层中电子排布式分别为___________。
A.K层,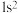 | B.M层,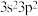 | C.M层,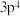 | D.L层,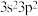 |
 的中子数为
的中子数为 原子的质量为
原子的质量为 表示)
表示)(5)计算硅元素的近似相对原子质量的计算式为:
 %
% %
% %,其中
%,其中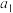 %。
%。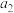 %……指各同位素的
%……指各同位素的(6)
 空间结构与
空间结构与 相似,
相似, 分子中存在的化学键
分子中存在的化学键 空间构型
空间构型A.离子键 B.共价键 C.金属键
(7)向盐酸中逐滴滴加硅酸钠溶液,当pH达到6~7时得到一种乳白色、半透明的分散系,其分散质为粒径在
 的
的 粒子。该分散系属于
粒子。该分散系属于A.溶液 B.悬浊液 C.胶体
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素。M基态原子L层中p轨道电子数是s轨道电子数的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满。
(1)R基态原子的电子排布式是_______ ,X和Y中电负性较大的是______ (填元素符号)。
(2)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1),回答下列各题:
①在周期表中,最可能处于同一族的是___________ 。
A.Q和R B.S和T C.T和U D.R和T E.R和U
②每种元素都出现相邻两个电离能的数据相差较大的情况,这一事实从一个侧面说明:________ ;如果R元素是短周期元素,你估计它的第2次电离能飞跃数据将发生在失去第___________ 个电子时。
③如果R、S、T是同周期的三种主族元素,则它们的原子序数由小到大的顺序是___________ ,其中___________ 元素的第一电离能异常高的原因是___________ 。
(1)R基态原子的电子排布式是
(2)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1),回答下列各题:
元素代号 | I1 | I2 | I3 | I4 |
Q | 2 080 | 4 000 | 6 100 | 9 400 |
R | 500 | 4 600 | 6 900 | 9 500 |
S | 740 | 1 500 | 7 700 | 10 500 |
T | 580 | 1 800 | 2 700 | 11 600 |
U | 420 | 3 100 | 4 400 | 5 900 |
①在周期表中,最可能处于同一族的是
A.Q和R B.S和T C.T和U D.R和T E.R和U
②每种元素都出现相邻两个电离能的数据相差较大的情况,这一事实从一个侧面说明:
③如果R、S、T是同周期的三种主族元素,则它们的原子序数由小到大的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)某元素最高化合价为+5,原子最外层电子数为2,半径是同族中最小 的,其核外电子排布式为______ ,价电子构型为______ ,属________ 区元素。
(2)某元素原子的价电子构型为4s24p1,它属于第________ 周期________ 族,最高正化合价为________ ,元素符号是________ 。
(3)原子序数为24的元素原子中有________ 个电子层,________ 个能级,________ 个未成对电子。
(4)请写出有2个能层的p轨道中只有一个未成对电子的基态原子的外围电子排布图(有几个写几个)________________ 。
(2)某元素原子的价电子构型为4s24p1,它属于第
(3)原子序数为24的元素原子中有
(4)请写出有2个能层的p轨道中只有一个未成对电子的基态原子的外围电子排布图(有几个写几个)
您最近一年使用:0次
【推荐2】㈠镁原子核外有____ 种不同运动状态的电子,____ 种不同能量状态的电子.
㈡A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为_____
(2)B元素的负一价离子的电子层结构与氩相同,B的原子结构示意图为_____
(3)C元素是第三周期中无未成对电子的主族元素,它的电子排布图为_____
(4)D元素基态原子的M层全充满,N层有一个电子,D基态原子的电子排布式为_____
(5)E原子共有3个价电子,其中一个价电子位于第三能层d轨道,指出该元素在周期表中所处的周期数和族序数_____
㈢.用符号“>”“<”或“=”连接下列各项关系.
(1)第一电离能:N_____ O,Mg_____ Ca.
(2)电负性:O_____ F,N_____ P.
(3)能量高低:ns_____ np,4s_____ 3d.
㈡A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为
(2)B元素的负一价离子的电子层结构与氩相同,B的原子结构示意图为
(3)C元素是第三周期中无未成对电子的主族元素,它的电子排布图为
(4)D元素基态原子的M层全充满,N层有一个电子,D基态原子的电子排布式为
(5)E原子共有3个价电子,其中一个价电子位于第三能层d轨道,指出该元素在周期表中所处的周期数和族序数
㈢.用符号“>”“<”或“=”连接下列各项关系.
(1)第一电离能:N
(2)电负性:O
(3)能量高低:ns
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(2019·全国Ⅲ卷)NH4H2PO4中,电负性最高的元素是___________ ;P的杂化方式为___________ ,P的杂化轨道与O的2p轨道形成___________ 键。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)在第二周期中,第一电离能最小的元素符号是______ 。第一电离能最大的元素符号是_____________ 。
(2)在元素周期表中,电负性最大的元素的名称是________ 。
(3)第四周期元素中,基态原子中未成对电子最多的元素原子序数是________ 。
(4)第一电离能关系:N_______ O;铍________ 硼。(填﹥、﹤或 = )
(5)写出34Se的电子排布式____________ 它位于元素周期表的_______ 周期______ 族。
(2)在元素周期表中,电负性最大的元素的名称是
(3)第四周期元素中,基态原子中未成对电子最多的元素原子序数是
(4)第一电离能关系:N
(5)写出34Se的电子排布式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)p电子的原子轨道呈______ 形;
(2)共价键的类型有两种分别是σ键和π键,σ键的对称方式为______ ;
(3)某元素位于元素周期表中第四周期,第VA族,元素符号是______ ,最高价氧化物对应的水化物的化学式______ ;
(4)用“>”或“<”填空:①能量:4p______ 5s ②离子半径:F-______ Na+;
(5)二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构如图所示。

①S2Cl2的结构式为______ ,其化学键类型有______ (填“极性键”“非极性键”或“极性键和非极性键”)。
②电负性:S______ Cl(填“>”或“<”),每个S原子有______ 对孤电子对。
(2)共价键的类型有两种分别是σ键和π键,σ键的对称方式为
(3)某元素位于元素周期表中第四周期,第VA族,元素符号是
(4)用“>”或“<”填空:①能量:4p
(5)二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构如图所示。

①S2Cl2的结构式为
②电负性:S
您最近一年使用:0次

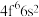 ,则
,则 价层电子排布式为
价层电子排布式为

