298 K时,将20 mL 3x mol·L−1 Na3AsO3、20 mL 3x mol·L−1 I2和20 mL NaOH溶液混合,发生反应: (aq)+I2(aq)+2OH−(aq)
(aq)+I2(aq)+2OH−(aq)
 (aq)+2I−(aq)+ H2O(l)。溶液中c(
(aq)+2I−(aq)+ H2O(l)。溶液中c( )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
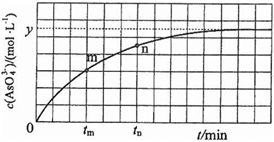
①下列可判断反应达到平衡的是__________ (填标号)。
a.溶液的pH不再变化
b.v(I−)=2v( )
)
c.c( )/c(
)/c( )不再变化
)不再变化
d.c(I−)=y mol·L−1
②tm时,v正_____ v逆(填“大于”“小于”或“等于”)。
 (aq)+I2(aq)+2OH−(aq)
(aq)+I2(aq)+2OH−(aq)
 (aq)+2I−(aq)+ H2O(l)。溶液中c(
(aq)+2I−(aq)+ H2O(l)。溶液中c( )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
①下列可判断反应达到平衡的是
a.溶液的pH不再变化
b.v(I−)=2v(
 )
)c.c(
 )/c(
)/c( )不再变化
)不再变化d.c(I−)=y mol·L−1
②tm时,v正
2018高三下·全国·专题练习 查看更多[1]
(已下线)《考前20天终极攻略》-5月25日 化学反应速率与化学平衡
更新时间:2018-06-15 15:49:05
|
相似题推荐
填空题
|
适中
(0.65)
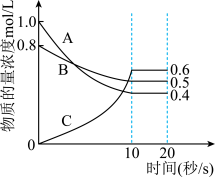
【推荐1】一定条件下,A气体与B气体反应生成C气体。反应过程中,反应物与生成物的浓度随时间变化的曲线如图所示。回答以下问题:_______ ,B气体的反应速率_______ 。
(2)该反应的化学方程式_______ 。
(3)反应后和反应前的压强之比_______ 。
(4)20s时,C气体的体积分数为_______ ,此时v(A)正 _______ v(C)逆(填“>”“<”或“=”)
(5)关于该反应的说法正确的是_______ 。(不定项选择)
a.到达10s时刻时该反应已停止
b.20s时刻时B气体的正反应速率等于逆反应速率
c.10s时刻时之前C气体的消耗速率小于它的生成速率
(2)该反应的化学方程式
(3)反应后和反应前的压强之比
(4)20s时,C气体的体积分数为
(5)关于该反应的说法正确的是
a.到达10s时刻时该反应已停止
b.20s时刻时B气体的正反应速率等于逆反应速率
c.10s时刻时之前C气体的消耗速率小于它的生成速率
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知:2NO2(g) N2O4(g)。在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示:
N2O4(g)。在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示:

(1)25min时,增加了__ (填化学式);
(2)a、b、c、d四个点所表示的反应体系中,气体颜色由深到浅的顺序是___ 。
 N2O4(g)。在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示:
N2O4(g)。在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示:
(1)25min时,增加了
(2)a、b、c、d四个点所表示的反应体系中,气体颜色由深到浅的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】研究化学反应的快慢和限度对人类的生产、生活具有重要意义。在一定条件下,向体积恒为 的密闭容器中通入
的密闭容器中通入 和
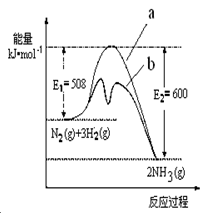
和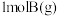 发生反应:
发生反应: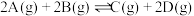 ,测得反应过程中
,测得反应过程中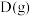 的物质的量分数随时间的变化关系如图:
的物质的量分数随时间的变化关系如图:
(1) 点的
点的
______  点的
点的 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(2) 内,用
内,用 表示的平均反应速率为
表示的平均反应速率为______  。
。
(3)该反应条件下,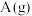 的平衡转化率约为
的平衡转化率约为______ %(保留1位小数)。
(4)测得不同压强下(其他条件不变)上述反应达平衡状态时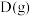 的物质的量分数如图所示。由图可得,影响该反应限度的一个因素是
的物质的量分数如图所示。由图可得,影响该反应限度的一个因素是______ ,为了促进更多的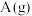 转化为生成物,可采取的措施是
转化为生成物,可采取的措施是______ 。
 的密闭容器中通入
的密闭容器中通入 和
和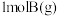 发生反应:
发生反应: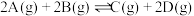 ,测得反应过程中
,测得反应过程中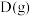 的物质的量分数随时间的变化关系如图:
的物质的量分数随时间的变化关系如图: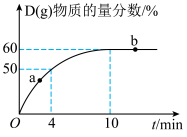
(1)
 点的
点的
 点的
点的 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(2)
 内,用
内,用 表示的平均反应速率为
表示的平均反应速率为 。
。(3)该反应条件下,
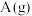 的平衡转化率约为
的平衡转化率约为(4)测得不同压强下(其他条件不变)上述反应达平衡状态时
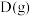 的物质的量分数如图所示。由图可得,影响该反应限度的一个因素是
的物质的量分数如图所示。由图可得,影响该反应限度的一个因素是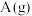 转化为生成物,可采取的措施是
转化为生成物,可采取的措施是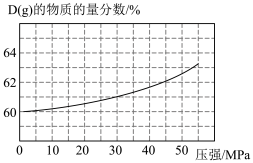
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ、下表是某研究性学习小组探究稀硫酸与金属锌反应的实验数据:
实验数据可发现有一个数据明显有错误,该数据是实验________ (填实验序号),理由是_______________________________________________
Ⅱ、在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g) 2SO3(g) △H<0
2SO3(g) △H<0
(1)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间是___________ 。
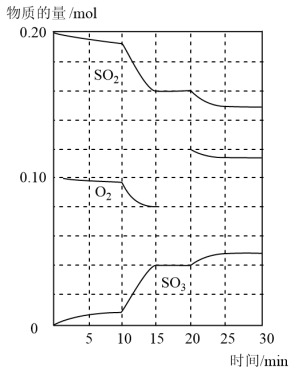
(2)据图判断,反应进行至20min时,曲线发生变化的原因是__________ (用文字表达);10min到15min的曲线变化的原因可能是_____________ (填写编号)。
A. 加了催化剂 B. 缩小容器体积
C. 降低温度 D. 增加SO3的物质的量
| 实验序号 | 金属质量/g | 金属状态 | c(H2SO4)/mol·L-1 | V(H2SO4)/mL | 溶液温度/℃ | 金属消失的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 丝 | 0.5 | 50 | 20 | 34 | 500 |
| 2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
| 3 | 0.10 | 丝 | 0.7 | 50 | 20 | 46 | 250 |
| 4 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
| 5 | 0.10 | 粉末 | 0.8 | 50 | 20 | 36 | 25 |
| 6 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 125 |
| 7 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 | 50 |
| 8 | 0.10 | 丝 | 1.1 | 50 | 20 | 34 | 100 |
| 9 | 0.10 | 丝 | 1.1 | 50 | 35 | 51 | 40 |
实验数据可发现有一个数据明显有错误,该数据是实验
Ⅱ、在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g)
 2SO3(g) △H<0
2SO3(g) △H<0(1)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间是

(2)据图判断,反应进行至20min时,曲线发生变化的原因是
A. 加了催化剂 B. 缩小容器体积
C. 降低温度 D. 增加SO3的物质的量
您最近一年使用:0次
【推荐2】氧、硫、硒、碲都位于元素周期表的VIA族,其化合物在化工生产中有广泛应用。
(1)下列性质的递变顺序不正确的是_____ (填字母)。
A.酸性:H2SeO4>H2SeO3 B.非金属性:O>S>Se>Te
C.还原性:H2Te>H2Se>H2S>H2O D.热稳定性:H2O>H2Te>H2Se>H2S
E.沸点: H2Te>H2Se>H2S>H2O
(2)在常温下进行的置换反应X+W→Y+V中, H2O可以扮演不同的“角色”。已知X、Y是短周期主族元素形成的单质,W、V是化合物。
①若W是水,且作还原剂,反应的化学方程式为_________ 。
②若V是水,为还原产物,反应的化学方程式为_____________ 。
(3) ①一定温度下,向恒容密闭容器中充入一定量的H2S,发生反应H2S(g) S2(g)+2H2(g)。下列情况中,可判断该反应达到平衡状态的是
S2(g)+2H2(g)。下列情况中,可判断该反应达到平衡状态的是_______ (填字母)。
A.混合气体的密度不再变化 B.混合气体的压强不再变化
C.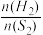 不再变化 D.H2S与H2的消耗速率相等
不再变化 D.H2S与H2的消耗速率相等
②已知:液态CS2完全燃烧生成CO2、SO2气体,每转移3mol电子时放出269.2kJ热量。写出表示CS2(1)的燃烧热的热化学方程式:______________ 。
(4) ①工业上,用S02还原TeC14溶液制备碲(Te),反应中氧化产物与还原产物的物质的量之比为____________ 。
②以石墨为电极,电解强碱性Na2TeO3溶液也可获得碲,电解过程中阴极的电极反应式为_____ ;阳极产生的气体是_____ (填化学式)。
(1)下列性质的递变顺序不正确的是
A.酸性:H2SeO4>H2SeO3 B.非金属性:O>S>Se>Te
C.还原性:H2Te>H2Se>H2S>H2O D.热稳定性:H2O>H2Te>H2Se>H2S
E.沸点: H2Te>H2Se>H2S>H2O
(2)在常温下进行的置换反应X+W→Y+V中, H2O可以扮演不同的“角色”。已知X、Y是短周期主族元素形成的单质,W、V是化合物。
①若W是水,且作还原剂,反应的化学方程式为
②若V是水,为还原产物,反应的化学方程式为
(3) ①一定温度下,向恒容密闭容器中充入一定量的H2S,发生反应H2S(g)
 S2(g)+2H2(g)。下列情况中,可判断该反应达到平衡状态的是
S2(g)+2H2(g)。下列情况中,可判断该反应达到平衡状态的是A.混合气体的密度不再变化 B.混合气体的压强不再变化
C.
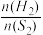 不再变化 D.H2S与H2的消耗速率相等
不再变化 D.H2S与H2的消耗速率相等②已知:液态CS2完全燃烧生成CO2、SO2气体,每转移3mol电子时放出269.2kJ热量。写出表示CS2(1)的燃烧热的热化学方程式:
(4) ①工业上,用S02还原TeC14溶液制备碲(Te),反应中氧化产物与还原产物的物质的量之比为
②以石墨为电极,电解强碱性Na2TeO3溶液也可获得碲,电解过程中阴极的电极反应式为
您最近一年使用:0次