天宫二号空间实验室已于2016 年9月15日22时04分在酒泉卫星发射中心发射成功。请回答下列问题:

(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英玻璃的成分是______ (填化学式)
(2)“碳纤维复合材料制品”应用于“天宫二号”的推进系统。碳纤维复合材料具有重量轻、可设计强度高的特点。碳纤维复合材料由碳纤维和合成树脂组成,其中合成树脂是高分子化合物,则制备合成树脂的反应类型是_____________ 。
(3)太阳能电池帆板是“天宫二号”空间运行的动力源泉,其性能直接影响到“天宫二号”的运行寿命和可靠性。
① 天宫二号使用的光伏太阳能电池,该电池的核心材料是_____ ,其能量转化方式为_____ 。
② 下图是一种全天候太阳能电池的工作原理:
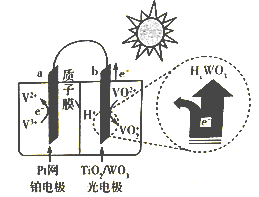
太阳照射时的总反应为V3++ VO2++ H2O=V2++VO2++2H+,则负极反应式为__________ ;夜间时,电池正极为______ (填“a”或“b”)。
(4)太阳能、风能发电逐渐得到广泛应用,下列说法中,正确的是______ ( 填字母序号)。
a.太阳能、风能都是清洁能源
b.太阳能电池组实现了太阳能到电能的转化
c.控制系统能够控制储能系统是充电还是放电
d.阳光或风力充足时,储能系统实现由化学能到电能的转化
(5)含钒废水会造成水体污染,对含钒废水(除VO2+外,还含有Al3+,Fe3+等)进行综合处理可实现钒资源的回收利用,流程如下:
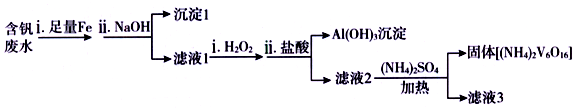
已知溶液pH 范围不同时,钒的存在形式如下表所示:
①加入NaOH 调节溶液pH至13时,沉淀1达最大量,并由灰白色转变为红褐色,用化学用语表示加入NaOH 后生成沉淀1的反应过程为_______ 、_______ ;所得滤液1中,铝元素的存在形式为__________ 。
②向碱性的滤液1 ( V的化合价为+4 )中加入H2O2的作用是________ (用离子方程式表示)。

(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英玻璃的成分是
(2)“碳纤维复合材料制品”应用于“天宫二号”的推进系统。碳纤维复合材料具有重量轻、可设计强度高的特点。碳纤维复合材料由碳纤维和合成树脂组成,其中合成树脂是高分子化合物,则制备合成树脂的反应类型是
(3)太阳能电池帆板是“天宫二号”空间运行的动力源泉,其性能直接影响到“天宫二号”的运行寿命和可靠性。
① 天宫二号使用的光伏太阳能电池,该电池的核心材料是
② 下图是一种全天候太阳能电池的工作原理:

太阳照射时的总反应为V3++ VO2++ H2O=V2++VO2++2H+,则负极反应式为
(4)太阳能、风能发电逐渐得到广泛应用,下列说法中,正确的是
a.太阳能、风能都是清洁能源
b.太阳能电池组实现了太阳能到电能的转化
c.控制系统能够控制储能系统是充电还是放电
d.阳光或风力充足时,储能系统实现由化学能到电能的转化
(5)含钒废水会造成水体污染,对含钒废水(除VO2+外,还含有Al3+,Fe3+等)进行综合处理可实现钒资源的回收利用,流程如下:

已知溶液pH 范围不同时,钒的存在形式如下表所示:
| 钒的化合价 | pH<2 | pH>11 |
| +4价 | VO2+,VO(OH)+ | VO(OH)3- |
| +5价 | VO2+ | VO43- |
①加入NaOH 调节溶液pH至13时,沉淀1达最大量,并由灰白色转变为红褐色,用化学用语表示加入NaOH 后生成沉淀1的反应过程为
②向碱性的滤液1 ( V的化合价为+4 )中加入H2O2的作用是
更新时间:2018-08-16 13:49:14
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】硫酸亚铁铵[(NH4]2Fe(SO4)2]是分析化学中的重要试剂。
[查阅资料]隔绝空气加热至500℃时硫酸亚铁铁铵能完全分解,分解产物中含有铁氧化物、硫氧化物、氨气和水蒸气等。
[实验探究]某化学小组选用下图所示部分装置进行实验(夹持装置略)
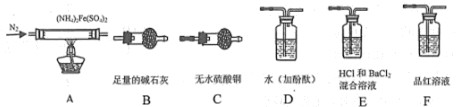
(1)验证分解产物中含有氨气和水蒸气,并探究残留固体成分。
①所选用装置的正确连接顺序为________ (填装置的字母序号)。
②证明有水蒸气生成的实验现象为___________ 。
③证明有氨气生成的实验现象为_______________ 。
④A中固体完全分解后变为红棕色粉末,设计实验证明A中残留固体仅为Fe2O3,而不含FeO或Fe3O4:_________ 。
(2)探究分解产物中的硫氧化物,连接装置A-E-F-B进行实验。
①实验过程中观察到:E中没有明显现象,F中溶液褪色,据此得出的结论是_________ 。
②B的作用是_________ 。
③实验证明(NH4]2Fe(SO4)2受热分解除上述产物外,还有N2生成,写出A中反应的化学方程式__________________ 。
[查阅资料]隔绝空气加热至500℃时硫酸亚铁铁铵能完全分解,分解产物中含有铁氧化物、硫氧化物、氨气和水蒸气等。
[实验探究]某化学小组选用下图所示部分装置进行实验(夹持装置略)

(1)验证分解产物中含有氨气和水蒸气,并探究残留固体成分。
①所选用装置的正确连接顺序为
②证明有水蒸气生成的实验现象为
③证明有氨气生成的实验现象为
④A中固体完全分解后变为红棕色粉末,设计实验证明A中残留固体仅为Fe2O3,而不含FeO或Fe3O4:
(2)探究分解产物中的硫氧化物,连接装置A-E-F-B进行实验。
①实验过程中观察到:E中没有明显现象,F中溶液褪色,据此得出的结论是
②B的作用是
③实验证明(NH4]2Fe(SO4)2受热分解除上述产物外,还有N2生成,写出A中反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知A是一种常见金属,F是一种红褐色沉淀。根据图中转化关系,回答下列问题。
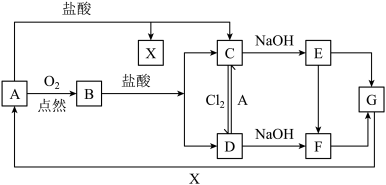
(1)写出F、G的化学式:F.________ ;G._______ 。
(2)检验D中阳离子的方法为_____________________________________________________
(3)保存C溶液时要加固体A的原因是_____________________________________________
(4)写出下列转化的离子方程式:
①B→C:______________________________________________________________________
②C→D:______________________________________________________________________

(1)写出F、G的化学式:F.
(2)检验D中阳离子的方法为
(3)保存C溶液时要加固体A的原因是
(4)写出下列转化的离子方程式:
①B→C:
②C→D:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】中学化学常见物质A、B、C、D、X、Y,存在如下图转化关系(部分物质和条件略去)
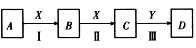
(1)若A为NaOH溶液,X为CO2,D是沉淀,则Y可为________ (填序号)。
A.SO3 B.Ba(OH)2 C.H2SO4 D.CaO
(2)若A为黄铁矿(FeS2),D是H2SO4,则反应Ⅱ的化学方程式为_________________________ 。
(3)若A为溶于水呈碱性的气体,则A与D反应生成的一种化肥的化学式为_____________ ,反应Ⅰ的化学方程式为__________________ ,D的浓溶液与炭反应的化学方程式__________________________ 。
(4)若A和X均为单质,反应Ⅲ的现象是白色沉淀,在空气中迅速变成灰绿色,最后变成红褐色,则反应II的离子方程式为_____________________ 。

(1)若A为NaOH溶液,X为CO2,D是沉淀,则Y可为
A.SO3 B.Ba(OH)2 C.H2SO4 D.CaO
(2)若A为黄铁矿(FeS2),D是H2SO4,则反应Ⅱ的化学方程式为
(3)若A为溶于水呈碱性的气体,则A与D反应生成的一种化肥的化学式为
(4)若A和X均为单质,反应Ⅲ的现象是白色沉淀,在空气中迅速变成灰绿色,最后变成红褐色,则反应II的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】氮和硫的化合物在工农业生产、生活中具有重要应用。请回答下列问题:
(1)航天领域中常用肼
 作为火箭发射的助燃剂。
作为火箭发射的助燃剂。
①已知各共价键键能如下表:
 的结构为
的结构为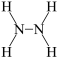 。
。
 ;
;
________  。
。
② 与氨气相似,是一种碱性气体,易溶于水,生成弱碱
与氨气相似,是一种碱性气体,易溶于水,生成弱碱 。用电离方程式表示
。用电离方程式表示 显碱性的原因
显碱性的原因___________ 。
(2)查阅资料可知,常温下,部分弱电解质的电离平衡常数如表:
① 的电离平衡常数的表达式
的电离平衡常数的表达式
___________ ;
②常温下,等浓度的下列溶液a. ;b.
;b. ;c.
;c. ,其
,其 由大到小的顺序是
由大到小的顺序是___________ (用字母表示)。
(3)某同学设计一个肼
 燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中
燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中
 为阳离子交换膜。
为阳离子交换膜。
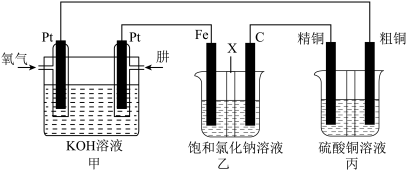
①通入肼的电极为___________ (填“正极”或“负极”),正极的电极反应式为___________ 。
②若甲中有 氧气(标准况下)参加反应,乙中通过离子交换膜的阳离子个数为
氧气(标准况下)参加反应,乙中通过离子交换膜的阳离子个数为___________ ,丙中硫酸铜溶液的浓度___________ (填“变大”、“变小”或“不变”)。
(1)航天领域中常用肼
 作为火箭发射的助燃剂。
作为火箭发射的助燃剂。①已知各共价键键能如下表:
 |  |  |  |  | |
键能 | 946 | 497 | 193 | 391 | 463 |
 的结构为
的结构为 。
。 ;
;
 。
。②
 与氨气相似,是一种碱性气体,易溶于水,生成弱碱
与氨气相似,是一种碱性气体,易溶于水,生成弱碱 。用电离方程式表示
。用电离方程式表示 显碱性的原因
显碱性的原因(2)查阅资料可知,常温下,部分弱电解质的电离平衡常数如表:
| 弱电解质 |  |  |  |
电离平衡常数 |  | 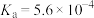 | 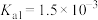 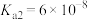 |
 的电离平衡常数的表达式
的电离平衡常数的表达式
②常温下,等浓度的下列溶液a.
 ;b.
;b. ;c.
;c. ,其
,其 由大到小的顺序是
由大到小的顺序是(3)某同学设计一个肼
 燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中
燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中 为阳离子交换膜。
为阳离子交换膜。
①通入肼的电极为
②若甲中有
 氧气(标准况下)参加反应,乙中通过离子交换膜的阳离子个数为
氧气(标准况下)参加反应,乙中通过离子交换膜的阳离子个数为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
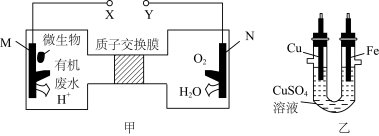
【推荐2】图甲是一种利用微生物将废水中的尿素[CO(NH2)2]的化学能直接转化为电能,并生成对环境友好物质的装置,同时利用此装置的电能在铁片上镀铜。
回答下列问题:
(1)铁电极应与___ 极(填“X”或“Y”)相连,H+应向___ 极(填“M”或者“N”)做定向移动。
(2)M极发生的电极反应式为___ ;若铜片上的质量减少1.92g,则甲装置中消耗CO(NH2)2的质量为___ g。
(3)常温下,若将铁电极换成石墨电极并与Y极相连,则当电路中通过0.01mol电子时,铜电极发生的电极反应式为___ ,此时溶液的pH=___ (此时溶液体积为100mL)。通电一段时间后,向所得的溶液中加入0.1molCuO后恰好恢复到电解前的浓度和pH,则电解过程中转移电子的物质的量为___ (忽略溶液体积变化)。

回答下列问题:
(1)铁电极应与
(2)M极发生的电极反应式为
(3)常温下,若将铁电极换成石墨电极并与Y极相连,则当电路中通过0.01mol电子时,铜电极发生的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】如图所示,某同学设计一个甲烷燃料电池并探究电解原理。已知C的电极材料为金属锌单质,其余皆为惰性电极,工作一段时间后,D电极表面有紫红色光亮物质析出。根据要求回答相关问题:
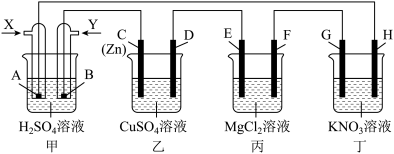
(1)通入甲烷的电极为______ (填“X”或“Y”)极,该电极的电极反应式为______ 。
(2)乙装置中锌电极的电极反应式为______ 。如果利用乙装置在铁件表面镀铜,则铁件应与______ (填“C”或“D”)极的电极材料互换,阳极换为铜单质,电镀一段时间后,电解液中Cu2+浓度将______ (填“增大”“减小”或“不变”)。
(3)电解一段时间后,检验丙装置中E极产物的操作及现象为______ ,该装置的电解总反应离子方程式为______ 。
(4)若甲装置在标准状况下有2.24L氧气参加反应,则丁装置两极产生的气体总体积为______ L;且丁装置溶液的pH______ (填“增大”“减小”或“不变”)。

(1)通入甲烷的电极为
(2)乙装置中锌电极的电极反应式为
(3)电解一段时间后,检验丙装置中E极产物的操作及现象为
(4)若甲装置在标准状况下有2.24L氧气参加反应,则丁装置两极产生的气体总体积为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐1】有机玻璃(聚甲基丙烯酸甲酯)具有透光率高、自重轻、安全性能高等优点,目前它广泛用于制作仪器仪表零件、照明灯罩、光学镜片、透明屋顶、电话亭、广告灯箱、标志牌等。如图是以2-甲基丙烯为原料合成有机玻璃E(聚-2-甲基丙烯酸甲酯)的路线:

(1)有机化合物 中含有的官能团名称是
中含有的官能团名称是______________ 。
(2)写出B的结构简式:________________ 。
(3)写出反应①的化学方程式______________ 。
(4)写出反应⑥的化学方程式_______________ 。
(5)在上述①~⑥反应中,属于取代反应的是_______ ,属于加成反应的是_______ 。
(6)写出E的结构简式:_______ 。
(7)写出有机物 通过缩聚反应形成的高分子聚酯F的结构简式:
通过缩聚反应形成的高分子聚酯F的结构简式:_________ 。

(1)有机化合物
 中含有的官能团名称是
中含有的官能团名称是(2)写出B的结构简式:
(3)写出反应①的化学方程式
(4)写出反应⑥的化学方程式
(5)在上述①~⑥反应中,属于取代反应的是
(6)写出E的结构简式:
(7)写出有机物
 通过缩聚反应形成的高分子聚酯F的结构简式:
通过缩聚反应形成的高分子聚酯F的结构简式:
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐2】本题为选做题,包括A、B两题。选学《化学与生活》模块的考生答A题,选学《有机化学基础》模块的考生答B题。每位考生只可选做1题,若两题都作答,则以A题计分。
A.《化学与生活》
(1)材料与人类吃、穿、住、行、用、医疗、通信等密切相关
①下列分子式或结构简式可表示维生素C的______ (填字母)。
a.C6H8O6 b.C6H10O6 c.
②玻璃钢门窗被国际上称为继木、钢、铝、塑之后的第五代门窗产品。玻璃钢属于下列材料中的____ (填字母)。
a.金属材料 b.无机非金属材料 c. 复合材料
③黏土是陶瓷的生产原料,其主要组成可表示为Al2Si2Ox(OH)4,则x=______ (填字母)。
a.1 b.3 c.5
(2)绿色发展可使 “天更蓝,水更清,空气更清新,生活更美好”。
①传统的一次性塑料袋有聚氯乙烯、氯乙烯等,它们在环境中难降解易造成白色污染,合成聚氯乙烯的单体为_____ (写结构简式)。
②燃煤产生的NO2是形成硝酸型酸雨的元凶,在催化剂及加热条件下用NH3与NO2反应可生成无毒无污染的气体,该反应的化学方程式为______ 。
③含铬(Cr2O72ˉ)的酸性废水处理方法之一可采用(NH4)2Fe(SO4)2将Cr2O72ˉ还原为Cr3+,再用氨水将Cr3+转变成难溶的Cr(OH)3。该方案运用了污水处理方法中的沉淀法和______ 。处理后的废水中因含有大量_____ (填离子符号),能导致水体富营养化,还需进一步处理。
(3)保持营养平衡,合理使用药物是保证身心健康、提高生活质量的有效手段。
①有些氨基酸人体自身不能合成,要从外界才能获得,这些氨基酸称为________ 。苹果中含有一定量的铁元素,人体缺铁会导致的疾病是_____ 。
②含碘食盐中添加有KIO3,可用KI、盐酸及淀粉溶液检验,该反应的离子方程式为_______ 。
③人类历史上最重要的抗生素是_____ (填名称);“铝镁加”是一种新型的抗酸剂,它的主要成分的化学式为:Al2Mg6(OH)14(CO3)2·4H2O,它与胃酸主要成分反应的化学方程式为______ 。
B.《有机化学基础》
(1)有机化合物的结构对其性质有着重要的影响。
①下列有机物易溶于水的是____ (填字母)。
a. 乙烷 b.乙醇 c.乙酸乙酯
②下列有机物常温下呈气态的是_____ (填字母)。
a.正丁烷 b.苯 c.溴乙烷
③分子式为C2H4O2的有机物中既能发生银镜反应又能发生水解反应的是_____ (填字母)。
a.CH3COOH b.HOCH2CHO c. HCOOCH3
(2)芴酮可用作工程塑料的改进剂。某芴酮可通过下列反应得到:

①化合物Ⅱ中含氧官能团为____ 和_____ (写名称)。
②鉴别化合物Ⅰ和化合物Ⅱ可用的试剂为_____ (写化学式)。
③1mol化合物Ⅰ最多可与_____ molNaOH完全反应。
(3)囧烷(E)的一种合成路线如下:

①A→B的反应类型为_____ ;B中手性碳原子数目为_____ (填数字)。
②E的分子式______ ;A可用于合成一种常见的人造橡胶的单体,由A制备该单体的化学方程式为______ 。
③满足下列条件的D的同分异体的结构简式为_____ 。
Ⅰ.含有1个苯环,无其它环状结构,能与FeCl3溶液发生显色反应。
Ⅱ.核磁共振氢谱有4组峰且面积比为3∶3∶2∶2。
A.《化学与生活》
(1)材料与人类吃、穿、住、行、用、医疗、通信等密切相关
①下列分子式或结构简式可表示维生素C的
a.C6H8O6 b.C6H10O6 c.

②玻璃钢门窗被国际上称为继木、钢、铝、塑之后的第五代门窗产品。玻璃钢属于下列材料中的
a.金属材料 b.无机非金属材料 c. 复合材料
③黏土是陶瓷的生产原料,其主要组成可表示为Al2Si2Ox(OH)4,则x=
a.1 b.3 c.5
(2)绿色发展可使 “天更蓝,水更清,空气更清新,生活更美好”。
①传统的一次性塑料袋有聚氯乙烯、氯乙烯等,它们在环境中难降解易造成白色污染,合成聚氯乙烯的单体为
②燃煤产生的NO2是形成硝酸型酸雨的元凶,在催化剂及加热条件下用NH3与NO2反应可生成无毒无污染的气体,该反应的化学方程式为
③含铬(Cr2O72ˉ)的酸性废水处理方法之一可采用(NH4)2Fe(SO4)2将Cr2O72ˉ还原为Cr3+,再用氨水将Cr3+转变成难溶的Cr(OH)3。该方案运用了污水处理方法中的沉淀法和
(3)保持营养平衡,合理使用药物是保证身心健康、提高生活质量的有效手段。
①有些氨基酸人体自身不能合成,要从外界才能获得,这些氨基酸称为
②含碘食盐中添加有KIO3,可用KI、盐酸及淀粉溶液检验,该反应的离子方程式为
③人类历史上最重要的抗生素是
B.《有机化学基础》
(1)有机化合物的结构对其性质有着重要的影响。
①下列有机物易溶于水的是
a. 乙烷 b.乙醇 c.乙酸乙酯
②下列有机物常温下呈气态的是
a.正丁烷 b.苯 c.溴乙烷
③分子式为C2H4O2的有机物中既能发生银镜反应又能发生水解反应的是
a.CH3COOH b.HOCH2CHO c. HCOOCH3
(2)芴酮可用作工程塑料的改进剂。某芴酮可通过下列反应得到:

①化合物Ⅱ中含氧官能团为
②鉴别化合物Ⅰ和化合物Ⅱ可用的试剂为
③1mol化合物Ⅰ最多可与
(3)囧烷(E)的一种合成路线如下:

①A→B的反应类型为
②E的分子式
③满足下列条件的D的同分异体的结构简式为
Ⅰ.含有1个苯环,无其它环状结构,能与FeCl3溶液发生显色反应。
Ⅱ.核磁共振氢谱有4组峰且面积比为3∶3∶2∶2。
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】Favorskii反应是化工生产中的重要反应,它是利用炔烃与羰基化合物在强碱性下发生反应,得到炔醇,反应原理为:

以下合成路线是某化工厂生产流程的一部分:
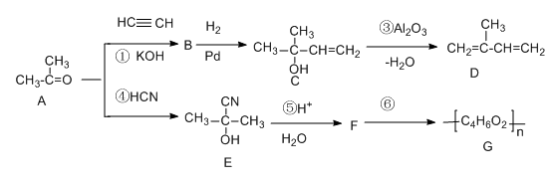
已知: ;
;
请回答下列问题:
(1)写出F中官能团的名称_____________________ 。
(2)写出D的名称(系统命名)____________________ 。
(3)④的反应类型是__________ ;B的结构简式是______________ 。
(4)已知H与D互为同分异构体,H属于炔烃,其核磁共振氢谱有3种吸收峰,则H的结构简式为:____________________________ 。

以下合成路线是某化工厂生产流程的一部分:

已知:
 ;
;请回答下列问题:
(1)写出F中官能团的名称
(2)写出D的名称(系统命名)
(3)④的反应类型是
(4)已知H与D互为同分异构体,H属于炔烃,其核磁共振氢谱有3种吸收峰,则H的结构简式为:
您最近一年使用:0次
【推荐1】废弃电脑的CPU中含有贵重金属Cu、Ag、Au,可回收利用,部分流程如下:

(1)铜元素在周期表中位于______ ,基态铜原子的核外电子排布式为______ 。
(2)电脑CPU在使用时会涂抹一层散热硅脂(一种液体橡胶,主要成分为聚二甲基硅氧烷和聚甲基硅氧烷),可用______洗去;
(3)用Zn粉还原 的化学反应方程式为
的化学反应方程式为______ ;
(4)试剂1为______ (填名称,下同),试剂2为______ ;
(5)加入过其铁粉的原因是______ ;
(6)滤渣2溶于试剂2的原因是______ ;(用离子反应方程式表示)
(7)金属铜的晶胞结构如图所示,铜原子之间的最小距离为apm,则铜晶胞的密度为______  (
( 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。

(1)铜元素在周期表中位于
(2)电脑CPU在使用时会涂抹一层散热硅脂(一种液体橡胶,主要成分为聚二甲基硅氧烷和聚甲基硅氧烷),可用______洗去;
| A.NaOH溶液 | B.纯碱溶液 | C.稀硫酸 | D.酒精 |
(3)用Zn粉还原
 的化学反应方程式为
的化学反应方程式为(4)试剂1为
(5)加入过其铁粉的原因是
(6)滤渣2溶于试剂2的原因是
(7)金属铜的晶胞结构如图所示,铜原子之间的最小距离为apm,则铜晶胞的密度为
 (
( 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】某研究小组制备 ,再利用高温合成法制备无水
,再利用高温合成法制备无水 ,流程如下:
,流程如下:
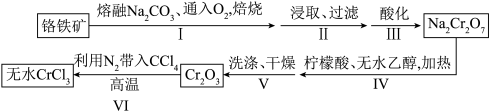
已知:(1)铬铁矿的主要成分为 。
。
(2) 高温条件下能被氧化。
高温条件下能被氧化。
请回答:
(1)下列有关说法不正确 的是_______。
(2)已知 的沸点为
的沸点为 ,为保证稳定的气流,适宜的加热方式为
,为保证稳定的气流,适宜的加热方式为_______ 。
(3)制备无水 时,在
时,在 的条件下进行的目的是
的条件下进行的目的是_______ 。
(4)为测定无水 中铬元素含量,可用已知浓度的硫酸亚铁铵标准溶液滴定
中铬元素含量,可用已知浓度的硫酸亚铁铵标准溶液滴定 。从下列选项中选择合理的仪器和操作,补全如下步骤[“_______”上填写
。从下列选项中选择合理的仪器和操作,补全如下步骤[“_______”上填写一件最关键仪器 ,“”内填写一种操作 ,均用字母表示]。_______(精确称取无水 样品
样品 )→放入锥形瓶中(_______)→往锥形瓶中(_______)(_______)→用_______(盛装硫酸亚铁铵标准溶液,滴定
)→放入锥形瓶中(_______)→往锥形瓶中(_______)(_______)→用_______(盛装硫酸亚铁铵标准溶液,滴定 )→滴定至中)
)→滴定至中) _______ 。
【仪器】a.托盘天平;b.酸式滴定管;c.分析天平;d.碱式滴定管;e.锥形瓶
【操作】f.加2滴 -苯代邻氨基苯甲酸溶液;g.加
-苯代邻氨基苯甲酸溶液;g.加 后加热至样品溶解; h.加入过硫酸铵溶液,加热使
后加热至样品溶解; h.加入过硫酸铵溶液,加热使 氧化成
氧化成 ,冷却; i.溶液颜色由櫻桃红色变为亮绿色至滴定终点
,冷却; i.溶液颜色由櫻桃红色变为亮绿色至滴定终点
(5)如果固态 中有痕量的
中有痕量的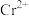 存在,则与水迅速反应生成
存在,则与水迅速反应生成 的水合物,将其溶液蒸发可析暗绿色的
的水合物,将其溶液蒸发可析暗绿色的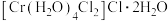 晶体,若将暗绿色溶液冷却到
晶体,若将暗绿色溶液冷却到 以下,并通入
以下,并通入 气体,则可析出紫色晶体。用乙醚处理紫色溶液并通入
气体,则可析出紫色晶体。用乙醚处理紫色溶液并通入 气体后,就析出了另一种淡绿色晶体,则上述紫色晶体和淡绿色晶体的化学式分别为
气体后,就析出了另一种淡绿色晶体,则上述紫色晶体和淡绿色晶体的化学式分别为_______ 、_______ 。(已知等量的暗绿色晶体、紫色晶体、淡绿色晶体消耗的硝酸银的物质的量之比为 )
)
 ,再利用高温合成法制备无水
,再利用高温合成法制备无水 ,流程如下:
,流程如下:
已知:(1)铬铁矿的主要成分为
 。
。(2)
 高温条件下能被氧化。
高温条件下能被氧化。请回答:
(1)下列有关说法
| A.步骤Ⅰ,将铬铁矿置于熔盐形成的液体中可增大接触面积,加快反应速率 |
B.步骤Ⅱ,浸取过滤后所得滤渣为 |
| C.步骤Ⅴ,用蒸馏水反复洗涤样品至滴下液体为无色时,可视为洗涤完成 |
D.步骤Ⅵ,不断增大 的流速,可大幅提高 的流速,可大幅提高 的产量 的产量 |
 的沸点为
的沸点为 ,为保证稳定的气流,适宜的加热方式为
,为保证稳定的气流,适宜的加热方式为(3)制备无水
 时,在
时,在 的条件下进行的目的是
的条件下进行的目的是(4)为测定无水
 中铬元素含量,可用已知浓度的硫酸亚铁铵标准溶液滴定
中铬元素含量,可用已知浓度的硫酸亚铁铵标准溶液滴定 。从下列选项中选择合理的仪器和操作,补全如下步骤[“_______”上填写
。从下列选项中选择合理的仪器和操作,补全如下步骤[“_______”上填写 样品
样品 )→放入锥形瓶中(_______)→往锥形瓶中(_______)(_______)→用_______(盛装硫酸亚铁铵标准溶液,滴定
)→放入锥形瓶中(_______)→往锥形瓶中(_______)(_______)→用_______(盛装硫酸亚铁铵标准溶液,滴定 )→滴定至中)
)→滴定至中) 【仪器】a.托盘天平;b.酸式滴定管;c.分析天平;d.碱式滴定管;e.锥形瓶
【操作】f.加2滴
 -苯代邻氨基苯甲酸溶液;g.加
-苯代邻氨基苯甲酸溶液;g.加 后加热至样品溶解; h.加入过硫酸铵溶液,加热使
后加热至样品溶解; h.加入过硫酸铵溶液,加热使 氧化成
氧化成 ,冷却; i.溶液颜色由櫻桃红色变为亮绿色至滴定终点
,冷却; i.溶液颜色由櫻桃红色变为亮绿色至滴定终点(5)如果固态
 中有痕量的
中有痕量的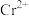 存在,则与水迅速反应生成
存在,则与水迅速反应生成 的水合物,将其溶液蒸发可析暗绿色的
的水合物,将其溶液蒸发可析暗绿色的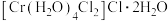 晶体,若将暗绿色溶液冷却到
晶体,若将暗绿色溶液冷却到 以下,并通入
以下,并通入 气体,则可析出紫色晶体。用乙醚处理紫色溶液并通入
气体,则可析出紫色晶体。用乙醚处理紫色溶液并通入 气体后,就析出了另一种淡绿色晶体,则上述紫色晶体和淡绿色晶体的化学式分别为
气体后,就析出了另一种淡绿色晶体,则上述紫色晶体和淡绿色晶体的化学式分别为 )
)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】以电解金属锰阳极渣(主要成分为 ,杂质为Pb、Fe、Ca、Mg元素的化合物)和黄铁矿
,杂质为Pb、Fe、Ca、Mg元素的化合物)和黄铁矿 (杂质为
(杂质为 )为原料制备
)为原料制备 的工艺流程如下:
的工艺流程如下:

已知: ,
,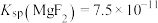 。
。
回答下列问题:
(1)为提高酸浸效果,可采取的措施有______ (写出两项)。
(2)“酸浸”过程中没有S单质生成,滤渣①的主要成分为(填化学式)______ ; 参与反应的离子方程式为
参与反应的离子方程式为________ 。
(3)向氧化过滤后的溶液中加入HF以除去溶液中钙元素和镁元素,除钙前滤液中( 浓度为
浓度为 mol⋅L
mol⋅L ,当溶液中
,当溶液中 mol⋅L
mol⋅L 时,除钙率为
时,除钙率为______ 。
(4)将“碱化”步骤所得含少量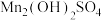 的
的 固体加去离子水打成浆,通空气氧化过程溶液pH随时间变化如图所示,pH先基本不变后迅速下降的原因为
固体加去离子水打成浆,通空气氧化过程溶液pH随时间变化如图所示,pH先基本不变后迅速下降的原因为____________ 。

(5)向滤液④中加入氧化钙,可得到在上述流程中循环利用的物质是____________ ;“一系列操作”包括____________ 。
 ,杂质为Pb、Fe、Ca、Mg元素的化合物)和黄铁矿
,杂质为Pb、Fe、Ca、Mg元素的化合物)和黄铁矿 (杂质为
(杂质为 )为原料制备
)为原料制备 的工艺流程如下:
的工艺流程如下:
已知:
 ,
,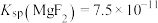 。
。回答下列问题:
(1)为提高酸浸效果,可采取的措施有
(2)“酸浸”过程中没有S单质生成,滤渣①的主要成分为(填化学式)
 参与反应的离子方程式为
参与反应的离子方程式为(3)向氧化过滤后的溶液中加入HF以除去溶液中钙元素和镁元素,除钙前滤液中(
 浓度为
浓度为 mol⋅L
mol⋅L ,当溶液中
,当溶液中 mol⋅L
mol⋅L 时,除钙率为
时,除钙率为(4)将“碱化”步骤所得含少量
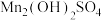 的
的 固体加去离子水打成浆,通空气氧化过程溶液pH随时间变化如图所示,pH先基本不变后迅速下降的原因为
固体加去离子水打成浆,通空气氧化过程溶液pH随时间变化如图所示,pH先基本不变后迅速下降的原因为
(5)向滤液④中加入氧化钙,可得到在上述流程中循环利用的物质是
您最近一年使用:0次



