NO是大气污染物之一,在一定条件下,采用活性炭可发生下列反应:2NO(g)+C(s)  N2(g)+CO2(g)。现在温度一定,容积为1 L的密闭容器中发生该反应,各物质的物质的量如下表所示:
N2(g)+CO2(g)。现在温度一定,容积为1 L的密闭容器中发生该反应,各物质的物质的量如下表所示:
下列判断正确的是
 N2(g)+CO2(g)。现在温度一定,容积为1 L的密闭容器中发生该反应,各物质的物质的量如下表所示:
N2(g)+CO2(g)。现在温度一定,容积为1 L的密闭容器中发生该反应,各物质的物质的量如下表所示:| 物质 | NO | 活性炭 | N2 | CO2 |
| 起始物质的量/mol | 0.100 | 1.030 | 0 | 0 |
| 2 min时的物质的量/mol | a | b | 0.030 | 0.030 |
| A.表格中的a∶b=2∶1 |
| B.2 min内,v(NO)=0.015 mol·L-1·min-1 |
C.若该温度下,反应的平衡常数为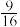 ,则2 min时反应已经达到平衡 ,则2 min时反应已经达到平衡 |
| D.增加活性炭可以提高NO的转化率 |
2018高二上·全国·专题练习 查看更多[3]
(已下线)2018年9月23日 《每日一题》人教选修4-每周一测(已下线)2019年9月22日 《每日一题》选修4—— 每周一测夯基提能2020届高三化学选择题对题专练——选修四化学反应原理——化学反应速率(提升练习)
更新时间:2018-09-20 21:04:51
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH,一般认为通过如下步骤来实现;①CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1 ②CO(g)+2H2(g)=CH3OH(g) ΔH2;体系能量变化如图所示。下列有关说法正确的是


| A.ΔH1<ΔH2 |
| B.步骤②反应ΔS>0 |
| C.二氧化碳加氢制甲醇的总反应速率取决于步骤① |
D.二氧化碳加氢制甲醇的总反应的平衡常数K=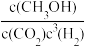 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在硫酸的工业生产中,通过下列反应使SO2转化为SO3:2SO2(g)+O2(g) 2SO3(g)。一定温度下,在甲、乙、丙、丁四个容积均为2L的恒容密闭容器中投入SO2(g)、O2(g)和SO3(g),其相关数据如表所示。下列判断中,正确的是
2SO3(g)。一定温度下,在甲、乙、丙、丁四个容积均为2L的恒容密闭容器中投入SO2(g)、O2(g)和SO3(g),其相关数据如表所示。下列判断中,正确的是
 2SO3(g)。一定温度下,在甲、乙、丙、丁四个容积均为2L的恒容密闭容器中投入SO2(g)、O2(g)和SO3(g),其相关数据如表所示。下列判断中,正确的是
2SO3(g)。一定温度下,在甲、乙、丙、丁四个容积均为2L的恒容密闭容器中投入SO2(g)、O2(g)和SO3(g),其相关数据如表所示。下列判断中,正确的是| 甲 | 乙 | 丙 | 丁 | ||
| 起始物质的量 | n(SO2)/mol | 0.4 | 0.8 | 0.8 | 0.4 |
| n(O2)/mol | 0.24 | 0.24 | 0.48 | 0.28 | |
| n(SO3)/mol | 0 | 0 | 0 | 0.4 | |
| SO2的平衡转化率/% | 80 | 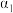 | 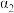 | 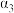 | |
| SO3的平衡含量/% | a | b | c | d | |
| A.平衡时,α1>α2 | B.平衡时,c(SO2,丙)=2c(SO2,甲) |
| C.平衡时,c<d | D.该温度下,平衡常数值为400L•mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】恒容条件下,1mol HI发生如下反应:2HI(g)⇌H2(g)+I2(g)。已知 ,
, 分别为正、逆反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下x(HI)随时间的变化。下列说法正确的是
分别为正、逆反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下x(HI)随时间的变化。下列说法正确的是

 ,
, 分别为正、逆反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下x(HI)随时间的变化。下列说法正确的是
分别为正、逆反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下x(HI)随时间的变化。下列说法正确的是
| A.该反应为放热反应 |
B.平衡状态时 |
C.a、b两点反应速率: |
D.当反应进行到a点时, |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知反应 ,不同温度下,容器中
,不同温度下,容器中 浓度与反应时间的关系如图所示,下列说法正确的是
浓度与反应时间的关系如图所示,下列说法正确的是

 ,不同温度下,容器中
,不同温度下,容器中 浓度与反应时间的关系如图所示,下列说法正确的是
浓度与反应时间的关系如图所示,下列说法正确的是
A. |
B. 点的正反应速率大于 点的正反应速率大于 点的逆反应速率 点的逆反应速率 |
C. 点的反应速率小于 点的反应速率小于 点的反应速率 点的反应速率 |
D. 点时 点时 的浓度为 的浓度为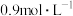 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
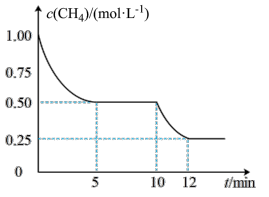
【推荐3】在密闭容器中进行反应 ,测得
,测得 随反应时间(t)的变化如图所示。下列判断正确的是( )
随反应时间(t)的变化如图所示。下列判断正确的是( )
 ,测得
,测得 随反应时间(t)的变化如图所示。下列判断正确的是( )
随反应时间(t)的变化如图所示。下列判断正确的是( )
A.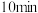 时,改变的外界条件可能是温度 时,改变的外界条件可能是温度 |
B.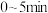 内, 内,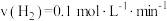 |
C.恒温下,缩小容器体积,达到新平衡时 比原平衡时的小 比原平衡时的小 |
D.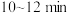 时反应的平衡常数逐渐增大 时反应的平衡常数逐渐增大 |
您最近一年使用:0次

 ,2min末达到平衡,生成0.8molW。下列说法错误的是
,2min末达到平衡,生成0.8molW。下列说法错误的是



