甲、乙、丙为常见单质,乙、丙两元素在周期表中位于同一主族。X、A、B、C、D、E、F、G均为常见的化合物,其中A和X的摩尔质量相同,A、G的焰色反应为黄色。在一定条件下,各物质相互转化关系如右图。请回答:

(1)X的电子式为____________________ ,写出E的化学式:____________ 。
(2)写出B与G溶液反应生成F的离子方程式:____________________________ 。
(3)写出A与H2O反应的化学反应方程式:______________________________ 。
(4)在上图的反应中,不属于氧化还原反应的是(填序号)___________________ 。

(1)X的电子式为
(2)写出B与G溶液反应生成F的离子方程式:
(3)写出A与H2O反应的化学反应方程式:
(4)在上图的反应中,不属于氧化还原反应的是(填序号)
更新时间:2018-09-21 09:43:38
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】I. “84消毒液”能有效杀灭甲型H1N1等病毒,某同学购买了一瓶“威露士”牌“84消毒液”,并查阅相关资料和消毒液包装说明得到如下信息:
“84消毒液”:含25%NaClO、1000mL、密度1.49g·cm-3,稀释100倍(体积比)后使用。长时间放置易与空气中的CO2反应而导致浓度偏低。
(1)该“84消毒液”的物质的量浓度约为___________ mol·L-1。
(2)某同学取100mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=___________ mol·L-1。
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%密度1.19g·cm-3的消毒液。下列说法正确的是___________ (填字母)。
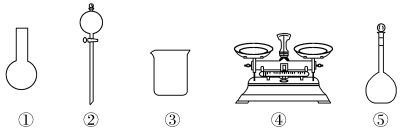
A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.利用购买的商品NaClO来配制可能导致结果偏低
(4)下列操作会导致溶液浓度偏低的是___________(填字母)。
Ⅱ.Na2FeO4是一种新型消毒剂,可由NaClO在碱性条件下与 Fe(OH)3反应制得。 2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O
(5)①用“双线桥”标明该反应中电子的转移及数目___________
②氧化剂与氧化产物的物质的量之比为___________ ;
③若反应转移 3mol 电子,则生成 Na2FeO4的物质的量是___________ 。
“84消毒液”:含25%NaClO、1000mL、密度1.49g·cm-3,稀释100倍(体积比)后使用。长时间放置易与空气中的CO2反应而导致浓度偏低。
(1)该“84消毒液”的物质的量浓度约为
(2)某同学取100mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%密度1.19g·cm-3的消毒液。下列说法正确的是

A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.利用购买的商品NaClO来配制可能导致结果偏低
(4)下列操作会导致溶液浓度偏低的是___________(填字母)。
| A.未用蒸馏水洗涤烧杯内壁或未将洗涤液注入容量瓶 |
| B.配制前,容量瓶中有少量蒸馏水 |
| C.定容时俯视容量瓶刻度线 |
| D.颠倒摇匀后发现凹液面低于刻度线又加水补上 |
Ⅱ.Na2FeO4是一种新型消毒剂,可由NaClO在碱性条件下与 Fe(OH)3反应制得。 2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O
(5)①用“双线桥”标明该反应中电子的转移及数目
②氧化剂与氧化产物的物质的量之比为
③若反应转移 3mol 电子,则生成 Na2FeO4的物质的量是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】有4种钠的化合物W、X、Y、Z,它们之间存在如下关系:
①W X+H2O+CO2↑
X+H2O+CO2↑
②Z+CO2→X+O2
③Z+H2O→Y+O2↑
④X+Ca(OH)2→Y+CaCO3↓
试回答下列问题:
(1)W、X、Y、Z的化学式分别是W:__ 、X:__ 、Y:__ 、Z__ 。
(2)以上4个化学反应,属于氧化还原反应的是__ (填反应序号),反应中还原剂是__ (写化学式)。反应②中每生成标况下3.36L气体,转移电子的数目为__ 。
①W
 X+H2O+CO2↑
X+H2O+CO2↑②Z+CO2→X+O2
③Z+H2O→Y+O2↑
④X+Ca(OH)2→Y+CaCO3↓
试回答下列问题:
(1)W、X、Y、Z的化学式分别是W:
(2)以上4个化学反应,属于氧化还原反应的是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】硫化氢的转化是资源利用和环境保护的重要研究课题。
(1)工业上利用克劳斯法将H2S转化为硫单质回收。为实现硫的最大回收,部分 H2S燃烧先生成SO2,SO2和剩余的H2S反应的物质的量之比为_______ 。
(2)硫化氢(H2S)是一种有毒、有害的不良气体。处理某废气中的 H2S,是将废气与空气混合通入FeCl2、CuCl2、FeCl3的混合液中,其转化的流程如图所示。
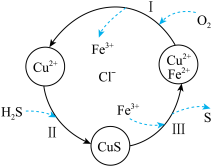
①参与循环的阳离子有Cu2+、_______ 。
②过程Ⅲ中发生的离子反应为:_______ 。
③H2S 是一种弱酸,试用化学原理解释过程Ⅱ能发生的原因是:_______ 。
④该循环过程总反应为:_______ 。
(3)将烧碱吸收H2S后的溶液加入到如图所示的电解池的阳极区进行电解。电解过程中阳极区发生如下反应:S2--2e-=S;(n-1)S+S2-=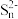
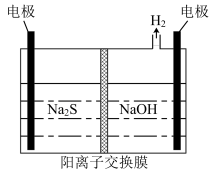
①写出电解时阴极的电极反应式:_______
②电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成_______ 。
(1)工业上利用克劳斯法将H2S转化为硫单质回收。为实现硫的最大回收,部分 H2S燃烧先生成SO2,SO2和剩余的H2S反应的物质的量之比为
(2)硫化氢(H2S)是一种有毒、有害的不良气体。处理某废气中的 H2S,是将废气与空气混合通入FeCl2、CuCl2、FeCl3的混合液中,其转化的流程如图所示。

①参与循环的阳离子有Cu2+、
②过程Ⅲ中发生的离子反应为:
③H2S 是一种弱酸,试用化学原理解释过程Ⅱ能发生的原因是:
④该循环过程总反应为:
(3)将烧碱吸收H2S后的溶液加入到如图所示的电解池的阳极区进行电解。电解过程中阳极区发生如下反应:S2--2e-=S;(n-1)S+S2-=
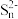

①写出电解时阴极的电极反应式:
②电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下图是无机物A~F在一定条件下的转化关系(部分产物及反应条件未标出)。其中A为气体;A~F都含有相同的元素。
试回答下列问题:
(1)写出下列物质的化学式:C_________ 、F_________
(2)写出下列反应的化学方程式:
①____________________________________ 。
③___________________________ ,该反应氧化剂与还原剂的物质的量之比为_________ 。
(3)铜与E的浓溶液反应的离子方程式为_________ 。
(4)25.6g铜与含有1.4 mol E的浓溶液恰好完全反应,最终得到气体的体积为(标准状况下)_________ L。
试回答下列问题:
(1)写出下列物质的化学式:C
(2)写出下列反应的化学方程式:
①
③
(3)铜与E的浓溶液反应的离子方程式为
(4)25.6g铜与含有1.4 mol E的浓溶液恰好完全反应,最终得到气体的体积为(标准状况下)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
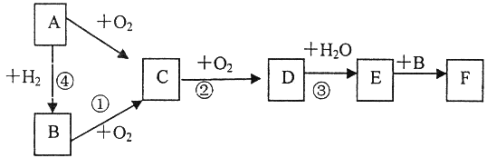
【推荐2】物质A~L有如图转化关系,其中A为用途广泛的金属,其合金是制造飞机和宇宙飞船的理想材料,D、E为气体单质。已知一般情况下,难溶性氢氧化物在加热条件下会分解为对应的氧化物和水。试回答下列问题。
(1)金属A为___________ ,(填写化学式,下同)气体B为___________ ,沉淀L为___________ 。
(2)写出G→H的离子方程式:___________ 。
(3)写出J→K的离子方程式:___________ 。
(4)检验溶液H中的金属阳离子的方法是___________ 。
(5)向200 mL 3 mol·L-1溶液K中加入60 g铁、铜混合物(铁和铜的物质的量之比为1∶1),充分反应后过滤,所得滤液中溶质的物质的量为___________ 。

(1)金属A为
(2)写出G→H的离子方程式:
(3)写出J→K的离子方程式:
(4)检验溶液H中的金属阳离子的方法是
(5)向200 mL 3 mol·L-1溶液K中加入60 g铁、铜混合物(铁和铜的物质的量之比为1∶1),充分反应后过滤,所得滤液中溶质的物质的量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
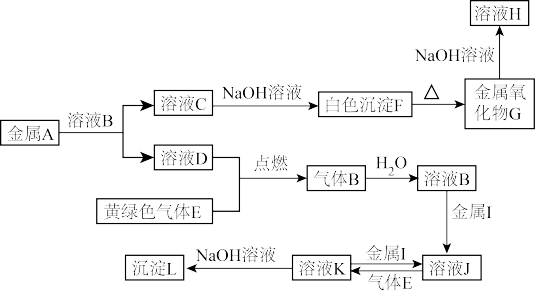
【推荐3】某种常见的白色晶体A,与盐酸反应产生无刺激性气味的气体B,将B通入澄清石灰水,石灰水变浑浊。若在A的水溶液中加氢氧化钡溶液微热,则析出白色沉淀C和无色气体D,D可以使湿润的红色石蕊试纸变蓝。加热固体A,可生成水、B和D,而且B和D的物质的量之比为1:1。
(1)根据以上事实,可以判断出A是________ ,B是________ ,C是________ 。
(2)加热固体A生成水、B和D的化学方程式是_________________________ ,A与盐酸反应的离子方程式是___________________________________ ,A与氢氧化钡溶液反应的离子方程式是___________________________________________ 。
(1)根据以上事实,可以判断出A是
(2)加热固体A生成水、B和D的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某小组同学利用以下实验装置研究 的性质(经检验,装置的气密性良好)。
的性质(经检验,装置的气密性良好)。
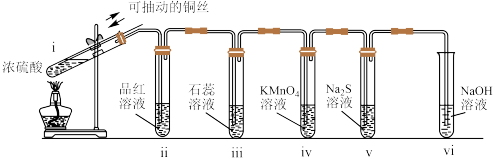
(1)装置i中发生反应的化学方程式__________ 。
(2)ⅱ中观察品红溶液褪色,结论是: 有
有__________ 性。
(3)ⅲ中石蕊溶液变红,说明 与
与 反应生成了酸性物质。写出该反应的化学方程式
反应生成了酸性物质。写出该反应的化学方程式__________ 。
(4)ⅳ中观察到的现象是__________ ,结论是: 有
有__________ 性。
(5)ⅴ中产生淡黄色浑浊,结论是: 有
有__________ 性。
(6) 溶液用于吸收多余的
溶液用于吸收多余的 ,反应的离子方程式
,反应的离子方程式__________ 。
 的性质(经检验,装置的气密性良好)。
的性质(经检验,装置的气密性良好)。
(1)装置i中发生反应的化学方程式
(2)ⅱ中观察品红溶液褪色,结论是:
 有
有(3)ⅲ中石蕊溶液变红,说明
 与
与 反应生成了酸性物质。写出该反应的化学方程式
反应生成了酸性物质。写出该反应的化学方程式(4)ⅳ中观察到的现象是
 有
有(5)ⅴ中产生淡黄色浑浊,结论是:
 有
有(6)
 溶液用于吸收多余的
溶液用于吸收多余的 ,反应的离子方程式
,反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】为探究 的性质,采用下列实验装置制少量
的性质,采用下列实验装置制少量 并进行相应的实验探究:
并进行相应的实验探究:
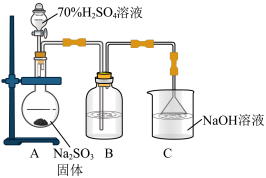
(1)装置A中盛放浓硫酸的仪器名称是___________ 。
(2)若B中的试剂是品红溶液,B中溶液红色褪去, 表现的性质
表现的性质___________ 。
(3)若B中的试剂是酸性 溶液,则B中的现象是
溶液,则B中的现象是___________ ,写出反应的离子方程式( 被还原为
被还原为 )
)___________ 。
(4)装置C中倒置漏斗的作用是___________ ,反应的离子方程式为___________ 。
(5)已知: 可还原某含碲物质(主要成分为
可还原某含碲物质(主要成分为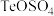 )溶液可得到粗碲。具体实验操作为:取该溶液于烧瓶中,加入适量
)溶液可得到粗碲。具体实验操作为:取该溶液于烧瓶中,加入适量 ,加热到一定温度,持续通入
,加热到一定温度,持续通入 ,待反应一定时间,过滤得到粗碲。在一定条件下,碲沉淀率与温度、还原时间的变化曲线分别如图1、图2所示:
,待反应一定时间,过滤得到粗碲。在一定条件下,碲沉淀率与温度、还原时间的变化曲线分别如图1、图2所示:
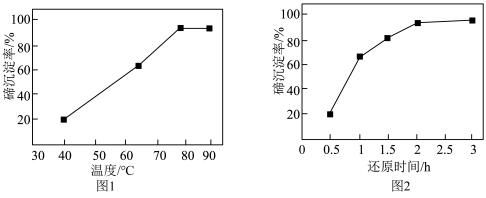
①由图可知,最适宜的温度和还原时间分别为___________ 。
②图1中80℃后,升高温度,碲沉淀率几乎不再升高,甚至有下降趋势。可能的原因是________ 。
 的性质,采用下列实验装置制少量
的性质,采用下列实验装置制少量 并进行相应的实验探究:
并进行相应的实验探究:
(1)装置A中盛放浓硫酸的仪器名称是
(2)若B中的试剂是品红溶液,B中溶液红色褪去,
 表现的性质
表现的性质(3)若B中的试剂是酸性
 溶液,则B中的现象是
溶液,则B中的现象是 被还原为
被还原为 )
)(4)装置C中倒置漏斗的作用是
(5)已知:
 可还原某含碲物质(主要成分为
可还原某含碲物质(主要成分为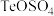 )溶液可得到粗碲。具体实验操作为:取该溶液于烧瓶中,加入适量
)溶液可得到粗碲。具体实验操作为:取该溶液于烧瓶中,加入适量 ,加热到一定温度,持续通入
,加热到一定温度,持续通入 ,待反应一定时间,过滤得到粗碲。在一定条件下,碲沉淀率与温度、还原时间的变化曲线分别如图1、图2所示:
,待反应一定时间,过滤得到粗碲。在一定条件下,碲沉淀率与温度、还原时间的变化曲线分别如图1、图2所示:
①由图可知,最适宜的温度和还原时间分别为
②图1中80℃后,升高温度,碲沉淀率几乎不再升高,甚至有下降趋势。可能的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某实验小组探究SO2与AgNO3溶液的反应。
I.制取SO2
(1)实验室中可用多种方法制取SO2,结合下列供选择的试剂和装置,选出一种可行的方法,该方法反应的化学方程式为___________ ,对应的发生装置是___________ (填标号)。
可供选择的试剂:Cu(s)、C(s)、Na2SO3(s)、98%的H2SO4、70%的H2SO4
可供选择的发生装置:
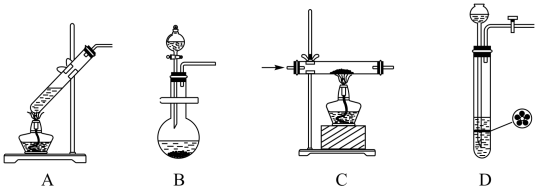
II.实验探究
将足量SO2通入下列装置,得到白色沉淀b和无色溶液c。
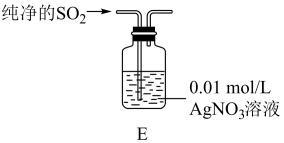
【查阅资料】Ag2SO3难溶于水,Ag2SO4微溶于水且能溶于物质的量浓度大于3mol·L-1的硝酸。
【分析讨论】
(2)实验探究装置中还存在一个重要缺陷,你的改进方法是___________ 。
(3)对体系中有关物质性质的分析:SO2具有还原性,可能被装置中的 、Ag+或
、Ag+或______ (填化学式)氧化生成 。
。
(4)对白色沉淀b的猜想:猜想一,沉淀b是Ag2SO4;猜想二,沉淀b是Ag2SO3;猜想三,沉淀b是Ag2SO3和Ag2SO4的混合物。
【实验验证】
取白色沉淀b,加入一定量的5mol·L-1的硝酸,沉淀全部溶解,并产生无色气体,气体遇空气变红棕色;取无色溶液c,加入盐酸酸化的0.1mol/LBaCl2溶液,无明显现象。
【实验结论】
①不能用Ba(NO3)2溶液代替BaCl2溶液的原因是___________ 。
②猜想___________ (填“一”“二”“三”)正确,沉淀溶解的化学方程式为___________ 。
I.制取SO2
(1)实验室中可用多种方法制取SO2,结合下列供选择的试剂和装置,选出一种可行的方法,该方法反应的化学方程式为
可供选择的试剂:Cu(s)、C(s)、Na2SO3(s)、98%的H2SO4、70%的H2SO4
可供选择的发生装置:

II.实验探究
将足量SO2通入下列装置,得到白色沉淀b和无色溶液c。

【查阅资料】Ag2SO3难溶于水,Ag2SO4微溶于水且能溶于物质的量浓度大于3mol·L-1的硝酸。
【分析讨论】
(2)实验探究装置中还存在一个重要缺陷,你的改进方法是
(3)对体系中有关物质性质的分析:SO2具有还原性,可能被装置中的
 、Ag+或
、Ag+或 。
。(4)对白色沉淀b的猜想:猜想一,沉淀b是Ag2SO4;猜想二,沉淀b是Ag2SO3;猜想三,沉淀b是Ag2SO3和Ag2SO4的混合物。
【实验验证】
取白色沉淀b,加入一定量的5mol·L-1的硝酸,沉淀全部溶解,并产生无色气体,气体遇空气变红棕色;取无色溶液c,加入盐酸酸化的0.1mol/LBaCl2溶液,无明显现象。
【实验结论】
①不能用Ba(NO3)2溶液代替BaCl2溶液的原因是
②猜想
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】三个密闭容器分别装有A.Na2O2和NaHCO3, B.Na2O2和NH4HCO3, C.Na2O2和Ca(HCO3)2,其中每种物质均为1mol。将它们加热至300℃,充分反应后排出气体。
(1)写出各容器中残余物质的化学式及物质的量。
A._____ ; B._____ ; C._____ 。
(2)如果分别加入相同浓度的足量盐酸与残留物完全反应,则消耗盐酸的体积由大到小的顺序是_____ 。
(3)如果分别将A、B、C中原物质加入水中完全反应后溶质分别是什么?现象如何?
A:_____ ; B:_____ ; C:_____ 。
(1)写出各容器中残余物质的化学式及物质的量。
A.
(2)如果分别加入相同浓度的足量盐酸与残留物完全反应,则消耗盐酸的体积由大到小的顺序是
(3)如果分别将A、B、C中原物质加入水中完全反应后溶质分别是什么?现象如何?
A:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】在下列各变化中,反应①为常温下的反应,A、C、D均含氯元素,且A中氯元素的化合价介于C与D之间,E常温下为无色无味的液体,F为淡黄色粉末,G为常见的无色气体。
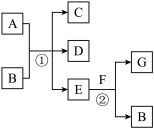
回答下列问题:
(1)A、G的化学式分别为___ 、__ 。
(2)F和E反应的化学方程式为___ 。
(3)写出反应①的化学方程式:__ 。

回答下列问题:
(1)A、G的化学式分别为
(2)F和E反应的化学方程式为
(3)写出反应①的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】为了验证 与
与 需要在水蒸气存在下才能反应,设计如下实验:
需要在水蒸气存在下才能反应,设计如下实验:
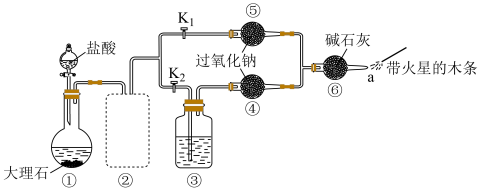
(1)①中反应可以制备 ,离子方程式为
,离子方程式为___________ 。
(2)制备的 气体中存在挥发的
气体中存在挥发的 气体,装置②可以将
气体,装置②可以将 杂质除去,请在虚线部分补充装置和试剂
杂质除去,请在虚线部分补充装置和试剂___________ 。
(3)③中试剂为浓硫酸,开始实验后分别打开 和
和 ,观察到
,观察到___________ (填现象)可以证实在没有水蒸气存在下 与
与 不反应。
不反应。
(4)有同学认为仅通过本实验,无法得到“ 在水蒸气存在下能够与
在水蒸气存在下能够与 反应”这个结论,理由是
反应”这个结论,理由是___________ ;请设计实验进一步证实该结论:___________ 。
(5)⑤中发生的化学方程式有___________ 。
(6)以下说法正确的是___________ 。
a. 中的阴离子是
中的阴离子是
b. 可以用作呼吸面具中的填充剂
可以用作呼吸面具中的填充剂
c.⑥中碱石灰的作用是排除空气中 和
和 对实验的干扰
对实验的干扰
 与
与 需要在水蒸气存在下才能反应,设计如下实验:
需要在水蒸气存在下才能反应,设计如下实验:
(1)①中反应可以制备
 ,离子方程式为
,离子方程式为(2)制备的
 气体中存在挥发的
气体中存在挥发的 气体,装置②可以将
气体,装置②可以将 杂质除去,请在虚线部分补充装置和试剂
杂质除去,请在虚线部分补充装置和试剂(3)③中试剂为浓硫酸,开始实验后分别打开
 和
和 ,观察到
,观察到 与
与 不反应。
不反应。(4)有同学认为仅通过本实验,无法得到“
 在水蒸气存在下能够与
在水蒸气存在下能够与 反应”这个结论,理由是
反应”这个结论,理由是(5)⑤中发生的化学方程式有
(6)以下说法正确的是
a.
 中的阴离子是
中的阴离子是
b.
 可以用作呼吸面具中的填充剂
可以用作呼吸面具中的填充剂c.⑥中碱石灰的作用是排除空气中
 和
和 对实验的干扰
对实验的干扰
您最近一年使用:0次



