粗食盐中除含有钙离子、镁离子、硫酸根离子等可溶性杂质外,还含有泥砂等不溶性杂质。我们食用的精盐是用粗食盐提纯而得到的。通过教材中“粗盐的提纯”及你做过的该实验回答下列问题。
(1)实验室进行NaCl溶液蒸发时,一般有以下操作过程 ①放置酒精灯;②固定铁圈位置;③放上蒸发皿(蒸发皿中盛有NaCl溶液);④加热搅拌;⑤停止加热。其正确的操作顺序为_________________ 。
(2)如何运用最简方法检验溶液中有无SO42-离子?__________________ 。如果有,应该如何除去SO42-离子?_________________________ 。
(3)在粗盐经过溶解→过滤后的溶液中滴加饱和Na2CO3溶液,直至不再产生沉淀为止。请问这步操作的目的是__________________________________________________ 。
(4)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的;溶解时:________ 。过滤时:_________ 。蒸发时:__________ 。
(1)实验室进行NaCl溶液蒸发时,一般有以下操作过程 ①放置酒精灯;②固定铁圈位置;③放上蒸发皿(蒸发皿中盛有NaCl溶液);④加热搅拌;⑤停止加热。其正确的操作顺序为
(2)如何运用最简方法检验溶液中有无SO42-离子?
(3)在粗盐经过溶解→过滤后的溶液中滴加饱和Na2CO3溶液,直至不再产生沉淀为止。请问这步操作的目的是
(4)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的;溶解时:
更新时间:2018-09-29 17:01:30
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】磷酸锌常用作氯化橡胶合成高分子材料的阻燃剂。工业上利用烧渣灰(主要含ZnO,还含少量FeO、Al2O3、CuO及SiO2)为原料制取磷酸锌的工艺流程如图所示:
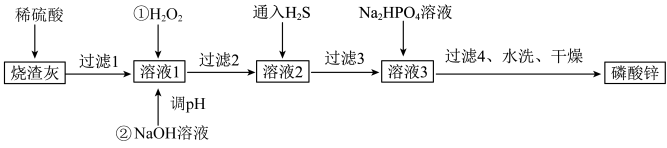
已知:①[Zn3(PO4)2]在水中几乎不溶,其在水中的溶解度随温度的升高而降低;
②“溶液1”中几种金属离子开始沉淀与沉淀完全的pH如表所示:
(1)烧渣灰加入稀硫酸时,请写出ZnO与稀硫酸反应的离子方程式___________
(2)加入H2O2的作用___________
(3)经过滤2得到滤渣的主要成分是Fe(OH)3和Al(OH)3,则用NaOH溶液调节pH的范围是___________ 。
(4)加入Na2HPO4溶液发生反应的离子方程式为___________ 。
(5)洗涤磷酸锌沉淀时应选用___________ (填“冷水”或“热水”),确认磷酸锌洗涤干净的操作是___________ 。
(6)通入H2S是为了除铜离子,25°C时,当通入H2S达到饱和时测得溶液的pH=1,c(H2S)=0.1 mol·L-1,此时溶液中c(Cu2+)=6.3×10-15mol·L-1,则CuS的溶度积Ksp=___________ (已知:25°C时,H2S的电离平衡常数Ka1=1×10-7 mol∙L-1,Ka2=1×10-15 mol∙L-1)。

已知:①[Zn3(PO4)2]在水中几乎不溶,其在水中的溶解度随温度的升高而降低;
②“溶液1”中几种金属离子开始沉淀与沉淀完全的pH如表所示:
| 金属离子 | Al3+ | Fe3+ | Cu2+ | Zn2+ |
| 开始沉淀的pH | 3.0 | 2.2 | 5.4 | 6.5 |
| 完全沉淀的pH | 5.0 | 3.6 | 6.7 | 8.5 |
(1)烧渣灰加入稀硫酸时,请写出ZnO与稀硫酸反应的离子方程式
(2)加入H2O2的作用
(3)经过滤2得到滤渣的主要成分是Fe(OH)3和Al(OH)3,则用NaOH溶液调节pH的范围是
(4)加入Na2HPO4溶液发生反应的离子方程式为
(5)洗涤磷酸锌沉淀时应选用
(6)通入H2S是为了除铜离子,25°C时,当通入H2S达到饱和时测得溶液的pH=1,c(H2S)=0.1 mol·L-1,此时溶液中c(Cu2+)=6.3×10-15mol·L-1,则CuS的溶度积Ksp=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】钛( 是一种化学性质稳定的过渡元素,在航空航天、海洋工程和生物医疗等领域具有极为重要的实用价值。工业上以钛铁矿(
是一种化学性质稳定的过渡元素,在航空航天、海洋工程和生物医疗等领域具有极为重要的实用价值。工业上以钛铁矿( ,含
,含 、
、 、
、 等杂质)为主要原料制取
等杂质)为主要原料制取 的流程如下:
的流程如下: 的形式存在于溶液中;
的形式存在于溶液中;
② 煅烧生产
煅烧生产 。
。
回答下列问题:
(1)滤渣1的主要成分为_______________ (填化学式);绿矾中铁的化合价是__________________ 。
(2)“操作X”工序需控制温度不能过高,从产品角度分析原因为_______________________ 。
(3)“水解”析出 ,该反应的离子方程式是
,该反应的离子方程式是______________________________ 。
(4)“洗涤”工序,检验 已洗涤干净的方法为
已洗涤干净的方法为_______________________ 。
(5)写出“高温氯化”工序中反应的化学方程式:____________________________________ 。
(6)镍钛记忆合金可用于飞机和宇宙飞船。已知一种镍钛合金的晶胞结构如图所示,若合金的密度为 ,
, 代表阿伏加德罗常数的值,则晶胞中两个钛原子间的最近距离是
代表阿伏加德罗常数的值,则晶胞中两个钛原子间的最近距离是______________  (用含
(用含 和
和 的计算式表示,不必化简)。
的计算式表示,不必化简)。
 是一种化学性质稳定的过渡元素,在航空航天、海洋工程和生物医疗等领域具有极为重要的实用价值。工业上以钛铁矿(
是一种化学性质稳定的过渡元素,在航空航天、海洋工程和生物医疗等领域具有极为重要的实用价值。工业上以钛铁矿( ,含
,含 、
、 、
、 等杂质)为主要原料制取
等杂质)为主要原料制取 的流程如下:
的流程如下:
 的形式存在于溶液中;
的形式存在于溶液中;②
 煅烧生产
煅烧生产 。
。回答下列问题:
(1)滤渣1的主要成分为
(2)“操作X”工序需控制温度不能过高,从产品角度分析原因为
(3)“水解”析出
 ,该反应的离子方程式是
,该反应的离子方程式是(4)“洗涤”工序,检验
 已洗涤干净的方法为
已洗涤干净的方法为(5)写出“高温氯化”工序中反应的化学方程式:
(6)镍钛记忆合金可用于飞机和宇宙飞船。已知一种镍钛合金的晶胞结构如图所示,若合金的密度为
 ,
, 代表阿伏加德罗常数的值,则晶胞中两个钛原子间的最近距离是
代表阿伏加德罗常数的值,则晶胞中两个钛原子间的最近距离是 (用含
(用含 和
和 的计算式表示,不必化简)。
的计算式表示,不必化简)。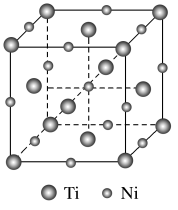
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】某固体可能由KNO3、K2SO4、KCl、NaCl、CuCl2和Na2CO3中的一种或几种组成。依次进行下列五步实验,观察到的实验现象记录如下:①将固体加水得到无色溶液;②向上述溶液中滴加过量BaCl2溶液,有白色沉淀生成。将该沉淀滤出,得到的沉淀可完全溶于稀HNO3;③向②的滤液中加入AgNO3溶液,有白色沉淀生成,该沉淀不溶于稀HNO3。
(1)据此,可判断出固体中肯定有_________ ,肯定没有_________ ,可能含有_________ 。
(2)写出②中反应的离子方程式_____________________ 、___________________ 。
(1)据此,可判断出固体中肯定有
(2)写出②中反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】从钒铬锰矿渣(主要成分为 、
、 、
、 )中提铬的一种工艺流程如下:
)中提铬的一种工艺流程如下: ](在空气中易被氧化.回答下列问题:
](在空气中易被氧化.回答下列问题:
(1)Cr元素位于元素周期表第_______ 周期_______ 族。
(2)用 溶液制备
溶液制备 胶体的化学方程式为
胶体的化学方程式为_______ 。
(3)常温下,各种形态五价钒粒子总浓度的对数[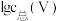 ]与pH关系如图1。已知钒铬锰矿渣硫酸浸液中
]与pH关系如图1。已知钒铬锰矿渣硫酸浸液中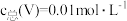 ,“沉钒”过程控制
,“沉钒”过程控制 ,则与胶体共沉降的五价钒粒子的存在形态为
,则与胶体共沉降的五价钒粒子的存在形态为_______ (填化学式)。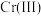 、
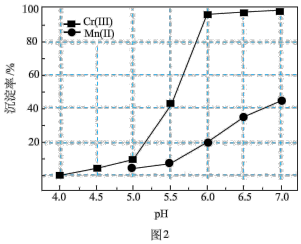
、 的沉淀率与pH关系如图2。“沉铬”过程最佳pH为
的沉淀率与pH关系如图2。“沉铬”过程最佳pH为_______ ;在该条件下滤液B中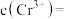
_______  【
【 近似为
近似为 ,
, 的
的 近似为
近似为 】。
】。 的离子方程式为
的离子方程式为_______ 。
(6)“提纯”过程中 的作用为
的作用为_______ 。
 、
、 、
、 )中提铬的一种工艺流程如下:
)中提铬的一种工艺流程如下: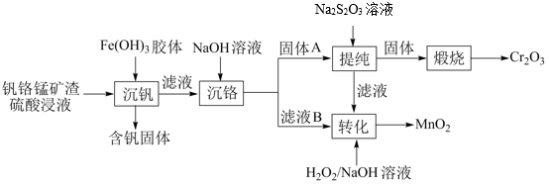
 ](在空气中易被氧化.回答下列问题:
](在空气中易被氧化.回答下列问题:(1)Cr元素位于元素周期表第
(2)用
 溶液制备
溶液制备 胶体的化学方程式为
胶体的化学方程式为(3)常温下,各种形态五价钒粒子总浓度的对数[
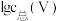 ]与pH关系如图1。已知钒铬锰矿渣硫酸浸液中
]与pH关系如图1。已知钒铬锰矿渣硫酸浸液中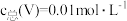 ,“沉钒”过程控制
,“沉钒”过程控制 ,则与胶体共沉降的五价钒粒子的存在形态为
,则与胶体共沉降的五价钒粒子的存在形态为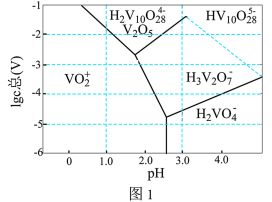
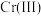 、
、 的沉淀率与pH关系如图2。“沉铬”过程最佳pH为
的沉淀率与pH关系如图2。“沉铬”过程最佳pH为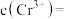
 【
【 近似为
近似为 ,
, 的
的 近似为
近似为 】。
】。
 的离子方程式为
的离子方程式为(6)“提纯”过程中
 的作用为
的作用为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】从砷盐净化渣(成分为Cu、As、Zn、ZnO、Co和SiO2)中回收有利用价值的金属,解决了长期以来影响砷盐净化工艺推广的技术难题,具有较强的实践指导意义。其工艺流程如图:
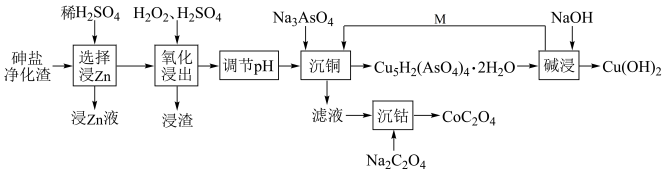
回答下列问题:
(1)在“选择浸Zn”时为提高效率可以采取的措施是_______ (任写一条)。其他条件不变时,Zn和Co的浸出率随pH变化如图所示,则“选择浸Zn”过程中,最好控制溶液的pH=_______ 。

(2)“氧化浸出”时,As转化为H3AsO4,则该反应中氧化剂和还原剂的物质的量之比为_______ 。“浸渣”的主要成分为_______ (填化学式)。
(3)用NaOH溶液调节氧化浸出液至弱酸性,再加入Na3AsO4进行“沉铜”,得到难溶性的Cu5H2(AsO4)4·2H2O,则“沉铜”的离子方程式为_______ 。
(4)“碱浸”时,除回收得到Cu(OH)2外,还得到物质M,且M在该工艺流程中可循环利用,M的化学式为_______ 。
(5)“沉钴”中的离子方程式为_______ 。所得草酸钴晶体洗涤后可得到纯净的晶体,证明晶体已经洗涤干净的操作是_______ 。
(6)在空气中煅烧草酸钴会生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为1.344L(标准状况),则该钴氧化物的化学式为_______ 。

回答下列问题:
(1)在“选择浸Zn”时为提高效率可以采取的措施是

(2)“氧化浸出”时,As转化为H3AsO4,则该反应中氧化剂和还原剂的物质的量之比为
(3)用NaOH溶液调节氧化浸出液至弱酸性,再加入Na3AsO4进行“沉铜”,得到难溶性的Cu5H2(AsO4)4·2H2O,则“沉铜”的离子方程式为
(4)“碱浸”时,除回收得到Cu(OH)2外,还得到物质M,且M在该工艺流程中可循环利用,M的化学式为
(5)“沉钴”中的离子方程式为
(6)在空气中煅烧草酸钴会生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为1.344L(标准状况),则该钴氧化物的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】一种高效无机水处理剂——聚合氯化铝晶体的化学式为[Al2(OH)nCl6-n·xH2O]m。它可通过调节AlCl3溶液的pH,促进其水解而结晶析出。其制备原料主要是铝加工行业的废渣——铝灰,它主要含Al2O3、Al,还有SiO2等杂质。聚合氯化铝生产的工艺流程如下:

(1)搅拌加热操作过程中发生反应的离子方程式为_______________________________________ 。
(2)生产过程中实验操作B、D的名称均为________ 。
(3)反应中副产品a是________ ,试剂b是________ 。(用化学式表示)
(4)生产过程中可循环使用的物质是________ (用化学式表示)。
(5)调节pH=4.0~4.5的目的是______________________________________________ 。
(6)为得到较纯净的晶体,生产过程中C物质可选用________ 。
A.氨水 B.NaAlO2 C.NaOH D.Al2O3 E.Al

(1)搅拌加热操作过程中发生反应的离子方程式为
(2)生产过程中实验操作B、D的名称均为
(3)反应中副产品a是
(4)生产过程中可循环使用的物质是
(5)调节pH=4.0~4.5的目的是
(6)为得到较纯净的晶体,生产过程中C物质可选用
A.氨水 B.NaAlO2 C.NaOH D.Al2O3 E.Al
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】铁、铜及其化合物在工业生产中有重要的用途。运用相关知识,回答下列问题:
(1)电子工业常用30%的FeCl3溶液腐蚀覆在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式_______ 。
(2)甲同学为了从使用过的腐蚀废液中回收铜,并获得氯化铁晶体,准备采用下列步骤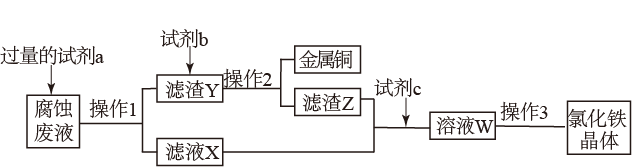
回答下列问题:
①试剂a是_______ (用化学式表示);操作Ⅰ用到的玻璃仪器有_______ 。
②滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为_______ 。
③上述流程中操作Ⅲ包括蒸发浓缩、_______ 、过滤、洗涤。
(3)乙同学为了探究Fe2(SO4)3与Cu的反应,做了如图所示实验:
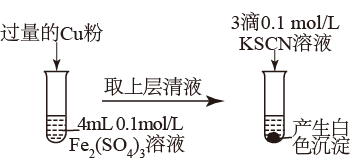
为了探究白色沉淀产生的原因,同学们查阅资料得知:
i.CuSCN是难溶于水的白色固体;
ii.SCN-的化学性质与I-的相似;
iii.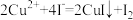 。
。
填写实验方案:
Cu2+与SCN-反应的离子方程式为_______ 。
(1)电子工业常用30%的FeCl3溶液腐蚀覆在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式
(2)甲同学为了从使用过的腐蚀废液中回收铜,并获得氯化铁晶体,准备采用下列步骤

回答下列问题:
①试剂a是
②滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为
③上述流程中操作Ⅲ包括蒸发浓缩、
(3)乙同学为了探究Fe2(SO4)3与Cu的反应,做了如图所示实验:

为了探究白色沉淀产生的原因,同学们查阅资料得知:
i.CuSCN是难溶于水的白色固体;
ii.SCN-的化学性质与I-的相似;
iii.
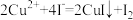 。
。填写实验方案:
| 实验方案 | 实验现象 |
| 步骤Ⅰ:取4mL0.2mol/LFeSO4溶液于试管中,向其中滴加3滴0.1mol/LKSCN溶液 | 无明显现象 |
| 步骤2:取4mL | 产生白色沉淀 |
Cu2+与SCN-反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】从含氯化钠、硝酸钾混合固体中提取氯化钠的过程如下图所示:

(1)试样预处理操作为____ ,此操作需要在____ 中进行,玻璃棒的作用是______ 。
(2)通过___ 法得到NaCl晶体。操作2必须趁热进行,原因是____ ,在“得到NaCl晶体实验操作中”,下列仪器无需用到的是____ 。
A.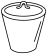 B.
B. C.
C.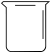 D.
D.

(1)试样预处理操作为
(2)通过
A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】硫酸亚铁铵晶体 俗称莫尔盐,是分析化学中的重要试剂,其化学性质与
俗称莫尔盐,是分析化学中的重要试剂,其化学性质与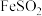 相近,但在空气中比一般的亚铁盐稳定。某同学在实验室中以铁粉与硫酸铵为原料按如下流程制备莫尔盐并测其产率(产率=
相近,但在空气中比一般的亚铁盐稳定。某同学在实验室中以铁粉与硫酸铵为原料按如下流程制备莫尔盐并测其产率(产率= )。
)。
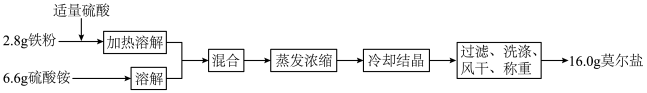
请回答下列问题:
(1)向莫尔盐溶液中加入氨水,久置后产生红褐色沉淀,该红褐色沉淀为___________ (填化学式)。莫尔盐溶液也能使酸性 溶液褪色,反应的离子方程式为
溶液褪色,反应的离子方程式为___________ 。
(2)用适量硫酸溶解铁粉时,还原产物是___________ (填化学式)。
(3)蒸发浓缩时,溶液应装在___________ 中(填仪器名称)。蒸发时不能蒸干溶液,而要在有晶体析出时立刻停止加热,原因是___________
(4)某同学通过上述流程制得莫尔盐16.0g,则实验产率为___________ (保留1位小数)。
 俗称莫尔盐,是分析化学中的重要试剂,其化学性质与
俗称莫尔盐,是分析化学中的重要试剂,其化学性质与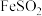 相近,但在空气中比一般的亚铁盐稳定。某同学在实验室中以铁粉与硫酸铵为原料按如下流程制备莫尔盐并测其产率(产率=
相近,但在空气中比一般的亚铁盐稳定。某同学在实验室中以铁粉与硫酸铵为原料按如下流程制备莫尔盐并测其产率(产率= )。
)。
请回答下列问题:
(1)向莫尔盐溶液中加入氨水,久置后产生红褐色沉淀,该红褐色沉淀为
 溶液褪色,反应的离子方程式为
溶液褪色,反应的离子方程式为(2)用适量硫酸溶解铁粉时,还原产物是
(3)蒸发浓缩时,溶液应装在
(4)某同学通过上述流程制得莫尔盐16.0g,则实验产率为
您最近一年使用:0次



