亚硝酸氯(C1NO)是有机合成中的重要试剂。可由NO与Cl2在通常条件下反应得到,化学方程式为2NO(g)+C12(g) 2C1NO(g),
2C1NO(g),
(1)已知几种化学键的键能数据如下表(亚硝酸氯的结构为Cl-N=O):
则2NO(g)+C12(g) 2C1NO(g)反应的△H和a的关系为△H=
2C1NO(g)反应的△H和a的关系为△H=____ kJ/mol。
(2)在1L的恒容密闭容器中充入2molNO(g)和1molC12(g),在不同温度下测得c(C1NO)与时间的关系如图A:
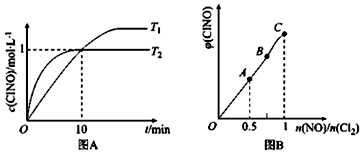
① 由图A可判断T1____ T2,该反应的△H____ 0 (填“>”“<”或“=”)。
② 反应开始到10min时NO的平均反应速率v(NO)=______ mol/(L·min)。
(3)一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(C12)的变化图象如图B,则A、B、C三状态中,NO的转化率最大的是________ 点。
 2C1NO(g),
2C1NO(g),(1)已知几种化学键的键能数据如下表(亚硝酸氯的结构为Cl-N=O):
| 化学键 | N≡O | Cl-Cl | Cl-N | N=O |
| 键能(kJ/mol) | 630 | 243 | a | 607 |
 2C1NO(g)反应的△H和a的关系为△H=
2C1NO(g)反应的△H和a的关系为△H=(2)在1L的恒容密闭容器中充入2molNO(g)和1molC12(g),在不同温度下测得c(C1NO)与时间的关系如图A:

① 由图A可判断T1
② 反应开始到10min时NO的平均反应速率v(NO)=
(3)一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(C12)的变化图象如图B,则A、B、C三状态中,NO的转化率最大的是
更新时间:2018-10-27 15:05:18
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】化学反应过程中释放或吸收的热量在生活、生产、科技及科学研究中具有广泛应用。
(1)“神舟”系列火箭用偏二甲肼( )作燃料,
)作燃料, 作氧化剂,反应后产物无污染。
作氧化剂,反应后产物无污染。
反应1: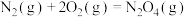

反应2: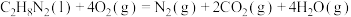
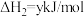
写出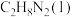 和
和 反应生成
反应生成 、
、 、
、 的热化学方程式:
的热化学方程式:__________________ 。
(2)已知,在25℃和101KPa下,部分化学键的键能数据如表所示。
①25℃和101KPa下,工业合成氨的反应中每生成1 mol  就会放出46 kJ热量,在该条件下,向某容器中加入2 mol
就会放出46 kJ热量,在该条件下,向某容器中加入2 mol  、6 mol
、6 mol  及合适的催化剂,充分反应后测得其放出的热量小于92 kJ,原因可能是
及合适的催化剂,充分反应后测得其放出的热量小于92 kJ,原因可能是________________ ,表中的a=______ 。
②科学家发现了一种新的气态分子 (图),在25℃和101 KPa下,
(图),在25℃和101 KPa下, 转化为
转化为 的热化学方程式为
的热化学方程式为______________________ ,由此可知 与
与 中更稳定的是
中更稳定的是______ (填化学式)。

③已知:
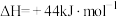 。甲烷是一种常用燃料,则表示甲烷的燃烧热的热化学方程式为
。甲烷是一种常用燃料,则表示甲烷的燃烧热的热化学方程式为_________________________ 。
(1)“神舟”系列火箭用偏二甲肼(
 )作燃料,
)作燃料, 作氧化剂,反应后产物无污染。
作氧化剂,反应后产物无污染。反应1:
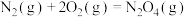

反应2:
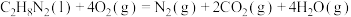
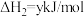
写出
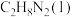 和
和 反应生成
反应生成 、
、 、
、 的热化学方程式:
的热化学方程式:(2)已知,在25℃和101KPa下,部分化学键的键能数据如表所示。
| 化学键 | H-H | H-N |  | O=O | C-H | C=O | H-O | N-N |
键能( ) ) | 436 | 391 | a | 498 | 414 | 803 | 462 | 193 |
 就会放出46 kJ热量,在该条件下,向某容器中加入2 mol
就会放出46 kJ热量,在该条件下,向某容器中加入2 mol  、6 mol
、6 mol  及合适的催化剂,充分反应后测得其放出的热量小于92 kJ,原因可能是
及合适的催化剂,充分反应后测得其放出的热量小于92 kJ,原因可能是②科学家发现了一种新的气态分子
 (图),在25℃和101 KPa下,
(图),在25℃和101 KPa下, 转化为
转化为 的热化学方程式为
的热化学方程式为 与
与 中更稳定的是
中更稳定的是
③已知:

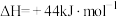 。甲烷是一种常用燃料,则表示甲烷的燃烧热的热化学方程式为
。甲烷是一种常用燃料,则表示甲烷的燃烧热的热化学方程式为
您最近一年使用:0次
【推荐2】氮元素的单质及其化合物在工农业生产、生活中有着重要作用。
(1)已知:N2(g)+3H2(g)=2NH3(g) =-92.4kJ·mol-1;相关键能数据如下表:
=-92.4kJ·mol-1;相关键能数据如下表:
则a=__________ 。
(2)如图表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。则图中M点所表示的平衡体系中,N2的转化率为_____________ 。

(1)已知:N2(g)+3H2(g)=2NH3(g)
 =-92.4kJ·mol-1;相关键能数据如下表:
=-92.4kJ·mol-1;相关键能数据如下表:N N N | H—H | N—H | |
| 键能/kJ·mol-1 | 945 | 436 | a |
则a=
(2)如图表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。则图中M点所表示的平衡体系中,N2的转化率为

您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】按要求填空
(I)写出下列反应的热化学方程式。
(1)N2(气态)与H2(气态)起反应,完全反应生成34g NH3(气态)放出92.2 kJ的热量:________________________________________ 。
(2)标况下22.4L N2(气态)与适量O2(气态)起反应,生成NO(气态)需吸收68 kJ的热量:______________________________________ 。
(3)卫星发射时可用肼(N2H4)为燃料,1 mol N2H4(气态)在O2(气态)中燃烧,生成N2(气态)和H2O(气态),放出534 kJ的热量:__________________________________________ 。
(4)已知断裂1 mol H—H键、1 mol N≡N键分别需要吸收436 kJ、946 kJ的能量,生成1 mol N—H键放出391 kJ的能量,试写出N2(g)与H2(g)反应生成NH3(g)的热化学方程式:___________________________________ 。
(II)已知: C(s)+ O2(g) === CO2(g) ΔH=-393.5 kJ/mol
2CO(g)+O2(g) === 2CO2(g) ΔH=-566 kJ/mol
TiO2(s)+2Cl2(g) === TiCl4(s)+O2(g) ΔH=+141 kJ/mol
则TiO2(s)+2Cl2(g)+2C(s) === TiCl4(s)+2CO(g) ΔH=__________________ 。
(I)写出下列反应的热化学方程式。
(1)N2(气态)与H2(气态)起反应,完全反应生成34g NH3(气态)放出92.2 kJ的热量:
(2)标况下22.4L N2(气态)与适量O2(气态)起反应,生成NO(气态)需吸收68 kJ的热量:
(3)卫星发射时可用肼(N2H4)为燃料,1 mol N2H4(气态)在O2(气态)中燃烧,生成N2(气态)和H2O(气态),放出534 kJ的热量:
(4)已知断裂1 mol H—H键、1 mol N≡N键分别需要吸收436 kJ、946 kJ的能量,生成1 mol N—H键放出391 kJ的能量,试写出N2(g)与H2(g)反应生成NH3(g)的热化学方程式:
(II)已知: C(s)+ O2(g) === CO2(g) ΔH=-393.5 kJ/mol
2CO(g)+O2(g) === 2CO2(g) ΔH=-566 kJ/mol
TiO2(s)+2Cl2(g) === TiCl4(s)+O2(g) ΔH=+141 kJ/mol
则TiO2(s)+2Cl2(g)+2C(s) === TiCl4(s)+2CO(g) ΔH=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】乙炔广泛用于焊接、焊割及有机合成等方面。
(1)已知下列热化学方程式:
4CH4 (g)+3O2(g)==2C2H2(g)+6H2O(g) △H1=a kJ•mol-1;
2H2(g)+O2(g)==2H2O(g) △H2=b kJ•mol-1;
2CH4(g)==C2H2(g)+3H2 (g) △H3
①△H3=____________________ (用含a、b的代数式表示)kJ•mol-1。
②已知下列共价键的键能数据:
则△H3=____________________ (填数值)kJ•mol-1。
(2)氯仿(CHCl3)与金属银共热可以制取乙炔,该反应的化学方程式为__________________________ 。
(3)向压强为1.0×104 kPa的恒压密闭容器中充入1 mol乙炔和1 mol HCl气体,在催化剂作用下乙炔与HCl发生反应:HC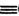 CH(g)+HCl(g)
CH(g)+HCl(g) CH2==CHCl(g),乙炔的平衡转化率与温度的关系如图所示。
CH2==CHCl(g),乙炔的平衡转化率与温度的关系如图所示。
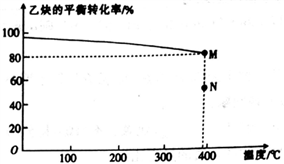
①该反应的△H__________ (填“>”或“<”)0,N点时乙炔的反应速率v(正)________ (填“>”或“<” 或“=”) v(逆)。
② M点对应温度下,该反应的平衡常数Kp=_________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)(kPa)-1,
(1)已知下列热化学方程式:
4CH4 (g)+3O2(g)==2C2H2(g)+6H2O(g) △H1=a kJ•mol-1;
2H2(g)+O2(g)==2H2O(g) △H2=b kJ•mol-1;
2CH4(g)==C2H2(g)+3H2 (g) △H3
①△H3=
②已知下列共价键的键能数据:
| 共价键 | C—H | H—H | C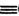 C C |
| 键能/ kJ•mol-1 | 413.4 | 436 | 812 |
(2)氯仿(CHCl3)与金属银共热可以制取乙炔,该反应的化学方程式为
(3)向压强为1.0×104 kPa的恒压密闭容器中充入1 mol乙炔和1 mol HCl气体,在催化剂作用下乙炔与HCl发生反应:HC
 CH(g)+HCl(g)
CH(g)+HCl(g) CH2==CHCl(g),乙炔的平衡转化率与温度的关系如图所示。
CH2==CHCl(g),乙炔的平衡转化率与温度的关系如图所示。
①该反应的△H
② M点对应温度下,该反应的平衡常数Kp=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】T0C时,在一个体积为2L的容器中,A气体和B气体反应反应生成C气体,反应过程中A、B、C浓度变化如图所示.

(1) 写出该反应的方程式:_______________
(2) 计算该温度下该反应的平衡常数:_______________
(3) 已知:K(300℃)>K(350℃),该反应是____________ 热反应.
(4) 0~4分钟时,B的平均反应速率为:_______________
(5) 到达平衡时A的转化率为:_______________
(6) 恒容条件下,下列措施中能使n(A)/n(C)降低的有____________ .
A.充入氦气 B.使用催化剂
C.再充入2.4molA和1.6molB D.降低温度.

(1) 写出该反应的方程式:
(2) 计算该温度下该反应的平衡常数:
(3) 已知:K(300℃)>K(350℃),该反应是
(4) 0~4分钟时,B的平均反应速率为:
(5) 到达平衡时A的转化率为:
(6) 恒容条件下,下列措施中能使n(A)/n(C)降低的有
A.充入氦气 B.使用催化剂
C.再充入2.4molA和1.6molB D.降低温度.
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】一定温度下,向体积为2L的密闭容器中加入1mol N2和 3.2 molH2进行如下反应:N2(g)+3H2(g) 2NH3(g)△H<0,反应2min后,测得N2的物质的量为0.2 mol。
2NH3(g)△H<0,反应2min后,测得N2的物质的量为0.2 mol。
(1)写出该反应的平衡常数表达式 K =___ ,温度升高时,该反应的平衡常数___ (填“增大”“减小”或“不变”),2min内,H2的物质的量减少了___ mol,NH3的物质的量增加了___ mol,该温度下,计算此反应的平衡常数为___ 。
(2)在2分钟内,用N2的浓度变化表示的平均反应速率为___ 。
(3)达平衡后将容器的体积缩小为原来的一半,则H2的浓度将___ (填“增大”“减小”或“不变”)。
 2NH3(g)△H<0,反应2min后,测得N2的物质的量为0.2 mol。
2NH3(g)△H<0,反应2min后,测得N2的物质的量为0.2 mol。(1)写出该反应的平衡常数表达式 K =
(2)在2分钟内,用N2的浓度变化表示的平均反应速率为
(3)达平衡后将容器的体积缩小为原来的一半,则H2的浓度将
您最近一年使用:0次
【推荐1】某地质学家经勘测发现一种新的磁黄铁矿,主要成分为Fe1-xS1+x,杂质不含Fe、S。分析可知该磁黄铁矿中,铁元素中三价铁的质量分数为75%。取5吨 73%的该磁黄铁矿,用接触法制硫酸,若沸腾炉中煅烧的损耗率为4%,接触室中反应的转化率为94%,SO3的吸收效率为97%,则最多可制得98.3%的浓硫酸的质量是______________ 。(保留2位小数)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】含氮化合物在化学工业中有着重要的应用,回答下列问题:
(1)一定条件下,硝酸铵加热分解得到的产物只有N2O和H2O。250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的平衡常数表达式为K=___________ ;若有1mol硝酸铵完全分解,则转移电子的数目为___________ (设NA为阿伏加 德罗常数的值)。
(2)硝基苯甲酸乙酯在碱性条件下发生反应:O2NC6H4COOC2H5+OH- O2NC6H4COO-+C2H5OH。两种反应物的初始浓度均为0.80mol·L-1,T℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。
O2NC6H4COO-+C2H5OH。两种反应物的初始浓度均为0.80mol·L-1,T℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。
①该反应在60~90s与90~120s内的平均反应速率分别约为___________ ,___________ ;比较两者大小可得出的结论是______________________ 。
②计算T℃时该反应的平衡常数为______________________ 。
③为提高O2NC6H4COOC2H5的平衡转化率,除可适当控制反应温度外,还可以采取的措施为______________________ (写出一条即可)。
(1)一定条件下,硝酸铵加热分解得到的产物只有N2O和H2O。250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的平衡常数表达式为K=
(2)硝基苯甲酸乙酯在碱性条件下发生反应:O2NC6H4COOC2H5+OH-
 O2NC6H4COO-+C2H5OH。两种反应物的初始浓度均为0.80mol·L-1,T℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。
O2NC6H4COO-+C2H5OH。两种反应物的初始浓度均为0.80mol·L-1,T℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。| t/s | 0 | 60 | 90 | 120 | 160 | 260 | 300 | 360 | 400 |
| a/% | 0 | 33.0 | 41.8 | 48.8 | 58.0 | 69.0 | 70.4 | 71.0 | 71.0 |
①该反应在60~90s与90~120s内的平均反应速率分别约为
②计算T℃时该反应的平衡常数为
③为提高O2NC6H4COOC2H5的平衡转化率,除可适当控制反应温度外,还可以采取的措施为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】含氮化合物在化学工业中有着重要的应用,回答下列问题:
(1)由N2O和NO反应生成N2和NO2的能量变化(表示生成1molN2的能量变化)如图所示,该反应的热化学方程式为______________________ 。
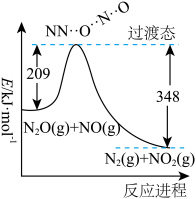
(2)一定条件下,硝酸铵加热分解得到的产物只有N2O和H2O。250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的平衡常数表达式为K=___________ ;若有1mol硝酸铵完全分解,则转移电子的数目为___________ (设NA为阿伏伽德罗常数的值)。
(3)硝基苯甲酸乙酯在碱性条件下发生反应:O2NC6H4COOC2H5+OH- O2NC6H4COO-+C2H5OH。两种反应物的初始浓度均为0.80mol·L-1,T℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。
O2NC6H4COO-+C2H5OH。两种反应物的初始浓度均为0.80mol·L-1,T℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。
①该反应在60~90s与90~120s内的平均反应速率分别约为___________ ,___________ ;比较两者大小可得出的结论是______________________ 。
②计算T℃时该反应的平衡常数为______________________ 。
③为提高O2NC6H4COOC2H5的平衡转化率,除可适当控制反应温度外,还可以采取的措施为______________________ (写出一条即可)。
(1)由N2O和NO反应生成N2和NO2的能量变化(表示生成1molN2的能量变化)如图所示,该反应的热化学方程式为

(2)一定条件下,硝酸铵加热分解得到的产物只有N2O和H2O。250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的平衡常数表达式为K=
(3)硝基苯甲酸乙酯在碱性条件下发生反应:O2NC6H4COOC2H5+OH-
 O2NC6H4COO-+C2H5OH。两种反应物的初始浓度均为0.80mol·L-1,T℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。
O2NC6H4COO-+C2H5OH。两种反应物的初始浓度均为0.80mol·L-1,T℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。| t/s | 0 | 60 | 90 | 120 | 160 | 260 | 300 | 360 | 400 |
| a/% | 0 | 33.0 | 41.8 | 48.8 | 58.0 | 69.0 | 70.4 | 71.0 | 71.0 |
②计算T℃时该反应的平衡常数为
③为提高O2NC6H4COOC2H5的平衡转化率,除可适当控制反应温度外,还可以采取的措施为
您最近一年使用:0次



