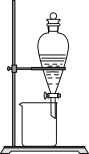
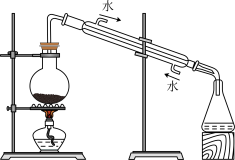
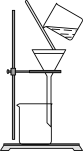
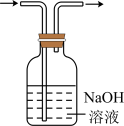
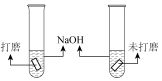
下列实验操作或结论正确的是
| A.分液漏斗不能将水与乙醇分离,但可以分离苯和四氯化碳 |
| B.在蒸馏过程中,发现蒸馏烧瓶中未加沸石或碎瓷片,可以立即补加 |
| C.在过滤和配制一定物质的量浓度的溶液中的玻璃棒作用完全相同 |
| D.测定同温同浓度NaCl和CH3COONa的pH可比较HCl和CH3COOH的酸性强弱 |
更新时间:2018-01-25 15:06:22
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】醋酸溶液中存在电离平衡:CH3COOH CH3COO-+H+,下列叙述中不正确的是
CH3COO-+H+,下列叙述中不正确的是
 CH3COO-+H+,下列叙述中不正确的是
CH3COO-+H+,下列叙述中不正确的是| A.pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH=7 |
| B.醋酸溶液中离子浓度的关系满足:c(H+)=c(CH3COO-)+c(OH-) |
| C.CH3COOH溶液中加入少量CH3COONa(s),醋酸电离平衡逆向移动 |
| D.0.1mol/L的CH3COOH溶液加水稀释,溶液中并非所有离子浓度都减小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】常温下,将pH=3的盐酸与pH=11的某碱溶液等体积混和后,所得溶液的pH值
| A.<7 | B.=7 | C.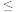 7 7 | D.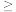 7 7 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】对危险化学品要在包装标签上印上警示性标志。下列的化学药品名称与警示标志名称对应不正确的是:
| A.酒精——易燃品 | B.浓硫酸——腐蚀品 |
| C.烧碱——剧毒品 | D.氯酸钾——强氧化剂 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列实验操作正确,并且与选项中实验目的匹配的是
| A | B | C | D |
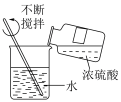 | 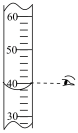 | 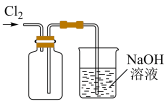 | 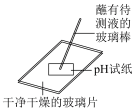 |
| 稀释浓硫酸 | 读取液体体积 | 收集氯气 | 测定饱和氯水的 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】工业上制备过碳酸钠(2Na2CO3·3H2O2)的一种流程如图:
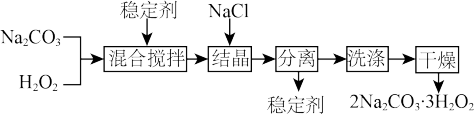
下列说法正确的是( )

下列说法正确的是( )
| A.可以用MnO2作稳定剂 |
| B.“分离”所用的主要玻璃仪器为烧杯、分液漏斗、玻璃棒 |
| C.2Na2CO3·3H2O2受热分解不属于氧化还原反应 |
| D.干燥过碳酸钠时可采用低温干燥法 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】用分液漏斗可以分离的一组液体混合物的是
| A.碘和苯 | B.乙醇和水 | C.苯和CCl4 | D.汽油和水 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列分离和提纯的实验操作中,正确的是
| A | B | C | D |
 | 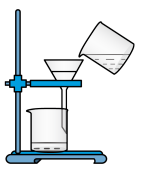 | 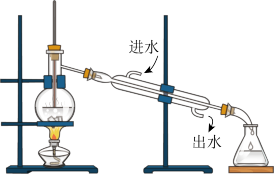 | 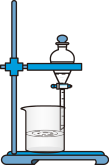 |
| 蒸发 | 过滤 | 蒸馏 | 分液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列实验操作、方法和装置均正确的是


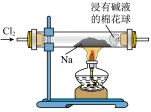
A.图①为制取少量 并可以控制反应停止 并可以控制反应停止 |
| B.图②为碳酸氢钠受热分解 |
| C.图③为比较二氧化锰、氯气和硫的氧化性 |
| D.图④为配制100mL2mol/L稀硫酸溶液 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】用如图所示实验装置进行相关实验探究,其中装置不合理的是
| A | B | C | D | |
| 目的 | 证明铝有致密氧化膜 | 鉴别纯碱与小苏打 | 证明 与烧碱溶液反应 与烧碱溶液反应 | 探究钠与 反应 反应 |
| 装置 |
|
|
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】下列实验操作、现象和结论都正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向25mL沸水中滴加5~6滴FeCl3饱和溶液,继续煮沸,生成红褐色沉淀 | 得到 胶体 胶体 |
| B | 称取4.0g固体NaOH于烧杯中,加入少量蒸馏水,配制溶解,转移至250mL容量瓶中定容 | 配制0.4000mol/L的NaOH溶液 |
| C | 盐酸和氢氧化钠溶液混合无现象 | 两者没有发生离子反应 |
| D | 向3mLKI溶液中滴加几滴双氧水,振荡,再滴加1mL淀粉溶液,溶液显蓝色 | 氧化性: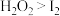 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 L-1的乙酸可以使石蕊溶液变红
L-1的乙酸可以使石蕊溶液变红