科学家最近研究出一种环保,安全的储氢方法,其原理可表示为NaHCO3+H2 HCOONa+H2O,下列有关说法不正确的是( )
HCOONa+H2O,下列有关说法不正确的是( )
 HCOONa+H2O,下列有关说法不正确的是( )
HCOONa+H2O,下列有关说法不正确的是( )| A.储氢、释氢过程均有能量变化 |
| B.储氢过程中,NaHCO3被还原 |
| C.NaHCO3、HCOONa均含有离子键和共价键 |
| D.释氢过程中,每消耗0.1 mol H2O放出2.24 L的H2 |
更新时间:2018-04-19 22:00:21
|
相似题推荐
单选题
|
适中
(0.64)
【推荐1】根据热化学方程式,正确的是
(1)CH4(g)+2O2(g)=CO2(g)+2H2O(g); △H1=-Q1 kJ·mol-1
(2)CH4(g)+2O2(g)=CO2(g)+2H2O(l); △H2=-Q2 kJ·mol-1
(1)CH4(g)+2O2(g)=CO2(g)+2H2O(g); △H1=-Q1 kJ·mol-1
(2)CH4(g)+2O2(g)=CO2(g)+2H2O(l); △H2=-Q2 kJ·mol-1
| A.Q1>Q2 | B.△H1>△H2 | C.Q1=Q2 | D.△H1<△H2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在催化剂作用下,以CO2和H2为原料进行合成CH3OH的实验。保持压强一定,将起始n(CO2)∶n(H2)=1∶3的混合气体通过装有催化剂的反应管,测得出口处CO2的转化率和CH3OH的选择性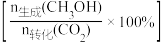 与温度的关系如下图所示。
与温度的关系如下图所示。
反应1∶CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H1=-49.5 kJ·mol-1
反应2∶CO2(g)+H2(g)=CO(g)+H2O(g) △H2=41.2 kJ·mol-1
下列说法正确的是
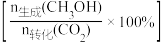 与温度的关系如下图所示。
与温度的关系如下图所示。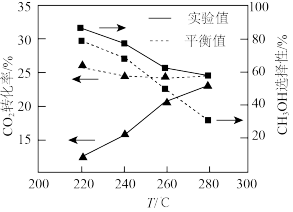
反应1∶CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H1=-49.5 kJ·mol-1
反应2∶CO2(g)+H2(g)=CO(g)+H2O(g) △H2=41.2 kJ·mol-1
下列说法正确的是
| A.CO(g)+2H2(g)=CH3OH(g)的△H=90.7kJ·mol-1 |
| B.280℃时,出口处CH3OH的体积分数的实验值小于平衡值 |
| C.220℃~240℃时CO2的平衡转化率随温度升高而降低,原因是反应2转化的CO2随温度的升高而减少 |
| D.220℃~280℃时,反应1的速率高于反应2的速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】最近有科学家发现正丁烷( )脱氢或不完全氧化也可制得1,3-丁二烯(
)脱氢或不完全氧化也可制得1,3-丁二烯(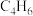 ),已知热化学方程式如下:( )
),已知热化学方程式如下:( )
① =
=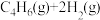
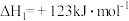
②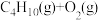 =
=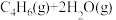
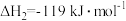
③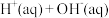 =
=
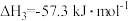
下列说法正确的是( )
 )脱氢或不完全氧化也可制得1,3-丁二烯(
)脱氢或不完全氧化也可制得1,3-丁二烯(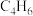 ),已知热化学方程式如下:( )
),已知热化学方程式如下:( )①
 =
=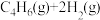
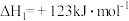
②
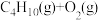 =
=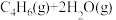
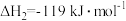
③
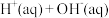 =
=
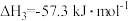
下列说法正确的是( )
A.由②可知,正丁烷( )的燃烧热为 )的燃烧热为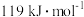 |
B.由①和②可推知: = =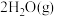 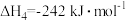 |
C. = = 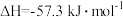 |
D.由①和②可知,同质量的正丁烷( )转变为1,3-丁二烯( )转变为1,3-丁二烯(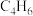 )所需要的能量相同 )所需要的能量相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】2A(g) B(g) ΔH= Q kJ·mol-1(Q>0);下列能量变化示意图正确的是
B(g) ΔH= Q kJ·mol-1(Q>0);下列能量变化示意图正确的是
 B(g) ΔH= Q kJ·mol-1(Q>0);下列能量变化示意图正确的是
B(g) ΔH= Q kJ·mol-1(Q>0);下列能量变化示意图正确的是A.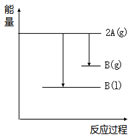 | B.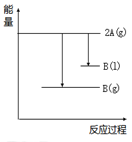 |
C. | D.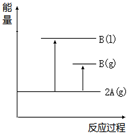 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】在一定的温度和压强下,将按一定比例混合的CO2和H2通过装有催化剂的反应器可得到甲烷.
已知: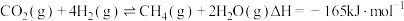
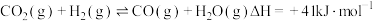
催化剂的选择是CO2甲烷化技术的核心.在两种不同催化剂作用下反应相同时间,测得CO2转化率和生成CH4选择性随温度变化的影响如图所示.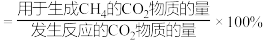
下列有关说法错误的是
已知:
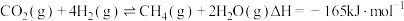
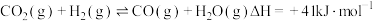
催化剂的选择是CO2甲烷化技术的核心.在两种不同催化剂作用下反应相同时间,测得CO2转化率和生成CH4选择性随温度变化的影响如图所示.
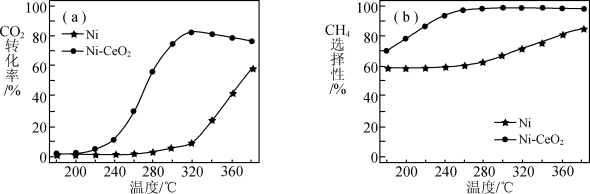
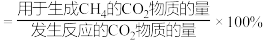
下列有关说法错误的是
A.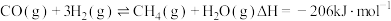 |
| B.延长W点的反应时间,能提高CO2的转化率 |
| C.在260~320℃间,以Ni-CeO2为催化剂,升高温度CH4的产率不变 |
| D.选择合适的催化剂、合适的温度有利于提高CH4的选择性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】如图1、图2分别表示 和
和 分解时的能量变化情况(单位:kJ)。下列说法错误的是
分解时的能量变化情况(单位:kJ)。下列说法错误的是
 和
和 分解时的能量变化情况(单位:kJ)。下列说法错误的是
分解时的能量变化情况(单位:kJ)。下列说法错误的是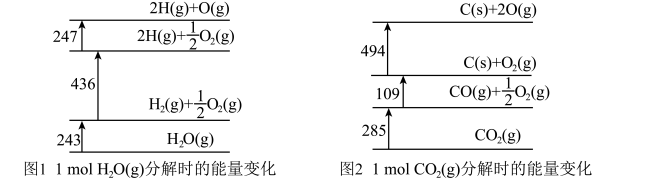
A.CO的燃烧热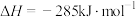 |
B. 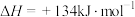 |
C.O=O的键能为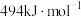 |
D.无法求得 的反应热 的反应热 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知:
①CO(g)+1/2O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
②H2(g)+1/2O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
下列说法正确的是( )
①CO(g)+1/2O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
②H2(g)+1/2O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
下列说法正确的是( )
| A.通常状况下,氢气的燃烧热为241.8 kJ·mol-1 |
| B.由①可知,1 mol CO(g)和1/2 mol O2(g)反应生成 1 mol CO2(g),放出283.0 kJ的热量 |
C.可用右图表示2CO2(g)===2CO(g)+O2(g)反应过程中的能量变化关系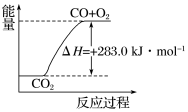 |
| D.分解1 mol H2O(g),其反应热为-241.8 kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
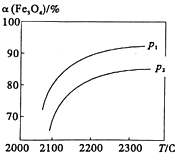
【推荐2】科学家研究以太阳能为热源分解Fe3O4,最终循环分解水制H2,其中一步重要反应为:2Fe3O4(s) 6FeO(s)+O2(g) △H=a kJ/mol。在一定压强下, Fe3O4的平衡转化率随温度变化的a(Fe3O4)―T曲线如图所示。下列有关说法不正确的是
6FeO(s)+O2(g) △H=a kJ/mol。在一定压强下, Fe3O4的平衡转化率随温度变化的a(Fe3O4)―T曲线如图所示。下列有关说法不正确的是
 6FeO(s)+O2(g) △H=a kJ/mol。在一定压强下, Fe3O4的平衡转化率随温度变化的a(Fe3O4)―T曲线如图所示。下列有关说法不正确的是
6FeO(s)+O2(g) △H=a kJ/mol。在一定压强下, Fe3O4的平衡转化率随温度变化的a(Fe3O4)―T曲线如图所示。下列有关说法不正确的是
| A.a>0 |
| B.压强p1>p2 |
| C.升高温度,该反应的平衡常数增大 |
| D.将体系中O2分离出去,能提高Fe3O4的转化率 |
您最近一年使用:0次

 结构及晶胞如图所示,白磷和红磷转化的热化学方程式为
结构及晶胞如图所示,白磷和红磷转化的热化学方程式为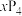 (白磷,s)
(白磷,s)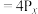 (红磷,s)
(红磷,s) 。下列说法正确的是
。下列说法正确的是
 属于共价晶体
属于共价晶体
 中充分燃烧生成等量
中充分燃烧生成等量 ,白磷放出的热量更多
,白磷放出的热量更多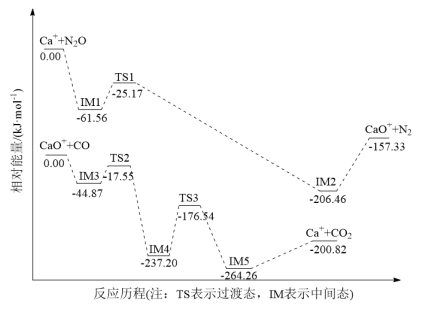
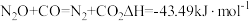
 CO+H2
CO+H2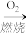 CO2+H2O
CO2+H2O 为原料合成甲醇是工业上的成熟方法,直接以
为原料合成甲醇是工业上的成熟方法,直接以 为原料生产甲醇是目前的研究热点。我国科学家用
为原料生产甲醇是目前的研究热点。我国科学家用
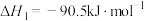

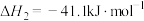

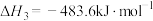
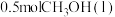 时,放出的热量小于45.25kJ
时,放出的热量小于45.25kJ
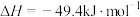
 为原料合成甲醇,同时生成
为原料合成甲醇,同时生成 ,该反应放出能量
,该反应放出能量

