T1 ℃时,向容积为2 L的密闭容器中充入一定量的CO和H2O(g),发生反应:CO(g)+H2O(g)  CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t2>t1),下列说法错误的是( )
CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t2>t1),下列说法错误的是( )
 CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t2>t1),下列说法错误的是( )
CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t2>t1),下列说法错误的是( )| 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 2.00 | 3.00 |
| t1 | 0.80 | |
| t2 | 1.80 |
| A.用H2表示反应在t1 min内的平均速率为v(H2)=0.60/t1mol·L-1·min-1 |
| B.保持其他条件不变,若起始时向容器中充入3.00 mol CO和2.00 mol H2O(g),达到平衡时,n(CO2)=1.20 mol |
| C.保持其他条件不变,在t2 min时向容器中再通入1.00 mol CO,与原平衡相比,达到新平衡时CO转化率将增大 |
| D.温度升至T2 ℃,上述反应的平衡常数为0.70,则正反应的ΔH<0 |
更新时间:2018-12-05 12:30:57
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】一定温度下,向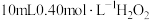 溶液中加入适量
溶液中加入适量 溶液,不同时刻测得生成
溶液,不同时刻测得生成 的体积(已折算为标准状况)如下表所示.资料显示,反应分两步进行:①
的体积(已折算为标准状况)如下表所示.资料显示,反应分两步进行:① ,②
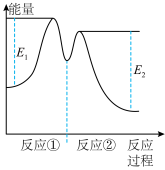
,② ,反应过程中能量变化如图所示.下列说法不正确的是
,反应过程中能量变化如图所示.下列说法不正确的是
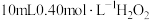 溶液中加入适量
溶液中加入适量 溶液,不同时刻测得生成
溶液,不同时刻测得生成 的体积(已折算为标准状况)如下表所示.资料显示,反应分两步进行:①
的体积(已折算为标准状况)如下表所示.资料显示,反应分两步进行:① ,②
,② ,反应过程中能量变化如图所示.下列说法不正确的是
,反应过程中能量变化如图所示.下列说法不正确的是
| 0 | 2 | 4 | 6 |
| 0 | 9.9 | 17.2 | 22.4 |

A.0~6min的平均反应速率: |
B. 的作用是增大过氧化氢的分解速率 的作用是增大过氧化氢的分解速率 |
| C.反应①是吸热反应、反应②是放热反应 |
D.反应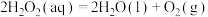 的 的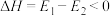 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】某密闭容器中加入0.3 mol A、0.1 mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图甲所示[t0~t1阶段c(B)未画出]。图乙为t2后改变互不相同的某一条件反应速率随时间变化的关系图,t3~t4阶段使用了催化剂。下列说法错误的是


| A.若t1=15 s,生成物C在t0~t1时间段的平均反应速率为 0.004mol·L-1·s-1 |
| B.t4~t5阶段改变的条件为减小压强,t5~t6改变的条件是升高化学反应的温度 |
| C.B的起始物质的量为0.02mol |
D.该化学反应的表达式为:3A B + 2C B + 2C |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
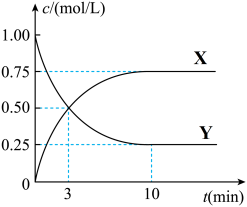
【推荐1】将CO2转化为甲醇的原理为CO2(g)+3H2(g) CH3OH(g)+H2O(g)ΔH<0。500℃时,在体积为100mL的固定容积的密闭容器中充入0.1molCO2、0.3molH2,测得CO2浓度与CH3OH浓度随时间的变化如图所示,从中得出的结论错误的是
CH3OH(g)+H2O(g)ΔH<0。500℃时,在体积为100mL的固定容积的密闭容器中充入0.1molCO2、0.3molH2,测得CO2浓度与CH3OH浓度随时间的变化如图所示,从中得出的结论错误的是
 CH3OH(g)+H2O(g)ΔH<0。500℃时,在体积为100mL的固定容积的密闭容器中充入0.1molCO2、0.3molH2,测得CO2浓度与CH3OH浓度随时间的变化如图所示,从中得出的结论错误的是
CH3OH(g)+H2O(g)ΔH<0。500℃时,在体积为100mL的固定容积的密闭容器中充入0.1molCO2、0.3molH2,测得CO2浓度与CH3OH浓度随时间的变化如图所示,从中得出的结论错误的是
| A.曲线X可以表示CH3OH(g)或H2O(g)的浓度变化 |
| B.平衡时CO2的转化率为75% |
| C.从反应开始到10min时,H2的反应速率v(H2)=0.225mol/(L﹒min) |
| D.500℃时该反应的平衡常数K=3 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
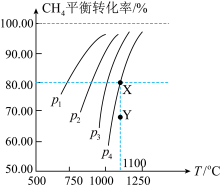
【推荐2】在容积为1L的密闭容器中充入0.1molCO2、0.1molCH4,在一定条件下发生反应CH4(g)+CO2(g) 2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强的关系如图,下列有关说法不正确的是
2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强的关系如图,下列有关说法不正确的是
 2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强的关系如图,下列有关说法不正确的是
2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强的关系如图,下列有关说法不正确的是
| A.该反应的正反应为吸热反应 |
| B.压强:p4>p3>p2>p1 |
| C.1100℃时该反应平衡常数约为1.64 |
| D.压强为p4时,在Y点:v(正)<v(逆) |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
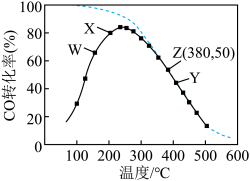
【推荐3】通过甲醇羧基化法取甲酸甲酯(HCOOCH3):CH3OH(g)+CO(g) HCOOCH3(g),在容积固定的密闭容器中,投入等物质的量CH3OH和CO,测得相同时间内CO的转化率随温度变化如图中实线所示(图中虚线表示相同条件下CO的平衡转化率随温度的变化),下列说法不正确的是
HCOOCH3(g),在容积固定的密闭容器中,投入等物质的量CH3OH和CO,测得相同时间内CO的转化率随温度变化如图中实线所示(图中虚线表示相同条件下CO的平衡转化率随温度的变化),下列说法不正确的是
 HCOOCH3(g),在容积固定的密闭容器中,投入等物质的量CH3OH和CO,测得相同时间内CO的转化率随温度变化如图中实线所示(图中虚线表示相同条件下CO的平衡转化率随温度的变化),下列说法不正确的是
HCOOCH3(g),在容积固定的密闭容器中,投入等物质的量CH3OH和CO,测得相同时间内CO的转化率随温度变化如图中实线所示(图中虚线表示相同条件下CO的平衡转化率随温度的变化),下列说法不正确的是
| A.此制取甲酸甲酯的反应△H<0 |
| B.图中X点,延长反应时间能提高CO转化率 |
| C.图中W点,升高温度能提高CO转化率 |
| D.380℃下,图中Z点,c起始(CH3OH)=5.0×10-4 mol/L,CO平衡转化率为50%,则平衡常数K(z)=2000 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】反应X(s)+2Y(g) 2W(g) ∆H =-akJ·mol-1(a>0),一定温度下,在恒容的密闭容器中,加入1molX和2molY发生反应,下列说法正确的是
2W(g) ∆H =-akJ·mol-1(a>0),一定温度下,在恒容的密闭容器中,加入1molX和2molY发生反应,下列说法正确的是
 2W(g) ∆H =-akJ·mol-1(a>0),一定温度下,在恒容的密闭容器中,加入1molX和2molY发生反应,下列说法正确的是
2W(g) ∆H =-akJ·mol-1(a>0),一定温度下,在恒容的密闭容器中,加入1molX和2molY发生反应,下列说法正确的是| A.当容器中气体的压强不再改变时,表明该反应一定已达到平衡状态 |
| B.当达到平衡状态时,X和Y的转化率之比为1:2 |
| C.当Y与W的物质的量浓度之比为1:1时,表明该反应一定已到达平衡状态 |
| D.当容器内气体的密度不再改变时,表明该反应一定已达到平衡状态 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】将1molCO(g)和1molH2O(g)充入某固定容积的反应器中,在一定条件下CO(g)+ H2O(g) CO2(g)+ H2(g)达到一定反应限度时有
CO2(g)+ H2(g)达到一定反应限度时有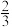 的CO转化成CO2,在相同条件下,将1molCO(g)和2molH2O(g)充入同一反应器中,当反应达到同一反应限度时,混合气体CO2的体积分数可能是( )
的CO转化成CO2,在相同条件下,将1molCO(g)和2molH2O(g)充入同一反应器中,当反应达到同一反应限度时,混合气体CO2的体积分数可能是( )
 CO2(g)+ H2(g)达到一定反应限度时有
CO2(g)+ H2(g)达到一定反应限度时有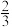 的CO转化成CO2,在相同条件下,将1molCO(g)和2molH2O(g)充入同一反应器中,当反应达到同一反应限度时,混合气体CO2的体积分数可能是( )
的CO转化成CO2,在相同条件下,将1molCO(g)和2molH2O(g)充入同一反应器中,当反应达到同一反应限度时,混合气体CO2的体积分数可能是( )| A.22.2% | B.28.2% | C.33.3% | D.37.8% |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】钴主要应用于电池材料、超级耐热合金、工具钢、硬质合金、磁性材料等传统领域。在相同温度下,某实验小组在容积完全相同的密闭容器中,分别利用如下反应来制备少量钴:①CoO(s)+H2(g) Co(s)+H2O(g)K1,平衡后气体中H2的物质的量分数为0.25;②CoO(s)+CO(g)
Co(s)+H2O(g)K1,平衡后气体中H2的物质的量分数为0.25;②CoO(s)+CO(g) Co(s)+CO2(g)K2,平衡后气体中CO的物质的量分数为0.20。下列说法正确的是
Co(s)+CO2(g)K2,平衡后气体中CO的物质的量分数为0.20。下列说法正确的是
 Co(s)+H2O(g)K1,平衡后气体中H2的物质的量分数为0.25;②CoO(s)+CO(g)
Co(s)+H2O(g)K1,平衡后气体中H2的物质的量分数为0.25;②CoO(s)+CO(g) Co(s)+CO2(g)K2,平衡后气体中CO的物质的量分数为0.20。下列说法正确的是
Co(s)+CO2(g)K2,平衡后气体中CO的物质的量分数为0.20。下列说法正确的是| A.反应①中H2的转化率高于反应②中CO的转化率 |
B.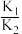 =0.75 =0.75 |
C.反应②的平衡常数表达式为K2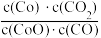 |
D.反应①和反应②达到平衡后: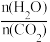 = =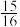 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在不同温度下,向 两个恒温、体积为
两个恒温、体积为 的恒容密闭容器中均通入
的恒容密闭容器中均通入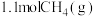 和
和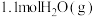 ,发生反应
,发生反应 。测得容器
。测得容器 中
中 物质的量、容器
物质的量、容器 中
中 物质的量随时间的变化曲线如图所示。下列说法正确的是
物质的量随时间的变化曲线如图所示。下列说法正确的是

 两个恒温、体积为
两个恒温、体积为 的恒容密闭容器中均通入
的恒容密闭容器中均通入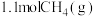 和
和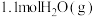 ,发生反应
,发生反应 。测得容器
。测得容器 中
中 物质的量、容器
物质的量、容器 中
中 物质的量随时间的变化曲线如图所示。下列说法正确的是
物质的量随时间的变化曲线如图所示。下列说法正确的是
A.反应 的 的 |
B. 容器前 容器前 用 用 表示的平均反应速率为 表示的平均反应速率为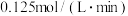 |
C.a容器达到平衡后,再充入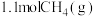 和 和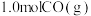 ,此时 ,此时 |
| D.两容器达到平衡时,b容器压强大于a容器压强 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某体积为2L的恒容密闭容器中通入1molCO和 ,一定温度下发生反应:
,一定温度下发生反应: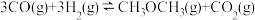 ,10min时达到化学平衡状态,测得
,10min时达到化学平衡状态,测得 的物质的量为0.2mol,下列有关叙述正确的是
的物质的量为0.2mol,下列有关叙述正确的是
 ,一定温度下发生反应:
,一定温度下发生反应: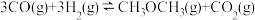 ,10min时达到化学平衡状态,测得
,10min时达到化学平衡状态,测得 的物质的量为0.2mol,下列有关叙述正确的是
的物质的量为0.2mol,下列有关叙述正确的是| A.达平衡后正、逆反应速率相等且均为零 |
B.10min内 的平均速率为 的平均速率为 |
| C.平衡时,CO的转化率为60% |
| D.升高温度,正反应速率加快,逆反应速率减慢 |
您最近半年使用:0次



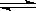 xC(g)+2D(g)。2min末该反应达到平衡,生成0.8mol D,并测得C的浓度为0.2mol·L-1。下列判断错误的是
xC(g)+2D(g)。2min末该反应达到平衡,生成0.8mol D,并测得C的浓度为0.2mol·L-1。下列判断错误的是 。向一体积为1L的恒容密闭容器中充入1mol
。向一体积为1L的恒容密闭容器中充入1mol 和2mol
和2mol ,在一定条件下发生上述反应,测得
,在一定条件下发生上述反应,测得 /mol
/mol
 的转化率
的转化率

