乙基环己烷常用作气相色谱对比样品,也用于有机合成。
(1)乙基环己烷(C8H16)脱氢制苯乙炔(C8H6)的热化学方程式如下:
①C8H16(l) C8H10(l)+3H2(g) ΔH1>0
C8H10(l)+3H2(g) ΔH1>0
②C8H10(l) C8H6(l)+2H2(g) ΔH2=a kJ·mol-1
C8H6(l)+2H2(g) ΔH2=a kJ·mol-1
③C8H6(l)+5H2(g) C8H16(l) ΔH3=b kJ·mol-1
C8H16(l) ΔH3=b kJ·mol-1
则反应①的ΔH1为__________ (用含a、b的代数式表示),有利于提高上述反应①的平衡转化率的条件是____ (填字母)。
A.高温高压 B.低温低压 C.高温低压 D.低温高压
(2)不同压强和温度下乙基环己烷的平衡转化率如下图所示。
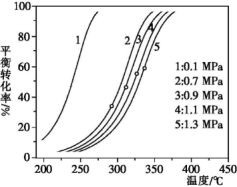
①在相同压强下升高温度,未达到新平衡前,v正____ (填“大于”“小于”或“等于”)v逆。
②研究表明,既升高温度又增大压强,C8H16(l)的转化率也升高,理由可能是____ 。
(3)t ℃,向恒容密闭反应器中充入1.00 mol C8H16(l)进行催化脱氢,测得液态C8H10(l)和C8H6(l)的产率x1和x2(以物质的量分数计)随时间变化关系如下图所示。
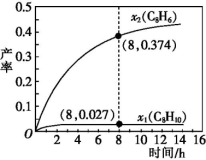
①在8 h时,反应体系内氢气的量为_____ mol(忽略其他副反应),液态C8H16(l)的转化率是_________ 。
②x1显著低于x2的原因是_____________ 。
(1)乙基环己烷(C8H16)脱氢制苯乙炔(C8H6)的热化学方程式如下:
①C8H16(l)
 C8H10(l)+3H2(g) ΔH1>0
C8H10(l)+3H2(g) ΔH1>0②C8H10(l)
 C8H6(l)+2H2(g) ΔH2=a kJ·mol-1
C8H6(l)+2H2(g) ΔH2=a kJ·mol-1 ③C8H6(l)+5H2(g)
 C8H16(l) ΔH3=b kJ·mol-1
C8H16(l) ΔH3=b kJ·mol-1则反应①的ΔH1为
A.高温高压 B.低温低压 C.高温低压 D.低温高压
(2)不同压强和温度下乙基环己烷的平衡转化率如下图所示。

①在相同压强下升高温度,未达到新平衡前,v正
②研究表明,既升高温度又增大压强,C8H16(l)的转化率也升高,理由可能是
(3)t ℃,向恒容密闭反应器中充入1.00 mol C8H16(l)进行催化脱氢,测得液态C8H10(l)和C8H6(l)的产率x1和x2(以物质的量分数计)随时间变化关系如下图所示。

①在8 h时,反应体系内氢气的量为
②x1显著低于x2的原因是
2018·湖南长沙·模拟预测 查看更多[2]
更新时间:2018-12-09 01:11:34
|
相似题推荐
填空题
|
困难
(0.15)
【推荐1】碘是生命体中的必需元素,请根据如下有关碘及其化合物的性质,回答下列问题:
(1) 实验室中制取少量碘可采用如下方法:KI + CuSO4 → A (白色)↓+ K2SO4 + I2。16.0 g CuSO4与过量KI反应后可得19.1 g 的A,写出A的化学式:_______ 。工业生产中,可用智利硝石(含有NaIO3)为原料,与NaHSO3反应后生成碘,写出此反应的离子方程式:_______ 。
(2)单质碘与氟气反应可得IF5,实验表明液态IF5具有一定的导电性,研究人员发现产生这一现象的可能原因在于IF5的自偶电离(如:2H2O⇌H3O++ OH-),生成的阳离子为_______ ;阴离子为_______ 。
(3)将单质碘与铝屑置于管式电炉中,隔绝空气加热至500℃得到棕色片状固体,此固体溶于Na2CO3溶液可产生白色沉淀和气体。请写出上述实验过程中发生的化学反应方程式:_______ ,_______ 。
(4) 某化学课外小组用海带为原料制得少量含碘离子的溶液。现用0.10 mol·L-1的酸性高锰酸钾溶液滴定20.00 mL该溶液需10.25 mL,则该溶液中碘离子的浓度为_______ mol·L-1(精确到0.01)。
(5) I2O5是白色粉末状固体,可用作氧化剂使H2S、CO、HCl等氧化,在合成氨工业中常用I2O5来定量测量CO的含量。已知:
2I2(s)+5O2(g)=2I2O5(s) ΔH=-75.56kJ•mol-1
2CO(g)+O2(g)=2CO2(g) ΔH=-566.0kJ•mol-1
写出CO(g)与I2O5(s)反应析出固态I2的热化学方程式:_______ 。
(1) 实验室中制取少量碘可采用如下方法:KI + CuSO4 → A (白色)↓+ K2SO4 + I2。16.0 g CuSO4与过量KI反应后可得19.1 g 的A,写出A的化学式:
(2)单质碘与氟气反应可得IF5,实验表明液态IF5具有一定的导电性,研究人员发现产生这一现象的可能原因在于IF5的自偶电离(如:2H2O⇌H3O++ OH-),生成的阳离子为
(3)将单质碘与铝屑置于管式电炉中,隔绝空气加热至500℃得到棕色片状固体,此固体溶于Na2CO3溶液可产生白色沉淀和气体。请写出上述实验过程中发生的化学反应方程式:
(4) 某化学课外小组用海带为原料制得少量含碘离子的溶液。现用0.10 mol·L-1的酸性高锰酸钾溶液滴定20.00 mL该溶液需10.25 mL,则该溶液中碘离子的浓度为
(5) I2O5是白色粉末状固体,可用作氧化剂使H2S、CO、HCl等氧化,在合成氨工业中常用I2O5来定量测量CO的含量。已知:
2I2(s)+5O2(g)=2I2O5(s) ΔH=-75.56kJ•mol-1
2CO(g)+O2(g)=2CO2(g) ΔH=-566.0kJ•mol-1
写出CO(g)与I2O5(s)反应析出固态I2的热化学方程式:
您最近一年使用:0次
填空题
|
困难
(0.15)
解题方法
【推荐1】对于一般的化学反应:aA十bB=cC + d D存在速率方程v=k[c(A)]m[c(B)]n,利用速率方程可算得化学反应的瞬时速率;m+n为反应级数,当m+n分别等于0、1、2……时分别称为零级反应、一级反应、二级反应…,k为反应速率常数,k与温度、活化能有关,与浓度无关。
Ⅰ.1073K时,反应:2NO(g) +H2(g)=N2(g) +2H2O(g)的实验数据如下表所示:
(1)通过分析表中实验数据,得该反应的速率方程表达式v=____________ ,为____________ 级反应。
Ⅱ.已知可逆反应A(g) B(g)的正、逆反应均为一级反应,且存在如下数据:
B(g)的正、逆反应均为一级反应,且存在如下数据:
试回答下列问题:
(2)600K时反应的平衡常数K=____________ ;
(3)正反应的△H____________ 0(填“>”或“<”)。
(4)850K时在容积为VL的恒容密闭容器中充入3 mol气体A,一段时间后达平衡。下列说法正确的是____________ (填序号)。
(5)600K时,在容积为1L的恒容密闭容器中充入2mol气体A,已知反应过程中物质的浓度、速率常数和反应时间之间满足如下关系:2.30lg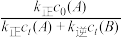 =(k正+k逆)t,[c0(A)为反应物A的起始浓度,ct(A)、ct(B)分别为A, B任意时刻的浓度,k为反应速率常数,t为反应时间〕,则:
=(k正+k逆)t,[c0(A)为反应物A的起始浓度,ct(A)、ct(B)分别为A, B任意时刻的浓度,k为反应速率常数,t为反应时间〕,则:
①t =__________ min时反应达平衡。
②反应一段时间后A, B浓度相等,则这段时间内正反应的平均反应速率v=_________ mol/( L·min)(保留整数);此时,逆反应的瞬时速率v=_________ mol/( L·min) (已知lg2=0.3, lg5=0.7)
Ⅰ.1073K时,反应:2NO(g) +H2(g)=N2(g) +2H2O(g)的实验数据如下表所示:
| 实验编号 | 初始浓度(mol·L-1) | 初始速率(mol·L-1·min-1) | |
| c(H2) | c(NO) | v | |
| 1 | 0.0060 | 0.0010 | 8.00×10-7 |
| 2 | 0.0060 | 0.0020 | 3.20×10-6 |
| 3 | 0.0060 | 0.0040 | 1.28×10-5 |
| 4 | 0.0030 | 0.0040 | 6.40×10-6 |
| 5 | 0.0015 | 0.0040 | 3.20×10-6 |
Ⅱ.已知可逆反应A(g)
 B(g)的正、逆反应均为一级反应,且存在如下数据:
B(g)的正、逆反应均为一级反应,且存在如下数据:| 温度(K) | 600 | 850 | |
| 速率常数 | k正(min-1) | 32 | 70 |
| k逆(min-1) | 8 | 12 | |
试回答下列问题:
(2)600K时反应的平衡常数K=
(3)正反应的△H
(4)850K时在容积为VL的恒容密闭容器中充入3 mol气体A,一段时间后达平衡。下列说法正确的是____________ (填序号)。
| A.恒温条件下,再向容器内加入一定量的气体A,达到新平衡时,A的转化率减小,体积分数增大 |
B.升高温度, 、 、 均增大,且 均增大,且 增大幅度大 增大幅度大 |
C.使用催化剂, 、 、 均增大,且比值不变 均增大,且比值不变 |
| D.达平衡后的任意时段内,正、逆反应的平均速率为零、瞬时速率也为零 |
| E.平衡时,混合气体的平均摩尔质量与起始时相同 |
| F.若在同温、同体积的恒容密闭绝热容器中,充入1.5mol气体B,达平衡时,A的浓度为上述平衡时的一半 |
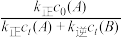 =(k正+k逆)t,[c0(A)为反应物A的起始浓度,ct(A)、ct(B)分别为A, B任意时刻的浓度,k为反应速率常数,t为反应时间〕,则:
=(k正+k逆)t,[c0(A)为反应物A的起始浓度,ct(A)、ct(B)分别为A, B任意时刻的浓度,k为反应速率常数,t为反应时间〕,则:①t =
②反应一段时间后A, B浓度相等,则这段时间内正反应的平均反应速率v=
您最近一年使用:0次
填空题
|
困难
(0.15)
解题方法
【推荐2】氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟制备氨基甲酸铵,并探究其分解反应平衡常数。反应的化学方程式: 2NH3(g)+CO2(g) NH2COONH4(s)。请按要求回答下列问题:
NH2COONH4(s)。请按要求回答下列问题:
(1)请在下图1方框内画出用浓氨水与生石灰制取氨气的装置简图______ 。
(2)氨基甲酸铵的装置如下图2所示。生成的氨基甲酸铵小晶体悬浮在四氯化碳中。
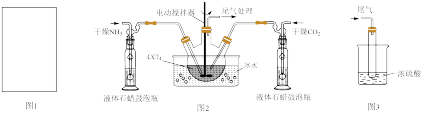
①从反应后的混合物中分离出产品的实验方法是______ (填操作名称)。
②上图3中浓硫酸的作用是______ 。
(3)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡。实验测得不同温度下的平衡数据列于下表:
①下列选项可以判断该分解反应达到平衡的是______ 。
A.2v(NH3)=v(CO2)
B.密闭容器内物质总质量不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
②该分解反应的焓变ΔH______ 0(填 “>”、“=”或“<”),25.0℃时分解平衡常数的值=______ 。
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0℃下达到分解平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量将______ (填“增加”,“减少”或“不变”)。
 NH2COONH4(s)。请按要求回答下列问题:
NH2COONH4(s)。请按要求回答下列问题:(1)请在下图1方框内画出用浓氨水与生石灰制取氨气的装置简图
(2)氨基甲酸铵的装置如下图2所示。生成的氨基甲酸铵小晶体悬浮在四氯化碳中。

①从反应后的混合物中分离出产品的实验方法是
②上图3中浓硫酸的作用是
(3)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡。实验测得不同温度下的平衡数据列于下表:
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度(×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
A.2v(NH3)=v(CO2)
B.密闭容器内物质总质量不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
②该分解反应的焓变ΔH
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0℃下达到分解平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量将
您最近一年使用:0次
填空题
|
困难
(0.15)
【推荐3】目前,“低碳经济”备受关注,CO2的产生及有效开发利用成为科学家研究的重要课题。试运用所学知识,解决下列问题:
(1)已知某反应的平衡表达式为: 它所对应的化学反应为:
它所对应的化学反应为:_______
(2)—定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器中,发生(1)中反应:其相关数据如下表所示:
①T10C时,该反应的平衡常数K=_______
②乙容器中,当反应进行到1.5min时,H2O(g)的物质的量浓度_______ (填选项字母)。
A.=0.8mol·L-1 B.=1.4 mol·L-1 C.<1.4 mol·L-1 D.>1.4 mol·L-1
③丙容器的容积为1L,T1℃时,按下列配比充入C(s)、H2O(g)、CO2(g)和H2(g), 达到平 衡时各气体的体积分数与甲容器完全相同的是_______ (填选项字母)。
A.0.6 mol、1.0 mol、0.5 mol、1.0 mol
B. 0.6 mol、2.0 mol、0 mol、0 mol
C.1.0 mol、2.0 mol、1.0 mol、2.0 mol
D. 0.25 mol、0.5 mol、0.75 mol、1.5 mol
(3)在一定条件下,科学家利用从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇,已知CH3OH、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式:______________________________ 。
(4)将燃煤废气中的CO2转化为甲醚的反应原理为:
2CO2(g)+ 6H2(g)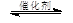 CH3OCH3(g)+ 3H2O(g)
CH3OCH3(g)+ 3H2O(g)
已知一定压强下,该反应在不同温度、不同投料比时,CO2的转化率见下表:
①该反应的焓变△H__ 0,熵变△S___ 0(填>、<或=)。
②用甲醚作为燃料电池原料,在碱性介质中该电池负极的电极反应式______________ 。若以1.12 L·min-1(标准状况)的速率向该电池中通入甲醚(沸点为-24.9 ℃),用该电池电解500 mL 2 mol·L-1 CuSO4溶液,通电0.50 min后,理论上可析出金属铜________ g。
(1)已知某反应的平衡表达式为:
 它所对应的化学反应为:
它所对应的化学反应为:(2)—定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器中,发生(1)中反应:其相关数据如下表所示:
| 容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol[ | 达到平衡所需时间/min | |
| C(s) | H2O(g) | H2(g) | ||||
| 甲 | 2 | T1 | 2 | 4 | 3.2 | 8 |
| 乙 | 1 | T2 | 1 | 2 | 1.2 | 3 |
①T10C时,该反应的平衡常数K=
②乙容器中,当反应进行到1.5min时,H2O(g)的物质的量浓度
A.=0.8mol·L-1 B.=1.4 mol·L-1 C.<1.4 mol·L-1 D.>1.4 mol·L-1
③丙容器的容积为1L,T1℃时,按下列配比充入C(s)、H2O(g)、CO2(g)和H2(g), 达到平 衡时各气体的体积分数与甲容器完全相同的是
A.0.6 mol、1.0 mol、0.5 mol、1.0 mol
B. 0.6 mol、2.0 mol、0 mol、0 mol
C.1.0 mol、2.0 mol、1.0 mol、2.0 mol
D. 0.25 mol、0.5 mol、0.75 mol、1.5 mol
(3)在一定条件下,科学家利用从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇,已知CH3OH、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式:
(4)将燃煤废气中的CO2转化为甲醚的反应原理为:
2CO2(g)+ 6H2(g)
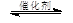 CH3OCH3(g)+ 3H2O(g)
CH3OCH3(g)+ 3H2O(g)已知一定压强下,该反应在不同温度、不同投料比时,CO2的转化率见下表:
| 投料比[n(H2)/ n(CO2)] | 500 K | 600 K | 700 K | 800 K |
| 1.5 | 45% | 33% | 20% | 12% |
| 2.0 | 60% | 43% | 28% | 15% |
| 3.0 | 83% | 62% | 37% | 22% |
①该反应的焓变△H
②用甲醚作为燃料电池原料,在碱性介质中该电池负极的电极反应式
您最近一年使用:0次
填空题
|
困难
(0.15)
【推荐1】从图表中获得有用的信息是化学学习和研究的重要能力。
(1)图1是在一定条件下,反应:CH4(g)+CO2(g) 2CO(g)+2H2(g)的实验曲线。
2CO(g)+2H2(g)的实验曲线。
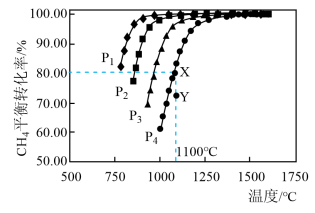
①图中P1、P2、P3、P4代表不同压强,则压强大小的排列顺序为___________ 。该反应的△H____ 0(选填“>”、“<”、“=”)。
②压强为 P4时,在 Y 点:υ(正)____ υ(逆)。(选填“>”、“<”、“=”);
③压强为P4时,密闭容器中CH4和CO2的起始浓度均为0.10 mol•L-1,则1100℃时该反应的化学平衡常数
为________ (保留三位有效数字)。
(2)温度与HCl压强对MgCl2·6H2O受热分解产物的影响如图所示,下列说法正确的是( )
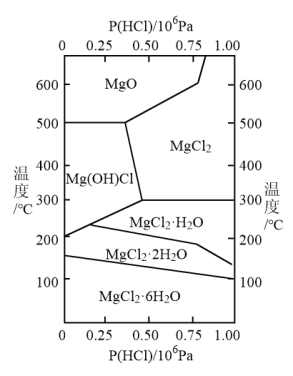
A.温度低于100℃,MgCl2·6H2O不会发生分解
B.要得到MgO温度至少需要加热至600℃
C.要得到无水MgCl2只要控制温度,不一定要在HCl气体中
D.在HCl气体压强为0.25×106Pa时,温度由室温升高至300℃,发生的反应为MgCl2·6H2O=Mg(OH)Cl+HCl+5H2O
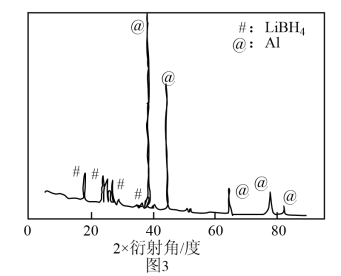
(3)X-射线衍射可用于判断某晶态物质是否存在。Al-LiBH4是新型产氢复合材料,常温下可以与H2O反应生成H2。图3是含LiBH4为25%时Al-LiBH4复合材料的X-射线衍射图谱,图4是该复合材料在25℃(图谱a)和75℃(图谱b)时与水反应后残留固体物质的X-射线衍射图谱。据图分析,25℃时Al-LiBH4复合材料中与水完全反应的物质是___ (填化学式),25℃和75℃时产物中不相同的物质是________ (填化学式)。

(1)图1是在一定条件下,反应:CH4(g)+CO2(g)
 2CO(g)+2H2(g)的实验曲线。
2CO(g)+2H2(g)的实验曲线。
①图中P1、P2、P3、P4代表不同压强,则压强大小的排列顺序为
②压强为 P4时,在 Y 点:υ(正)
③压强为P4时,密闭容器中CH4和CO2的起始浓度均为0.10 mol•L-1,则1100℃时该反应的化学平衡常数
为
(2)温度与HCl压强对MgCl2·6H2O受热分解产物的影响如图所示,下列说法正确的是

A.温度低于100℃,MgCl2·6H2O不会发生分解
B.要得到MgO温度至少需要加热至600℃
C.要得到无水MgCl2只要控制温度,不一定要在HCl气体中
D.在HCl气体压强为0.25×106Pa时,温度由室温升高至300℃,发生的反应为MgCl2·6H2O=Mg(OH)Cl+HCl+5H2O
(3)X-射线衍射可用于判断某晶态物质是否存在。Al-LiBH4是新型产氢复合材料,常温下可以与H2O反应生成H2。图3是含LiBH4为25%时Al-LiBH4复合材料的X-射线衍射图谱,图4是该复合材料在25℃(图谱a)和75℃(图谱b)时与水反应后残留固体物质的X-射线衍射图谱。据图分析,25℃时Al-LiBH4复合材料中与水完全反应的物质是


您最近一年使用:0次
填空题
|
困难
(0.15)
解题方法
【推荐2】目前,汽车尾气系统中均安装了催化转化器。在催化转化器中,汽车尾气中的CO和NO在催化剂的作用下发生反应: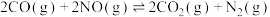

(1)已知:①
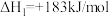
②
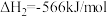
则
_______ kJ/mol。
(2)将CO和NO以一定流速通过两种不同的催化剂发生反应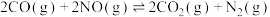 ,相同时间内测量逸出气体中
,相同时间内测量逸出气体中 的含量,从而确定尾气脱氮率(即NO的转化率),结果下图所示。
的含量,从而确定尾气脱氮率(即NO的转化率),结果下图所示。

①a点的
_______ b点的 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②c点_______ (填“是”或“否”)一定是平衡状态,理由是_______ 。
③研究表明氧气的存在对于NO的还原有抑制作用,原因是_______ 。
(3)对于反应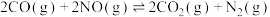 ,实验测得:
,实验测得: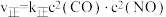 ,
,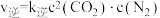 ,
, 、
、 分别是正、逆反应速率常数,且只是温度的函数。下列说法中正确的是
分别是正、逆反应速率常数,且只是温度的函数。下列说法中正确的是_______ 。
A.反应余热可以进入温差发电器为电能汽车提供动力
B.使用不同的催化剂反应的活化能随之改变
C.其他条件不变,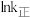 随1/T增大而增大
随1/T增大而增大
(4)T℃,将2molNO(g)和2molCO(g)通入体积为1L的恒容密闭容器发生上述反应,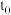 时达到平衡,测得反应过程中CO的转化率与时间的关系如下图,则a点处对应的
时达到平衡,测得反应过程中CO的转化率与时间的关系如下图,则a点处对应的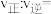
_______ 。

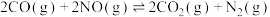

(1)已知:①

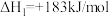
②

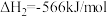
则

(2)将CO和NO以一定流速通过两种不同的催化剂发生反应
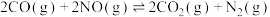 ,相同时间内测量逸出气体中
,相同时间内测量逸出气体中 的含量,从而确定尾气脱氮率(即NO的转化率),结果下图所示。
的含量,从而确定尾气脱氮率(即NO的转化率),结果下图所示。
①a点的

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②c点
③研究表明氧气的存在对于NO的还原有抑制作用,原因是
(3)对于反应
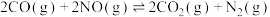 ,实验测得:
,实验测得: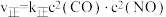 ,
,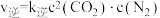 ,
, 、
、 分别是正、逆反应速率常数,且只是温度的函数。下列说法中正确的是
分别是正、逆反应速率常数,且只是温度的函数。下列说法中正确的是A.反应余热可以进入温差发电器为电能汽车提供动力
B.使用不同的催化剂反应的活化能随之改变
C.其他条件不变,
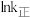 随1/T增大而增大
随1/T增大而增大(4)T℃,将2molNO(g)和2molCO(g)通入体积为1L的恒容密闭容器发生上述反应,
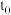 时达到平衡,测得反应过程中CO的转化率与时间的关系如下图,则a点处对应的
时达到平衡,测得反应过程中CO的转化率与时间的关系如下图,则a点处对应的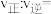

您最近一年使用:0次
填空题
|
困难
(0.15)
名校
解题方法
【推荐3】碳和氮的化合物在生产生活中广泛存在。回答下列问题:
(1)三氯化氮(NCl3)是一种黄色、油状、具有刺激性气味的挥发性有毒液体,各原子均满足8电子稳定结构。其电子式是_______ 。氯碱工业生产时,由于食盐水中通常含有少量NH4Cl,而在阳极区与生成的氯气反应产生少量NCl3,该反应的化学方程式为_______ 。
(2)利用CO可以将NO转化为无害的N2,其反应为: 2NO(g) +2CO(g) N2(g) +2CO2(g),向容积均为1L的甲、乙两个恒温(温度分别为300℃、T℃)容器中分别加入2.00molNO和2.00molCO,测得各容器中n(CO)随反应时间t的变化情况如下表所示:
N2(g) +2CO2(g),向容积均为1L的甲、乙两个恒温(温度分别为300℃、T℃)容器中分别加入2.00molNO和2.00molCO,测得各容器中n(CO)随反应时间t的变化情况如下表所示:
①甲容器中,0~40min 内用NO的浓度变化表示的反应速率v(NO)=___ 。
②该反应的△H_____ 0(填“>”或“<”)。
③甲容器反应达到平衡后,若容器内各物质的量均增加1倍,则平衡_____ (填“正向”、“逆向”或“不”)移动。
(3)H2A为二元弱酸。室温下配制一系列c(H2A)+c(HA−)+c(A2−)=0.100 mol∙L−1的H2A与NaOH的混合溶液。测得H2A、HA−、A2−的物质的量分数c(x)%(c(x)%= ×100%)随pH变化如图所示。
×100%)随pH变化如图所示。_______ 。
②室温下,若将0.100 mol∙L−1的H2A与a mol∙L−1的NaOH溶液等体积混合,使溶液的pH=7。则H2A的Ka2=______ mol∙L−1 (用a表示)
(4)将FeSO4置入抽空的刚性容器中,升高温度发生分解反应:2FeSO4(s) Fe2O3(s)+SO2(g)+SO3(g) (Ⅰ)。平衡时PSO3-T的关系如下图所示。660K时,该反应的平衡常数Kp(Ⅰ)=
Fe2O3(s)+SO2(g)+SO3(g) (Ⅰ)。平衡时PSO3-T的关系如下图所示。660K时,该反应的平衡常数Kp(Ⅰ)=______ (kPa)2,Kp (Ⅰ)随反应温度升高而______ (填“增大”“减小”或“不变”)。
(1)三氯化氮(NCl3)是一种黄色、油状、具有刺激性气味的挥发性有毒液体,各原子均满足8电子稳定结构。其电子式是
(2)利用CO可以将NO转化为无害的N2,其反应为: 2NO(g) +2CO(g)
 N2(g) +2CO2(g),向容积均为1L的甲、乙两个恒温(温度分别为300℃、T℃)容器中分别加入2.00molNO和2.00molCO,测得各容器中n(CO)随反应时间t的变化情况如下表所示:
N2(g) +2CO2(g),向容积均为1L的甲、乙两个恒温(温度分别为300℃、T℃)容器中分别加入2.00molNO和2.00molCO,测得各容器中n(CO)随反应时间t的变化情况如下表所示:| t/min | 0 | 40 | 80 | 120 | 160 |
| N甲(CO)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| N乙(CO)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
②该反应的△H
③甲容器反应达到平衡后,若容器内各物质的量均增加1倍,则平衡
(3)H2A为二元弱酸。室温下配制一系列c(H2A)+c(HA−)+c(A2−)=0.100 mol∙L−1的H2A与NaOH的混合溶液。测得H2A、HA−、A2−的物质的量分数c(x)%(c(x)%=
 ×100%)随pH变化如图所示。
×100%)随pH变化如图所示。
②室温下,若将0.100 mol∙L−1的H2A与a mol∙L−1的NaOH溶液等体积混合,使溶液的pH=7。则H2A的Ka2=
(4)将FeSO4置入抽空的刚性容器中,升高温度发生分解反应:2FeSO4(s)
 Fe2O3(s)+SO2(g)+SO3(g) (Ⅰ)。平衡时PSO3-T的关系如下图所示。660K时,该反应的平衡常数Kp(Ⅰ)=
Fe2O3(s)+SO2(g)+SO3(g) (Ⅰ)。平衡时PSO3-T的关系如下图所示。660K时,该反应的平衡常数Kp(Ⅰ)=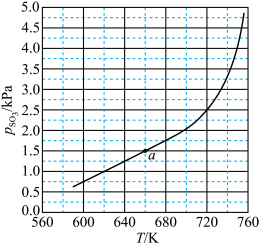
您最近一年使用:0次
填空题
|
困难
(0.15)
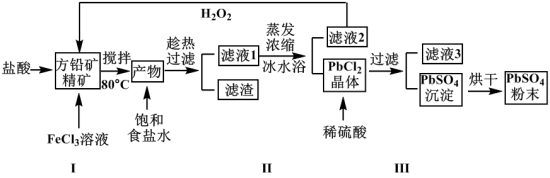
【推荐1】硫酸铅(PbSO4)广泛应用于制造铅蓄电池、白色颜料等。利用方铅矿精矿(PbS)直接制备硫酸铅粉末的流程如下:
已知:(ⅰ)PbCl2(s)+2Cl-(aq)

 (aq) △H>0
(aq) △H>0
(ⅱ)Ksp(PbSO4)=1.08×10-8,Ksp(PbCl2)=1.6×10-5
(ⅲ)Fe3+、Pb2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、7.04
(1)步骤Ⅰ中FeCl3溶液与PbS反应生成PbCl2和S的离子方程式为_____________________ ,步骤Ⅰ中另一个反应是H2O2与FeCl2、盐酸反应生成FeCl3,实现FeCl3的重复利用,其离子方程式为__________ ,加入盐酸的另一个目的是为了控制pH在0.5~1.0,原因是_____________________________ 。
(2)用化学平衡移动的原理解释步骤Ⅱ中使用冰水浴的原因___________________________ 。
(3)写出PbCl2晶体转化为PbSO4沉淀的离子方程式__________________________________ 。
(4)滤液3是_______________ 。
(5)铅蓄电池的电解液是稀硫酸(22%~28%),充电后两个电极上沉积的PbSO4分别转化为PbO2和Pb,铅蓄电池充电时阴极的电极反应式为________________________________ 。

已知:(ⅰ)PbCl2(s)+2Cl-(aq)


 (aq) △H>0
(aq) △H>0(ⅱ)Ksp(PbSO4)=1.08×10-8,Ksp(PbCl2)=1.6×10-5
(ⅲ)Fe3+、Pb2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、7.04
(1)步骤Ⅰ中FeCl3溶液与PbS反应生成PbCl2和S的离子方程式为
(2)用化学平衡移动的原理解释步骤Ⅱ中使用冰水浴的原因
(3)写出PbCl2晶体转化为PbSO4沉淀的离子方程式
(4)滤液3是
(5)铅蓄电池的电解液是稀硫酸(22%~28%),充电后两个电极上沉积的PbSO4分别转化为PbO2和Pb,铅蓄电池充电时阴极的电极反应式为
您最近一年使用:0次
填空题
|
困难
(0.15)
名校
解题方法
【推荐2】硫化钠主要用于皮革、毛纺、高档纸张、染料等行业。生产硫化钠大多采用无水芒硝(Na2SO4)—炭粉还原法,其流程示意图如下:

(1)若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生的总的化学反应方程式为____ 。
(2)上述流程中采用稀碱液比用热水更好,理由是___________ 。
(3)常温下,取硫化钠晶体(含少量NaOH)加入到硫酸铜溶液中,充分搅拌。若反应后测得溶液的pH=4,则此时溶液中c( S2-)=___ mol·L-1。
(已知:常温时CuS、Cu(OH)2的Ksp分别为8.8×10-36、2.2×10-20)
(4)①皮革工业废水中的汞常用硫化钠除去,汞的去除率与溶液的pH和x(x代表硫化钠的实际用量与理论用量的比值)有关(如图所示)。为使除汞效果最佳,应控制的条件是:x=___ ,pH控制在___ 范围。
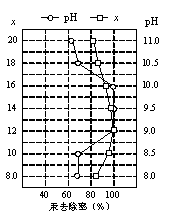
②某毛纺厂废水中含0.001 mol·L-1的硫化钠,与纸张漂白后的废水(含0.002 mol·L-1NaClO)按1:2的体积比混合,能同时较好处理两种废水,处理后的废水中所含的主要阴离子有_____ 。
(5)常温下利用Fe2+、Fe3+的相互转化,可将SO2转化为SO42-而实现SO2的处理(总反应为2SO2+O2+2H2O=2H2SO4)。已知,含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2+ + O2+ 4H+ =4Fe3+ + 2H2O,则另一反应的离子方程式为___________ 。

(1)若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生的总的化学反应方程式为
(2)上述流程中采用稀碱液比用热水更好,理由是
(3)常温下,取硫化钠晶体(含少量NaOH)加入到硫酸铜溶液中,充分搅拌。若反应后测得溶液的pH=4,则此时溶液中c( S2-)=
(已知:常温时CuS、Cu(OH)2的Ksp分别为8.8×10-36、2.2×10-20)
(4)①皮革工业废水中的汞常用硫化钠除去,汞的去除率与溶液的pH和x(x代表硫化钠的实际用量与理论用量的比值)有关(如图所示)。为使除汞效果最佳,应控制的条件是:x=

②某毛纺厂废水中含0.001 mol·L-1的硫化钠,与纸张漂白后的废水(含0.002 mol·L-1NaClO)按1:2的体积比混合,能同时较好处理两种废水,处理后的废水中所含的主要阴离子有
(5)常温下利用Fe2+、Fe3+的相互转化,可将SO2转化为SO42-而实现SO2的处理(总反应为2SO2+O2+2H2O=2H2SO4)。已知,含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2+ + O2+ 4H+ =4Fe3+ + 2H2O,则另一反应的离子方程式为
您最近一年使用:0次
填空题
|
困难
(0.15)
名校
解题方法
【推荐3】乙烯是制造塑料、合成橡胶和合成纤维等化学产品的基本原料。C2H6裂解制C2H4是化学工业的一个重要研究课题,目前裂解方法有电催化、光催化裂解、直接裂解、氧气或二氧化碳氧化乙烷裂解等。乙烷直接裂解、乙烷二氧化碳氧化裂解和乙烷氧气氧化裂解的反应如下:
(Ⅰ)C2H6(g) C2H4(g)+H2(g) △H1=+125kJ·mol-1
C2H4(g)+H2(g) △H1=+125kJ·mol-1
(Ⅱ)CO2(g)+C2H6(g) C2H4(g)+CO(g)+H2O(g) △H2=+177kJ·mol-1
C2H4(g)+CO(g)+H2O(g) △H2=+177kJ·mol-1
(Ⅲ)2C2H6(g)+O2(g) 2C2H4(g)+2H2O(g) △H3=-211.6kJ·mol-1
2C2H4(g)+2H2O(g) △H3=-211.6kJ·mol-1
回答下列问题:
(1)已知键能:E(C—H)=416kJ·mol-1,E(H—H)=436kJ·mol-1,由此计算生成1mol碳碳π键放出的能量为_______ kJ。
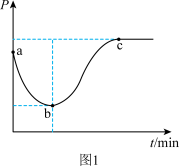
(2)在一绝热的恒容密闭容器中,通入一定量的C2H6发生反应(Ⅰ),反应过程中容器内压强(P)与时间(t)变化如图1所示,随着反应进行,a~b段压强减小的原因是_______ 。
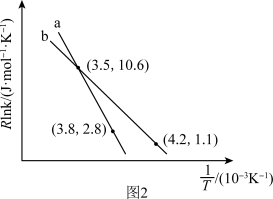
(3)反应(Ⅱ)的Arrhenius经验公式实验数据如图2中曲线a所示,已知Arrhenius经验公式Rlnk=- +C(Ea为活化能,k为速率常数,R和C为常数)。反应的活化能Ea=
+C(Ea为活化能,k为速率常数,R和C为常数)。反应的活化能Ea=_______ kJ·mol-1。当改变外界条件时,实验数据如图中曲线b所示,则实验可能改变的外界条件是_______ 。
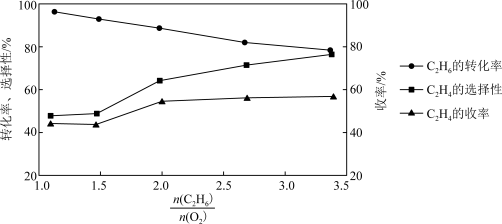
(4)乙烷氧气氧化裂解制乙烯,除发生反应(Ⅲ)之外,还发生副反应(Ⅳ):2C2H6(g)+7O2(g) 4CO2(g)+6H2O(g)。在800℃时用乙烷氧气氧化裂解制乙烯,乙烷的转化率、乙烯的选择性和收率随投料比
4CO2(g)+6H2O(g)。在800℃时用乙烷氧气氧化裂解制乙烯,乙烷的转化率、乙烯的选择性和收率随投料比 的变化关系如图所示:
的变化关系如图所示:
已知:C2H4的选择性=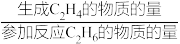 ×100%
×100%
C2H4的收率=C2H6的转化率×C2H4的选择性
①控制 =2而不采用选择性更高的
=2而不采用选择性更高的 =3.5,除可防止积碳外,另一原因是
=3.5,除可防止积碳外,另一原因是_______ ; <2时,
<2时, 越小,乙烷的转化率越大,乙烯的选择性和收率越小的原因是
越小,乙烷的转化率越大,乙烯的选择性和收率越小的原因是_______ 。
②一定温度和压强为5.8pMPa条件下,将C2H6和O2按物质的量之比为2∶3通入密闭弹性容器中发生反应,平衡时,C2H4选择性为60%,C2H4的收率为48%。该温度下,反应2C2H6(g)+O2(g) 2C2H4(g)+2H2O(g)的Kp=
2C2H4(g)+2H2O(g)的Kp=_______ (用含字母p的代数式表示,带单位。已知Kp是用反应体系中气体的分压来表示的平衡常数,分压=总压×物质的量分数)。
(Ⅰ)C2H6(g)
 C2H4(g)+H2(g) △H1=+125kJ·mol-1
C2H4(g)+H2(g) △H1=+125kJ·mol-1(Ⅱ)CO2(g)+C2H6(g)
 C2H4(g)+CO(g)+H2O(g) △H2=+177kJ·mol-1
C2H4(g)+CO(g)+H2O(g) △H2=+177kJ·mol-1(Ⅲ)2C2H6(g)+O2(g)
 2C2H4(g)+2H2O(g) △H3=-211.6kJ·mol-1
2C2H4(g)+2H2O(g) △H3=-211.6kJ·mol-1回答下列问题:
(1)已知键能:E(C—H)=416kJ·mol-1,E(H—H)=436kJ·mol-1,由此计算生成1mol碳碳π键放出的能量为
(2)在一绝热的恒容密闭容器中,通入一定量的C2H6发生反应(Ⅰ),反应过程中容器内压强(P)与时间(t)变化如图1所示,随着反应进行,a~b段压强减小的原因是

(3)反应(Ⅱ)的Arrhenius经验公式实验数据如图2中曲线a所示,已知Arrhenius经验公式Rlnk=-
 +C(Ea为活化能,k为速率常数,R和C为常数)。反应的活化能Ea=
+C(Ea为活化能,k为速率常数,R和C为常数)。反应的活化能Ea=
(4)乙烷氧气氧化裂解制乙烯,除发生反应(Ⅲ)之外,还发生副反应(Ⅳ):2C2H6(g)+7O2(g)
 4CO2(g)+6H2O(g)。在800℃时用乙烷氧气氧化裂解制乙烯,乙烷的转化率、乙烯的选择性和收率随投料比
4CO2(g)+6H2O(g)。在800℃时用乙烷氧气氧化裂解制乙烯,乙烷的转化率、乙烯的选择性和收率随投料比 的变化关系如图所示:
的变化关系如图所示:
已知:C2H4的选择性=
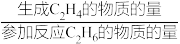 ×100%
×100%C2H4的收率=C2H6的转化率×C2H4的选择性
①控制
 =2而不采用选择性更高的
=2而不采用选择性更高的 =3.5,除可防止积碳外,另一原因是
=3.5,除可防止积碳外,另一原因是 <2时,
<2时, 越小,乙烷的转化率越大,乙烯的选择性和收率越小的原因是
越小,乙烷的转化率越大,乙烯的选择性和收率越小的原因是②一定温度和压强为5.8pMPa条件下,将C2H6和O2按物质的量之比为2∶3通入密闭弹性容器中发生反应,平衡时,C2H4选择性为60%,C2H4的收率为48%。该温度下,反应2C2H6(g)+O2(g)
 2C2H4(g)+2H2O(g)的Kp=
2C2H4(g)+2H2O(g)的Kp=
您最近一年使用:0次



