氮及其化合物如NH3及铵盐、N2H4、N2O4等在中学化学、化工工业、国防等领域占有重要地位。
(1)已知反应NO2(g)+CO(g) = NO(g) +CO2(g)的能量变化如上图所示,下列说法正确的是________ 。

(2)N2O4与NO2之间存在反应N2O4(g) 2NO2(g)。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度的变化如图所示。
2NO2(g)。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度的变化如图所示。
①由图推测该反应的△H___ 0(填“>”或“<”),理由为________________ 。
②图中a点对应温度下,已知N2O4的起始压强为108 kPa,则该温度下反应的平衡常数Kp=_________ kPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③在一定条件下,该反应N2O4、NO2的消耗速率与自身压强间存在关系υ( N2O4)=k1p(N2O4),υ(NO2)=k2p2(NO2),其中k1、k2是与反应温度有关的常数。相应的速率压强关系如图所示,一定温度下,k1、k2与平衡常数Kp的关系是k1=___________ ,在下图上标出的点中,能表示反应达到平衡状态的点为__________ (填字母代号)。
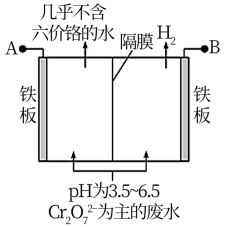
(3)采用电解法处理含铬废水原理如下图所示。阳极的电极反应式为___________ ,阳极区溶液中发生反应: ________________________ ,阴极产生的气体为_______ (填化学式)。
(1)已知反应NO2(g)+CO(g) = NO(g) +CO2(g)的能量变化如上图所示,下列说法正确的是

A.图中A→B的过程为放热过程
B.1molNO2和1molCO的键能总和大于1molNO和1molCO2的键能总和
C.该反应为氧化还原反应
D.1molNO2(g)和1molCO(g)的总能量低于1molNO(g)和1molCO2(g)的总能量
(2)N2O4与NO2之间存在反应N2O4(g)
 2NO2(g)。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度的变化如图所示。
2NO2(g)。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度的变化如图所示。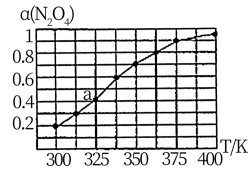
①由图推测该反应的△H
②图中a点对应温度下,已知N2O4的起始压强为108 kPa,则该温度下反应的平衡常数Kp=
③在一定条件下,该反应N2O4、NO2的消耗速率与自身压强间存在关系υ( N2O4)=k1p(N2O4),υ(NO2)=k2p2(NO2),其中k1、k2是与反应温度有关的常数。相应的速率压强关系如图所示,一定温度下,k1、k2与平衡常数Kp的关系是k1=

(3)采用电解法处理含铬废水原理如下图所示。阳极的电极反应式为
更新时间:2018-12-20 22:23:04
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】氮和碳的化合物在生产生活中应用广泛。
(1)①氯胺(NH2Cl)的电子式为_______________ 。
②NH2Cl与水反应生成强氧化性的物质,可作长效缓释消毒剂,该反应的化学方程式为__________________ 。
(2)用焦炭还原NO的反应为:2NO(g)+C(s) N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
①该反应为_______________ (填“放热”或“吸热”)反应。
②乙容器在200min达到平衡状态,则0~200min内用NO的浓度变化表示的平均反应速率v(NO)=___________ 。
(3)用焦炭还原NO2的反应为:2NO2(g)+2C(s) N2(g)+2CO2(g),在恒温条件下,1mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如下图所示:
N2(g)+2CO2(g),在恒温条件下,1mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如下图所示:

①A、B两点的浓度平衡常数关系:Kc(A)_____ Kc(B)(填“<”或“>”或“=”)。
②A、B、C三点中NO2的转化率最高的是__________ (填“A”或“B”或“C”)点。
③计算C点时该反应的压强平衡常数Kp(C)=________ (Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)最新研究发现,用隔膜电解法可以处理高浓度乙醛废水。原理:使用惰性电极电解,乙醛分别在阴、阳极转化为乙醇和乙酸,总反应为:2CH3CHO+H2O CH3CH2OH+CH3COOH。实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的 处理过程,其装置示意图如下图所示:
CH3CH2OH+CH3COOH。实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的 处理过程,其装置示意图如下图所示:
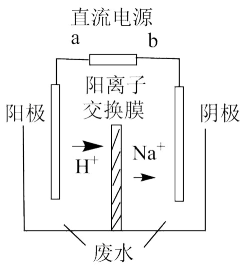
①试写出电解过程中,阴极的电极反应式:_________________________ 。
②在实际处理过程中,当电路中I=50A时,10min处理乙醛8.8g,则电流效率为__ (计算结果保留3位有效数字,每个电子的电量为1.6×10-19C,电流效率=实际反应所需电量/电路中通过电量×100%)。
(1)①氯胺(NH2Cl)的电子式为
②NH2Cl与水反应生成强氧化性的物质,可作长效缓释消毒剂,该反应的化学方程式为
(2)用焦炭还原NO的反应为:2NO(g)+C(s)
 N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:| t/min | 0 | 40 | 80 | 120 | 160 |
| n(NO)(甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| n(NO)(乙容器)/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
| n(NO)(丙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
②乙容器在200min达到平衡状态,则0~200min内用NO的浓度变化表示的平均反应速率v(NO)=
(3)用焦炭还原NO2的反应为:2NO2(g)+2C(s)
 N2(g)+2CO2(g),在恒温条件下,1mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如下图所示:
N2(g)+2CO2(g),在恒温条件下,1mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如下图所示:
①A、B两点的浓度平衡常数关系:Kc(A)
②A、B、C三点中NO2的转化率最高的是
③计算C点时该反应的压强平衡常数Kp(C)=
(4)最新研究发现,用隔膜电解法可以处理高浓度乙醛废水。原理:使用惰性电极电解,乙醛分别在阴、阳极转化为乙醇和乙酸,总反应为:2CH3CHO+H2O
 CH3CH2OH+CH3COOH。实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的 处理过程,其装置示意图如下图所示:
CH3CH2OH+CH3COOH。实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的 处理过程,其装置示意图如下图所示:
①试写出电解过程中,阴极的电极反应式:
②在实际处理过程中,当电路中I=50A时,10min处理乙醛8.8g,则电流效率为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】汽车尾气中排放的氮氧化物严重影响着我们的环境,NOx等有毒气体的转化一直是科学研究的热点。
回答下列问题:
(1)已知:尿素CO(NH2)2(g)能与尾气中的NO(g)反应生成CO2(g)、N2(g)、H2O(g)排出。经测定,每生成28 g N2(g)放出321.7 kJ热量,则该反应的热化学方程式为_________________ 。
(2)某研究小组发现用NH3还原法也可以处理氮氧化物,发生反应4NH3(g)+6NO(g) 5N2(g)+6H2O(g) △H=-1806.4 kJ·mol-1。
5N2(g)+6H2O(g) △H=-1806.4 kJ·mol-1。
①下列事实能说明该反应达到平衡状态的是_______________ (填选项字母)。
a.4v正(NH3)=5v逆(N2)
b.NH3(g)与H2O(g)的物质的量之比保持不变
c.恒容密闭容器中气体的密度保持不变
d.各组分的物质的量分数保持不变
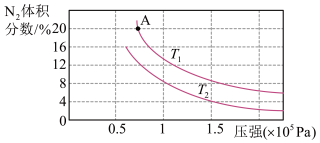
②向一密闭容器中充入2 mol NH3(g)和3 mol NO(g),发生上述反应,平衡混合物中N2的体积分数与压强、温度的关系如图所示(T代表温度),判断T1和T2的大小关系:T1______ T2(填“>”“<”或“=”),并说明理由:T1____________________________________ 。T1时,A点的坐标为(0.75,20),此时NO的转化率为__________ (保留三位有效数字)。
(3)科学研究表明,活性炭还原法也能处理氮氧化物,发生反应C(s)+2NO(g) N2(g)+CO2(g) △H>0。某探究小组向恒容密闭容器中加入足量的活性炭和1.0 mol NO(g),充分反应后达到化学平衡。
N2(g)+CO2(g) △H>0。某探究小组向恒容密闭容器中加入足量的活性炭和1.0 mol NO(g),充分反应后达到化学平衡。
①上述反应的平衡常数表达式为K=____________ 。
②其他条件不变,下列措施能同时提高化学反应速率和NO平衡转化率的是________ (填选项字母)。
a.通入氦气 b.加入催化剂 c.除去体系中的CO2 d.升高温度
(4)电化学法可对大气污染物NO2进行处理,某探究小组发现NO2、O2和熔融NaNO3可制作燃料电池,NO2被氧化成N2O5,写出负极的电极反应式:___________________________ 。
回答下列问题:
(1)已知:尿素CO(NH2)2(g)能与尾气中的NO(g)反应生成CO2(g)、N2(g)、H2O(g)排出。经测定,每生成28 g N2(g)放出321.7 kJ热量,则该反应的热化学方程式为
(2)某研究小组发现用NH3还原法也可以处理氮氧化物,发生反应4NH3(g)+6NO(g)
 5N2(g)+6H2O(g) △H=-1806.4 kJ·mol-1。
5N2(g)+6H2O(g) △H=-1806.4 kJ·mol-1。①下列事实能说明该反应达到平衡状态的是
a.4v正(NH3)=5v逆(N2)
b.NH3(g)与H2O(g)的物质的量之比保持不变
c.恒容密闭容器中气体的密度保持不变
d.各组分的物质的量分数保持不变
②向一密闭容器中充入2 mol NH3(g)和3 mol NO(g),发生上述反应,平衡混合物中N2的体积分数与压强、温度的关系如图所示(T代表温度),判断T1和T2的大小关系:T1

(3)科学研究表明,活性炭还原法也能处理氮氧化物,发生反应C(s)+2NO(g)
 N2(g)+CO2(g) △H>0。某探究小组向恒容密闭容器中加入足量的活性炭和1.0 mol NO(g),充分反应后达到化学平衡。
N2(g)+CO2(g) △H>0。某探究小组向恒容密闭容器中加入足量的活性炭和1.0 mol NO(g),充分反应后达到化学平衡。①上述反应的平衡常数表达式为K=
②其他条件不变,下列措施能同时提高化学反应速率和NO平衡转化率的是
a.通入氦气 b.加入催化剂 c.除去体系中的CO2 d.升高温度
(4)电化学法可对大气污染物NO2进行处理,某探究小组发现NO2、O2和熔融NaNO3可制作燃料电池,NO2被氧化成N2O5,写出负极的电极反应式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】利用含H2S的废气可回收硫,既可以保护环境又可资源化利用。回答下列问题:
(1)将H2S直接分解回收硫的同时得到氡能源的技术具有发展远景。起始时在反应器中充入一定量的H2S,在一定条件下发生反应2H2S(g) 2H2 (g)+S2(g),H2S热分解温度与平衡时气体组成如图所示:
2H2 (g)+S2(g),H2S热分解温度与平衡时气体组成如图所示:

①反应2H2S(g) 2H2(g)+S2(g)的△H=
2H2(g)+S2(g)的△H=___________ 0(填“>”或“<”)
②图中A点H2S的分解率为___________ (保留3位有效数字)
③若B点容器内气体总压为PPa,则此时反应的平衡常数Ka=___________ Pa(Kp为以分压表示的平衡常数,列出含P的代数式)。
(2)Fe3+溶液脱除H2S的原理如图所示:

①吸收塔中发生反应的化学方程式为___________ 。
②电解槽中再生FeCl3的原理是(结合方程式说明)___________ 。
③电解槽中的“交换膜”为___________ (填“阴离子”“阳离子”或“质子”)交换膜。
(3)H2S和空气按一定流速通入酸性FeCl3溶液,可实现空气脱硫得到单质硫。FeCl3溶液吸收H2S过程中,溶液中的n(Fe3+)、被吸收的n(H2S)随时间t的变化如图。

①t1以后,溶液中n(Fe3+)保持基本不变,原因是___________ 。
②t1以后的溶液中总反应方程式可以表示为___________ 。
(1)将H2S直接分解回收硫的同时得到氡能源的技术具有发展远景。起始时在反应器中充入一定量的H2S,在一定条件下发生反应2H2S(g)
 2H2 (g)+S2(g),H2S热分解温度与平衡时气体组成如图所示:
2H2 (g)+S2(g),H2S热分解温度与平衡时气体组成如图所示:
①反应2H2S(g)
 2H2(g)+S2(g)的△H=
2H2(g)+S2(g)的△H=②图中A点H2S的分解率为
③若B点容器内气体总压为PPa,则此时反应的平衡常数Ka=
(2)Fe3+溶液脱除H2S的原理如图所示:

①吸收塔中发生反应的化学方程式为
②电解槽中再生FeCl3的原理是(结合方程式说明)
③电解槽中的“交换膜”为
(3)H2S和空气按一定流速通入酸性FeCl3溶液,可实现空气脱硫得到单质硫。FeCl3溶液吸收H2S过程中,溶液中的n(Fe3+)、被吸收的n(H2S)随时间t的变化如图。

①t1以后,溶液中n(Fe3+)保持基本不变,原因是
②t1以后的溶液中总反应方程式可以表示为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】高炉炼铁是冶铁的主要方法,发生的主要反应为Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) ΔH=akJ·mol-1。
2Fe(s)+3CO2(g) ΔH=akJ·mol-1。
(1)已知:①Fe2O3(s)+3C(石墨,s)=2Fe(s)+3CO(g)ΔH1=+489.0kJ·mol-1
②C(石墨,s)+CO2(g)=2CO(g)ΔH2=+172.5kJ·mol-1
则a=__ 。
(2)冶炼铁的反应的平衡常数表达式为K=__ ,温度升高后,K值__ (填“增大”、“不变”或“减小”)。
(3)在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲和乙中,分别按表所示加入物质,反应经过一段时间后达到平衡。
①甲容器中CO的平衡转化率为__ 。
②下列说法正确的是__ (填字母)。
a.若容器内气体密度恒定,表示反应达到平衡状态
b.若容器内气体压强恒定时,标志反应达到平衡状态
c.甲、乙容器中,CO的平衡浓度之比为2∶3
d.增加Fe2O3的量可以提高CO的转化率
 2Fe(s)+3CO2(g) ΔH=akJ·mol-1。
2Fe(s)+3CO2(g) ΔH=akJ·mol-1。(1)已知:①Fe2O3(s)+3C(石墨,s)=2Fe(s)+3CO(g)ΔH1=+489.0kJ·mol-1
②C(石墨,s)+CO2(g)=2CO(g)ΔH2=+172.5kJ·mol-1
则a=
(2)冶炼铁的反应的平衡常数表达式为K=
(3)在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲和乙中,分别按表所示加入物质,反应经过一段时间后达到平衡。
| Fe2O3 | CO | Fe | CO2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 2.0 | 1.0 | 1.0 |
①甲容器中CO的平衡转化率为
②下列说法正确的是
a.若容器内气体密度恒定,表示反应达到平衡状态
b.若容器内气体压强恒定时,标志反应达到平衡状态
c.甲、乙容器中,CO的平衡浓度之比为2∶3
d.增加Fe2O3的量可以提高CO的转化率
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】甲醇是重要的化工原料,又是一种可再生能源,具有广泛的开发和应用前景。
(1)已知反应CO(g)+2H2(g) CH3OH(g)∆H=-99kJ.mol-1中的相关化学键键能如下:
CH3OH(g)∆H=-99kJ.mol-1中的相关化学键键能如下:
则x=__________________ 。
(2)在一容积可变的密闭容器中,1molCO与2molH2发生反应:CO(g)+2H2(g) CH3OH(g) ∆H1<0,CO在不同温度下的平衡转化率(α)与压强的关系如图所示。
CH3OH(g) ∆H1<0,CO在不同温度下的平衡转化率(α)与压强的关系如图所示。
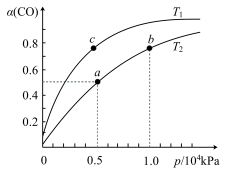
①a、b两点的反应速率:v(a)______ v(b)(填“>”、“<”、“=”)
②T1______ T2(填“>”、“<”、“=”),原因是_________________________ 。
③在c点条件下,下列叙述能说明上述反应能达到化学平衡状态的是________ (填代号)
a.H2的消耗速率是CH3OH生成速率的2倍
b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变
d.CO和CH3OH的物质的量之和保持不变
④计算图中a点的平衡常数KP=______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(1)已知反应CO(g)+2H2(g)
 CH3OH(g)∆H=-99kJ.mol-1中的相关化学键键能如下:
CH3OH(g)∆H=-99kJ.mol-1中的相关化学键键能如下:| 化学键 | H-H | C-O | C≡C | H-O | C-H |
| E/(kJ/mol) | 436 | 343 | x | 465 | 413 |
则x=
(2)在一容积可变的密闭容器中,1molCO与2molH2发生反应:CO(g)+2H2(g)
 CH3OH(g) ∆H1<0,CO在不同温度下的平衡转化率(α)与压强的关系如图所示。
CH3OH(g) ∆H1<0,CO在不同温度下的平衡转化率(α)与压强的关系如图所示。
①a、b两点的反应速率:v(a)
②T1
③在c点条件下,下列叙述能说明上述反应能达到化学平衡状态的是
a.H2的消耗速率是CH3OH生成速率的2倍
b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变
d.CO和CH3OH的物质的量之和保持不变
④计算图中a点的平衡常数KP=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】氢气是一种重要的工业原料和清洁能源,可用作合成氨、合成甲醇、合成盐酸的原料,冶金用还原剂等。
(1)工业合成氨的反应原理为N2(g)+3H2(g) 2NH3(g) ΔH=−92.4 kJ·mol−1。
2NH3(g) ΔH=−92.4 kJ·mol−1。
①该反应中的H2制取成本较高,工业生产中往往追求H2的转化率。增大H2的平衡转化率的措施有______________ (填字母代号)。
a.增大压强 b.升高温度 c.增大N2浓度
d.及时移走生成物NH3 e.使用高效催化剂
②某温度下,把10 mol N2与28 mol H2置于容积为10 L的恒容密闭容器内,10 min时反应达到平衡状态,测得平均速率v(NH3)=0.12 mol·L−1·min−1,H2的平衡转化率为______________ (保留三位有效数字),则该温度下反应的平衡常数K=_______________ 。
(2)为了减少CO对大气的污染,某研究性学习小组拟研究CO和H2O反应转化为绿色能源H2。已知:
2CO(g)+O2(g)═2CO2(g) △H=﹣566 kJ·mol-1
2H2(g)+O2(g)═2H2O(g) △H=﹣483.6 kJ·mol-1
H2O(g)═H2O(l) △H=﹣44.0 kJ·mol-1
①1 mol氢气生成液态水放出的热量为_________ kJ。
②写出CO和H2O(g)作用生成CO2和H2的热化学方程式_________ 。
(1)工业合成氨的反应原理为N2(g)+3H2(g)
 2NH3(g) ΔH=−92.4 kJ·mol−1。
2NH3(g) ΔH=−92.4 kJ·mol−1。①该反应中的H2制取成本较高,工业生产中往往追求H2的转化率。增大H2的平衡转化率的措施有
a.增大压强 b.升高温度 c.增大N2浓度
d.及时移走生成物NH3 e.使用高效催化剂
②某温度下,把10 mol N2与28 mol H2置于容积为10 L的恒容密闭容器内,10 min时反应达到平衡状态,测得平均速率v(NH3)=0.12 mol·L−1·min−1,H2的平衡转化率为
(2)为了减少CO对大气的污染,某研究性学习小组拟研究CO和H2O反应转化为绿色能源H2。已知:
2CO(g)+O2(g)═2CO2(g) △H=﹣566 kJ·mol-1
2H2(g)+O2(g)═2H2O(g) △H=﹣483.6 kJ·mol-1
H2O(g)═H2O(l) △H=﹣44.0 kJ·mol-1
①1 mol氢气生成液态水放出的热量为
②写出CO和H2O(g)作用生成CO2和H2的热化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某小组电解K2Cr2O7溶液,研究过程如下:
实验一
电压不同时,用石墨电极电解硫酸酸化的pH=2.5的饱和K2Cr2O7溶液,实验现象如下:
(1)阳极产生的气体是___________ 。
(2)电压为2.0V时,阴极区检出Cr3+,结合实验现象判断在阴极放电的主要离子是___________ 。
(3)电压高于5.0V时,被电解的主要物质是___________ 。
(4)实验二工业废水中常含有一定量的Cr2O 和CrO
和CrO ,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有还原沉淀法,该法的工艺流程为:
,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有还原沉淀法,该法的工艺流程为:
CrO
 Cr2O
Cr2O
 Cr3+
Cr3+ Cr(OH)3
Cr(OH)3
其中第①步存在平衡:2CrO (黄色)+2H+
(黄色)+2H+ Cr2O
Cr2O (橙色)+H2O
(橙色)+H2O
①若平衡体系的pH=2,则溶液显___________ 色。
②能说明第①步反应达平衡状态的是___________ 。
a、Cr2O 和CrO
和CrO 的浓度相同
的浓度相同
b、2v(Cr2O )=v(CrO
)=v(CrO )
)
c、溶液的颜色不变
③第②步中,还原1molCr2O 离子,需要
离子,需要___________ mol的FeSO4·7H2O。
④第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡: Cr(OH)3(s) Cr3+(aq)+3OH-(aq)常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至
Cr3+(aq)+3OH-(aq)常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至___________ 。
实验一
电压不同时,用石墨电极电解硫酸酸化的pH=2.5的饱和K2Cr2O7溶液,实验现象如下:
| 电压/V | 实验现象 |
| 2.0 | 阳极缓慢产生少量气泡,阴极没有气泡 |
| 3.0 | 阳极产生较多气泡,阴极产生少量气泡 |
| >5.0 | 两极均快速产生大量气泡,阴极产生气泡的速率约为阳极的2倍 |
(2)电压为2.0V时,阴极区检出Cr3+,结合实验现象判断在阴极放电的主要离子是
(3)电压高于5.0V时,被电解的主要物质是
(4)实验二工业废水中常含有一定量的Cr2O
 和CrO
和CrO ,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有还原沉淀法,该法的工艺流程为:
,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有还原沉淀法,该法的工艺流程为:CrO

 Cr2O
Cr2O
 Cr3+
Cr3+ Cr(OH)3
Cr(OH)3其中第①步存在平衡:2CrO
 (黄色)+2H+
(黄色)+2H+ Cr2O
Cr2O (橙色)+H2O
(橙色)+H2O①若平衡体系的pH=2,则溶液显
②能说明第①步反应达平衡状态的是
a、Cr2O
 和CrO
和CrO 的浓度相同
的浓度相同b、2v(Cr2O
 )=v(CrO
)=v(CrO )
)c、溶液的颜色不变
③第②步中,还原1molCr2O
 离子,需要
离子,需要④第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡: Cr(OH)3(s)
 Cr3+(aq)+3OH-(aq)常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至
Cr3+(aq)+3OH-(aq)常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】甲醇是重要的化工原料,用CO2和H2在催化剂的作用下合成甲醇,主要发生以下反应:
反应Ⅰ:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=-53.7kJ•mol-1
CH3OH(g)+H2O(g) △H1=-53.7kJ•mol-1
反应Ⅱ:CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41.2kJ•mol-1
CO(g)+H2O(g) △H2=+41.2kJ•mol-1
反应Ⅲ:CO(g)+2H2(g) CH3OH(g) △H3
CH3OH(g) △H3
 已知部分化学键的键能如表:
已知部分化学键的键能如表:
则△H3=____ kJ•mol-1,a=___ kJ•mol-1。
 在容积恒为2L的密闭容器中充入2molCH3OH(g)和2molCO(g),在一定温度下发生反应CH3OH(g)+CO(g)=HCOOCH3(g),测得容器内的压强随时间的变化如表所示。
在容积恒为2L的密闭容器中充入2molCH3OH(g)和2molCO(g),在一定温度下发生反应CH3OH(g)+CO(g)=HCOOCH3(g),测得容器内的压强随时间的变化如表所示。
①已知该条件下,该反应可自发进行,则其△H___ 0(填“<”、“>”或“=”),判断依据是___ 。
②在此条件下,0~4min的v(CH3OH)=___ kPa•min-1,该反应的平衡常数Kp=___ kPa-1(以分压表示,分压=总压×物质的量分数)。
(3)通过计算机对反应CH4(g)+H2O(g)=CO(g)+3H2(g)进行模拟实验,在0.1MPa时,不同温度下,不同水碳比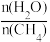 进行热力学计算,绘得反应平衡体系中H2的物质的量分数与水碳比、平衡温度的关系如图所示。水碳比和平衡温度对H2物质的量分数的影响,由图可知,温度一定时,H2的平衡物质的量分数与水碳比的关系是
进行热力学计算,绘得反应平衡体系中H2的物质的量分数与水碳比、平衡温度的关系如图所示。水碳比和平衡温度对H2物质的量分数的影响,由图可知,温度一定时,H2的平衡物质的量分数与水碳比的关系是__ ,可能的原因是___ 。

 电解法由甲醇和CO合成碳酸二甲酯的工作原理如图所示,则阳极的电极反应式为
电解法由甲醇和CO合成碳酸二甲酯的工作原理如图所示,则阳极的电极反应式为___ 。

反应Ⅰ:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1=-53.7kJ•mol-1
CH3OH(g)+H2O(g) △H1=-53.7kJ•mol-1反应Ⅱ:CO2(g)+H2(g)
 CO(g)+H2O(g) △H2=+41.2kJ•mol-1
CO(g)+H2O(g) △H2=+41.2kJ•mol-1反应Ⅲ:CO(g)+2H2(g)
 CH3OH(g) △H3
CH3OH(g) △H3 已知部分化学键的键能如表:
已知部分化学键的键能如表:| 化学键 | H—H | H—O | C=O | C≡O |
| 键能/kJ•mol-1 | 436 | 465 | a | 1076.8 |
 在容积恒为2L的密闭容器中充入2molCH3OH(g)和2molCO(g),在一定温度下发生反应CH3OH(g)+CO(g)=HCOOCH3(g),测得容器内的压强随时间的变化如表所示。
在容积恒为2L的密闭容器中充入2molCH3OH(g)和2molCO(g),在一定温度下发生反应CH3OH(g)+CO(g)=HCOOCH3(g),测得容器内的压强随时间的变化如表所示。| t/min | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| P/kPa | P0 | 0.8P0 | …… | …… | 0.7P0 | 0.7P0 | 0.7P0 |
②在此条件下,0~4min的v(CH3OH)=
(3)通过计算机对反应CH4(g)+H2O(g)=CO(g)+3H2(g)进行模拟实验,在0.1MPa时,不同温度下,不同水碳比
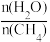 进行热力学计算,绘得反应平衡体系中H2的物质的量分数与水碳比、平衡温度的关系如图所示。水碳比和平衡温度对H2物质的量分数的影响,由图可知,温度一定时,H2的平衡物质的量分数与水碳比的关系是
进行热力学计算,绘得反应平衡体系中H2的物质的量分数与水碳比、平衡温度的关系如图所示。水碳比和平衡温度对H2物质的量分数的影响,由图可知,温度一定时,H2的平衡物质的量分数与水碳比的关系是
 电解法由甲醇和CO合成碳酸二甲酯的工作原理如图所示,则阳极的电极反应式为
电解法由甲醇和CO合成碳酸二甲酯的工作原理如图所示,则阳极的电极反应式为
您最近一年使用:0次
【推荐3】新型固体燃料电池的电解质是固体氧化锆和氧化钇,高温下允许氧离子( )在其间通过。如图所示,其中多孔电极不参与电极反应。
)在其间通过。如图所示,其中多孔电极不参与电极反应。
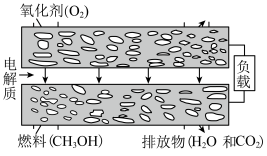
(1)①该电池的负极反应式为___________ 。
②若用上述甲醇燃料电池做电源,用惰性电极电解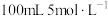 硫酸铜溶液,当阳极收集3.36L(标准状况)气体时,消耗甲醇的质量为
硫酸铜溶液,当阳极收集3.36L(标准状况)气体时,消耗甲醇的质量为___________ g,此时可向电解后的溶液中加入___________ (填化学式)使溶液复原。请写出电解硫酸铜溶液的离子方程式:___________ 。
(2)在微电子工业中, 常用作氮化硅的蚀刻剂,工业上通过电解含
常用作氮化硅的蚀刻剂,工业上通过电解含 等的无水熔融物生产
等的无水熔融物生产 ,其电解原理如图所示。
,其电解原理如图所示。
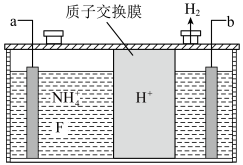
a电极为电解池的___________ (填“阴”或“阳”)极,写出该电极的电极反应式:___________ 。电解过程中还会生成少量氧化性极强的气体单质,该气体的分子式是___________ 。
 )在其间通过。如图所示,其中多孔电极不参与电极反应。
)在其间通过。如图所示,其中多孔电极不参与电极反应。
(1)①该电池的负极反应式为
②若用上述甲醇燃料电池做电源,用惰性电极电解
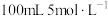 硫酸铜溶液,当阳极收集3.36L(标准状况)气体时,消耗甲醇的质量为
硫酸铜溶液,当阳极收集3.36L(标准状况)气体时,消耗甲醇的质量为(2)在微电子工业中,
 常用作氮化硅的蚀刻剂,工业上通过电解含
常用作氮化硅的蚀刻剂,工业上通过电解含 等的无水熔融物生产
等的无水熔融物生产 ,其电解原理如图所示。
,其电解原理如图所示。
a电极为电解池的
您最近一年使用:0次



