(1)147 g H2SO4的物质的量是________ ;0.5 mol H2SO4的质量是________ g;
(2)氧化铜在高温下发生分解反应:4CuO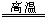 2Cu2O+O2↑,若反应过程中生成1molO2分子,则转移电子数为
2Cu2O+O2↑,若反应过程中生成1molO2分子,则转移电子数为____________ mol。
(3)反应:2FeCl3+2KI=2FeCl2+2KCl+I2,其中_____ 元素化合价升高,则该元素被_______ ,_____ 元素化合价降低;__________ 做还原剂,_______ 发生还原反应。
(4)钠在空气中燃烧的化学方程式:________________________________ ,1mol钠完全燃烧转移电子的个数为____________ 。
(2)氧化铜在高温下发生分解反应:4CuO
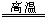 2Cu2O+O2↑,若反应过程中生成1molO2分子,则转移电子数为
2Cu2O+O2↑,若反应过程中生成1molO2分子,则转移电子数为(3)反应:2FeCl3+2KI=2FeCl2+2KCl+I2,其中
(4)钠在空气中燃烧的化学方程式:
更新时间:2018-12-28 08:10:23
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)标准状况下,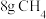 与
与___________ L的 气体含有相同的氢原子数。
气体含有相同的氢原子数。
(2)某气体氧化物的化学式为 ,在标准状况下,
,在标准状况下, 该氧化物的体积为
该氧化物的体积为 ,则该氧化物的摩尔质量为
,则该氧化物的摩尔质量为___________ 。
(3)在一定的温度和压强下,1体积气体 与3体积气体
与3体积气体 化合生成2体积气体化合物,则该化合物的化学式是
化合生成2体积气体化合物,则该化合物的化学式是___________ (用X、Y表示)。
(4)在150℃加热高氯酸铵发生分解反应;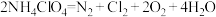 ,在150℃时其气态生成物组成的混合气的平均相对分子质量为
,在150℃时其气态生成物组成的混合气的平均相对分子质量为___________ (保留1位小数)。
(5)配制250mL0.1mol/L的 溶液,需5mol/LHAc溶液的体积为
溶液,需5mol/LHAc溶液的体积为___________ mL。
(6)下列关于 容量瓶的操作,正确的是___________。
容量瓶的操作,正确的是___________。
(7)古代青铜器的修复主旨是“修旧如旧”。
①铜锈为 ,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值,推测参与形成铜绿的物质有Cu和
,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值,推测参与形成铜绿的物质有Cu和___________ 。
②铜锈的成分非常复杂,主要成分有 和
和 ,考古学家将铜锈分为无害锈和有害锈,结构如图所示:
,考古学家将铜锈分为无害锈和有害锈,结构如图所示:

 属于
属于___________ (填“无害”或“有害”)锈,请解释原因:___________ 。
(1)标准状况下,
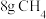 与
与 气体含有相同的氢原子数。
气体含有相同的氢原子数。(2)某气体氧化物的化学式为
 ,在标准状况下,
,在标准状况下, 该氧化物的体积为
该氧化物的体积为 ,则该氧化物的摩尔质量为
,则该氧化物的摩尔质量为(3)在一定的温度和压强下,1体积气体
 与3体积气体
与3体积气体 化合生成2体积气体化合物,则该化合物的化学式是
化合生成2体积气体化合物,则该化合物的化学式是(4)在150℃加热高氯酸铵发生分解反应;
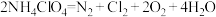 ,在150℃时其气态生成物组成的混合气的平均相对分子质量为
,在150℃时其气态生成物组成的混合气的平均相对分子质量为(5)配制250mL0.1mol/L的
 溶液,需5mol/LHAc溶液的体积为
溶液,需5mol/LHAc溶液的体积为(6)下列关于
 容量瓶的操作,正确的是___________。
容量瓶的操作,正确的是___________。A.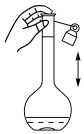 | B.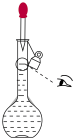 | C.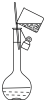 | D.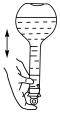 |
①铜锈为
 ,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值,推测参与形成铜绿的物质有Cu和
,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值,推测参与形成铜绿的物质有Cu和②铜锈的成分非常复杂,主要成分有
 和
和 ,考古学家将铜锈分为无害锈和有害锈,结构如图所示:
,考古学家将铜锈分为无害锈和有害锈,结构如图所示:
 属于
属于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)若将反应Fe+H2SO4=FeSO4+H2↑设计成原电池,可用铜作该电池装置的_______ (填“正”或“负”)极,该极上发生的电极反应为_______ 。
(2)如图为氢氧燃料电池的构造示意图,根据电子运动方向,可知氧气从_______ (填“a”或“b”)口通入,该电极的电极反应为_______ 。

(3)微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为:
Zn+2OH--2e-=ZnO+H2O
Ag2O+H2O+2e-=2Ag+2OH-
总反应为Ag2O+Zn=ZnO+2Ag
①Zn是_______ (填“正”或“负”)极,Ag2O发生_______ (填“氧化”或“还原”)反应。
②当电路通过1 mol电子时,负极消耗物质的质量是_______ g。
③在使用过程中,电解质溶液中KOH的物质的量_______ (填“增大”“减小”或“不变”)。
(1)若将反应Fe+H2SO4=FeSO4+H2↑设计成原电池,可用铜作该电池装置的
(2)如图为氢氧燃料电池的构造示意图,根据电子运动方向,可知氧气从

(3)微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为:
Zn+2OH--2e-=ZnO+H2O
Ag2O+H2O+2e-=2Ag+2OH-
总反应为Ag2O+Zn=ZnO+2Ag
①Zn是
②当电路通过1 mol电子时,负极消耗物质的质量是
③在使用过程中,电解质溶液中KOH的物质的量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】计算填空:
(1)______ mol CO2中含有氧原子数跟1.806×1024个H2O分子含有的氧原子数相同。
(2)3.01×1023个H2O所含电子的物质的量为________ mol。
(3)某同学将标准状况下44.8L的HCl气体溶于水,配成500mL的溶液,该HCl气体的物质的量为______ ,可知所配成的盐酸溶液的物质的量浓度为_____ 。
(4)标准状况下的甲烷和一氧化碳的混合气体8.96 L,其质量为7.60 g,则混合气体中甲烷的体积为______ ;一氧化碳的质量为_________ 。
(5)气态化合物A的化学式可以表示为OxFy,已知同温同压下10mLA受热完全分解生成15mLO2和10mL F2,则A的化学式为_____ 。
(6)将5 mol·L-1的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO 的物质的量浓度是
的物质的量浓度是______ mol·L-1。
(1)
(2)3.01×1023个H2O所含电子的物质的量为
(3)某同学将标准状况下44.8L的HCl气体溶于水,配成500mL的溶液,该HCl气体的物质的量为
(4)标准状况下的甲烷和一氧化碳的混合气体8.96 L,其质量为7.60 g,则混合气体中甲烷的体积为
(5)气态化合物A的化学式可以表示为OxFy,已知同温同压下10mLA受热完全分解生成15mLO2和10mL F2,则A的化学式为
(6)将5 mol·L-1的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO
 的物质的量浓度是
的物质的量浓度是
您最近一年使用:0次
【推荐1】实验室制备硫化氢往往用稀硫酸或稀盐酸而不能用稀硝酸是因为会发生以下反应: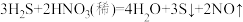
(1)在上述方程式上用单线桥标出电子转移的方向和数目。___________
(2)该反应中被还原的元素是___________ ,还原剂是___________ 。
(3)当有8个NO参加反应,上述反应转移的电子数目为___________ 个。
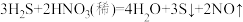
(1)在上述方程式上用单线桥标出电子转移的方向和数目。
(2)该反应中被还原的元素是
(3)当有8个NO参加反应,上述反应转移的电子数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】常见消毒剂有:①医用酒精;②“84”消毒液(主要成分是NaClO);③漂白粉;④二氧化氯;⑤O3;⑥高铁酸钠。
(1)上述物质中,消毒原理和其他不同的是___________ (填序号,下同)。
(2)上述物质中,其有效成分属于电解质的是___________ 。
(3)臭氧和氧气互为___________ (填“同位素”或“同素异形体”),它们在一定条件下可以相互转化,该变化过程属于___________ 。(填“氧化还原反应”或“非氧化还原反应”)。
(4)“84”消毒液和洁厕剂(主要成分是稀盐酸)混合使用会发生中毒事件,原因是___________ (用离子方程式表示)。
(5)配平下列方程式并用双线桥在方程式中标出电子转移的情况:___________ 。
 KClO3+
KClO3+ HCl(浓)=
HCl(浓)= KCl+
KCl+ ClO2↑+Cl2↑+H2O
ClO2↑+Cl2↑+H2O
(6)高铁酸钠(Na2FeO4)还是一种新型的净水剂。从其组成的阳离子来看,高铁酸钠属于___________ 盐,其中Fe的化合价是___________ 。其净水过程中所发生的化学反应主要为:4Na2FeO4+10H2O=4Fe(OH)3(胶体)+3O2↑+8NaOH,证明有Fe(OH)3胶体生成的实验操作:___________ 。
(1)上述物质中,消毒原理和其他不同的是
(2)上述物质中,其有效成分属于电解质的是
(3)臭氧和氧气互为
(4)“84”消毒液和洁厕剂(主要成分是稀盐酸)混合使用会发生中毒事件,原因是
(5)配平下列方程式并用双线桥在方程式中标出电子转移的情况:
 KClO3+
KClO3+ HCl(浓)=
HCl(浓)= KCl+
KCl+ ClO2↑+Cl2↑+H2O
ClO2↑+Cl2↑+H2O(6)高铁酸钠(Na2FeO4)还是一种新型的净水剂。从其组成的阳离子来看,高铁酸钠属于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)指出氧在下列各物质中的化合价,分别写出由氧气在一定条件下生成下列物质的化学方程式(必须注明反应条件)。
①Na2O:____________ ,_______________________________ 。
②Na2O2:___________ ,____________________________________ 。
(2)KO2能吸收CO2生成K2CO3和O2,故可用作特殊情况下的氧气源,试写出该反应的化学方程式___________________________________________________ 。
(3)人体内O 对健康有害,使人过早衰老,但在催化剂SOD存在下可以发生如下反应,请完成该反应的离子方程式:
对健康有害,使人过早衰老,但在催化剂SOD存在下可以发生如下反应,请完成该反应的离子方程式:
_____ O2-+_____ H2O=____ H2O2+O2+___ ______
①Na2O:
②Na2O2:
(2)KO2能吸收CO2生成K2CO3和O2,故可用作特殊情况下的氧气源,试写出该反应的化学方程式
(3)人体内O
 对健康有害,使人过早衰老,但在催化剂SOD存在下可以发生如下反应,请完成该反应的离子方程式:
对健康有害,使人过早衰老,但在催化剂SOD存在下可以发生如下反应,请完成该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】钠、铝和铁是中学化学常见的三种重要金属。请回答下列问题:
(1)钠在空气中燃烧生成_______ (填“Na2O”或“Na2O2”);
(2)Al2O3能溶于酸或强碱溶液生成盐和水,则Al2O3是一种_______ (填“酸性”“碱性”或“两性”)氧化物;
(3)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:_______ 。
(1)钠在空气中燃烧生成
(2)Al2O3能溶于酸或强碱溶液生成盐和水,则Al2O3是一种
(3)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:
您最近一年使用:0次
【推荐1】铁的化合物在实际中应用广泛,如氯化铁可用于五金蚀刻、污水处理及作催化剂、凝聚剂等,Na2FeO4 可用作净水剂等。
(1)氯化铁溶液用于五金蚀刻时的反应产物是氯化亚铁,再通入氯气,又可将其转化为氯化铁,则通入氯气后反应的离子方程式为_______ 。
(2)氯化铁还可以充当双氧水分解的催化剂, 1molH2O2发生分解时转移的电子数是_______ 。
(3)Na2FeO4是一种新型的净水消毒剂,可以通过下列反应制得: Fe (NO3) 3+NaOH+Cl2→Na2FeO4+NaNO3+ NaCl +H2O(未配平)。上述反应中氧化产物为_______ 。
(1)氯化铁溶液用于五金蚀刻时的反应产物是氯化亚铁,再通入氯气,又可将其转化为氯化铁,则通入氯气后反应的离子方程式为
(2)氯化铁还可以充当双氧水分解的催化剂, 1molH2O2发生分解时转移的电子数是
(3)Na2FeO4是一种新型的净水消毒剂,可以通过下列反应制得: Fe (NO3) 3+NaOH+Cl2→Na2FeO4+NaNO3+ NaCl +H2O(未配平)。上述反应中氧化产物为
您最近一年使用:0次
【推荐2】高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO3、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钾的主要反应为:2FeSO4+6Na2O2 2Na2FeO4+2Na2O+2Na2SO4+O2↑
2Na2FeO4+2Na2O+2Na2SO4+O2↑
①该反应的还原剂是___ ,每生成1 mol Na2FeO4,氧化剂得到____ mol电子。
②简要说明K2FeO4作为水处理剂时所起的作用:____________ 。
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式:____________ 。
②低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),说明_________ 。
(1)干法制备高铁酸钾的主要反应为:2FeSO4+6Na2O2
 2Na2FeO4+2Na2O+2Na2SO4+O2↑
2Na2FeO4+2Na2O+2Na2SO4+O2↑①该反应的还原剂是
②简要说明K2FeO4作为水处理剂时所起的作用:
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式:
②低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),说明
您最近一年使用:0次
【推荐3】Ca(ClO)2与浓盐酸反应会生成Cl2,该反应的化学方程式为:Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O
(1)氧化剂是___________ ;被还原的元素是___________ ;氧化产物是___________ ;还原剂与氧化剂的物质的量之比为___________ ;被氧化的HCl与参加反应的HCl物质的量之比是___________ 。
(2)若在标准状况下产生6.72LCl2,则转移的电子的数目为_________ 。
(3)用双线桥法表示该氧化还原反应中电子转移的方向和数目_______ 。
(1)氧化剂是
(2)若在标准状况下产生6.72LCl2,则转移的电子的数目为
(3)用双线桥法表示该氧化还原反应中电子转移的方向和数目
您最近一年使用:0次

 B
B C
C

