某课外活动小组探究镁与CO2、NO2的反应。
(1)实验发现点燃的镁条能在CO2气体中继续燃烧,产生黑、白两种固体,请用化学反应解释该现象_____________ 。
(2)该小组采用类比Mg与CO2反应的思路对Mg与NO2的反应进行预测:写出Mg与NO2反应的化学方程式_____________ 。
(3)设计实验验证猜测(用于连接玻璃管的乳胶管均内衬锡纸)
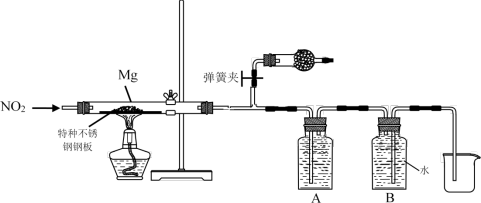
资料信息:2NO2 + 2NaOH = NaNO3 + NaNO2 + H2O
①装置A中的试剂是_____________ 。
②干燥管和装置B的作用分别是_____________ 、_____________ 。
③实验开始时正确的操作步骤是_____________ 。
a.通入NO2 b.打开弹簧夹
c.点燃酒精灯 d.当硬质玻璃管充满红综色气体后,关闭弹簧夹
(4)实验结束时,同学们观察到与预测相符合的现象,但当用水洗涤硬质玻璃管时,固体遇水产生有刺激性气味的气体,该气体能使湿润的石蕊试纸变蓝。
①同学们认为硬质玻璃管中还发生了另一个反应,该反应为_____________ ,
②请用化学方程式解释加水产生该气体的原因_____________ 。
(1)实验发现点燃的镁条能在CO2气体中继续燃烧,产生黑、白两种固体,请用化学反应解释该现象
(2)该小组采用类比Mg与CO2反应的思路对Mg与NO2的反应进行预测:写出Mg与NO2反应的化学方程式
(3)设计实验验证猜测(用于连接玻璃管的乳胶管均内衬锡纸)

资料信息:2NO2 + 2NaOH = NaNO3 + NaNO2 + H2O
①装置A中的试剂是
②干燥管和装置B的作用分别是
③实验开始时正确的操作步骤是
a.通入NO2 b.打开弹簧夹
c.点燃酒精灯 d.当硬质玻璃管充满红综色气体后,关闭弹簧夹
(4)实验结束时,同学们观察到与预测相符合的现象,但当用水洗涤硬质玻璃管时,固体遇水产生有刺激性气味的气体,该气体能使湿润的石蕊试纸变蓝。
①同学们认为硬质玻璃管中还发生了另一个反应,该反应为
②请用化学方程式解释加水产生该气体的原因
18-19高三上·湖北黄冈·阶段练习 查看更多[3]
湖北省黄冈市罗田县第一中学2019届高三上学期12月月考理科综合化学试题鲁科版(2019)高一必修第一册第三章C 高考挑战区 过模拟 2年模拟精编精练(已下线)专题07 铝、镁及其化合物(限时精练)-2022年高三毕业班化学常考点归纳与变式演练
更新时间:2019-01-04 23:01:14
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z三种物质有如下转化关系:

(1)根据上述转化关系,写出下列物质的
化学式:X_____ 、Y_____ 、Z___
试剂甲_____ ,试剂乙________
(2)写出上述③④⑤步反应的离子方程式:_____________ ;___________ ;___________

(1)根据上述转化关系,写出下列物质的
化学式:X
试剂甲
(2)写出上述③④⑤步反应的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】高纯 可以用于医药中间体、解酸剂、无机阻燃剂等;
可以用于医药中间体、解酸剂、无机阻燃剂等; 可用作补血剂。用硼泥(主要成分为
可用作补血剂。用硼泥(主要成分为 、
、 、
、 ,还含少量
,还含少量 、
、 、
、 和有机物)制备
和有机物)制备 和
和 的工艺流程如下:
的工艺流程如下:

已知:①该工业流程的条件下,部分金属离子开始沉淀和沉淀完全时的 如下表:
如下表:
②聚乙烯醇能吸附 和
和 并在聚乙烯醇表面生成颗粒大小一致的
并在聚乙烯醇表面生成颗粒大小一致的 。
。
请回答下列问题:
(1)“煅烧”的主要目的为__________ 。
(2)“滤渣1”的主要成分为不溶于酸的 和
和__________ ,两次“酸浸”时硫酸的用量都不宜过多,原因是__________ 。
(3)“氧化”时发生反应的离子方程式为__________ 。实际生产中 的用量比理论用量高的原因可能为
的用量比理论用量高的原因可能为__________ 。
(4)“调 ”时需控制溶液的
”时需控制溶液的 范围为
范围为__________ 。
(5)请简述 作无机阻燃剂的原理
作无机阻燃剂的原理__________ (答2点即可)。
(6)“沉镁”时要先加入聚乙烯醇溶液,后加入 溶液,若试剂加入顺序颠倒,导致的后果为
溶液,若试剂加入顺序颠倒,导致的后果为__________ 。
 可以用于医药中间体、解酸剂、无机阻燃剂等;
可以用于医药中间体、解酸剂、无机阻燃剂等; 可用作补血剂。用硼泥(主要成分为
可用作补血剂。用硼泥(主要成分为 、
、 、
、 ,还含少量
,还含少量 、
、 、
、 和有机物)制备
和有机物)制备 和
和 的工艺流程如下:
的工艺流程如下:
已知:①该工业流程的条件下,部分金属离子开始沉淀和沉淀完全时的
 如下表:
如下表: |  |  |  | |
| 开始沉淀 | 9.3 | 6.9 | 3.9 | 2.2 |
| 沉淀完全 | 10.8 | 8.4 | 4.7 | 3.2 |
②聚乙烯醇能吸附
 和
和 并在聚乙烯醇表面生成颗粒大小一致的
并在聚乙烯醇表面生成颗粒大小一致的 。
。请回答下列问题:
(1)“煅烧”的主要目的为
(2)“滤渣1”的主要成分为不溶于酸的
 和
和(3)“氧化”时发生反应的离子方程式为
 的用量比理论用量高的原因可能为
的用量比理论用量高的原因可能为(4)“调
 ”时需控制溶液的
”时需控制溶液的 范围为
范围为(5)请简述
 作无机阻燃剂的原理
作无机阻燃剂的原理(6)“沉镁”时要先加入聚乙烯醇溶液,后加入
 溶液,若试剂加入顺序颠倒,导致的后果为
溶液,若试剂加入顺序颠倒,导致的后果为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】实验室以一种工业废渣(主要成分为MgCO3、MgSO4,含有少量Fe、Al的氧化物)为原料制备MgCO3·3H2O。实验过程如下:
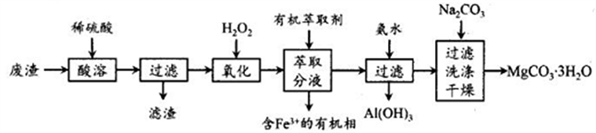
(1)为加快酸溶速率,可采取的办法有______ ,写出酸溶时废渣中主要成分发生反应的化学方程式为_________________ 。
(2)加入H2O2氧化时发生发应的离子方程式为_________________ 。
(3)用萃取分液的方法除去溶液中的Fe3+。
①检验溶液中是否含有Fe3+的最佳试剂是_________________ 。
②为使Fe3+ 尽可能多地从水相转移至有机相,采取的操作:向水溶液中加入一定量的萃取剂,_______ 、静置、分液,并重复多次。
③萃取时,向混合溶液(含Fe2+、Al3+、Mg2+)中加入适量盐酸,使Fe2+ 与Cl-生成[FeCl4]-,再用足量的乙醚(Et2O)进行萃取,乙醚与H+结合,生成了离子Et2O·H+,由于[FeCl4]-与Et2O·H+离子容易形成缔合物Et2O·H+·[FeCl4]-。该缔合物中,Cl-和Et2O分别取代了Fe2+和H+的配位水分子,并且中和了电荷,具有疏水性,能够溶于乙醚中。因此,就从水相转移到有机相中。该萃取剂不能萃取Al3+、Mg2+的原因是_________ 。
(4)已知:Ksp[Al(OH)3]=1.0×10-33,Ksp[(Mg(OH)2)=1.0×10-12.pH=8.5时Mg(OH)2开始沉淀。室温下,除去MgSO4溶液中的Al3+(使其浓度小于1×10-6mol·L-1),需加入氨水调节溶液pH的范围为____________ 。
(5)向滤液中加入Na2CO3溶液生成MgCO3 沉淀并用蒸馏水洗涤,检验沉淀是否洗净的操作是________________ 。
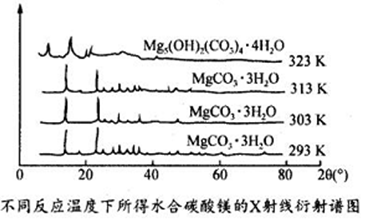
(6)干燥时需低温干燥,温度较高时发生副反应,写出MgCO3·3H2O在323K温度时发生转化的化学方程式________________ 。

(1)为加快酸溶速率,可采取的办法有
(2)加入H2O2氧化时发生发应的离子方程式为
(3)用萃取分液的方法除去溶液中的Fe3+。
①检验溶液中是否含有Fe3+的最佳试剂是
②为使Fe3+ 尽可能多地从水相转移至有机相,采取的操作:向水溶液中加入一定量的萃取剂,
③萃取时,向混合溶液(含Fe2+、Al3+、Mg2+)中加入适量盐酸,使Fe2+ 与Cl-生成[FeCl4]-,再用足量的乙醚(Et2O)进行萃取,乙醚与H+结合,生成了离子Et2O·H+,由于[FeCl4]-与Et2O·H+离子容易形成缔合物Et2O·H+·[FeCl4]-。该缔合物中,Cl-和Et2O分别取代了Fe2+和H+的配位水分子,并且中和了电荷,具有疏水性,能够溶于乙醚中。因此,就从水相转移到有机相中。该萃取剂不能萃取Al3+、Mg2+的原因是
(4)已知:Ksp[Al(OH)3]=1.0×10-33,Ksp[(Mg(OH)2)=1.0×10-12.pH=8.5时Mg(OH)2开始沉淀。室温下,除去MgSO4溶液中的Al3+(使其浓度小于1×10-6mol·L-1),需加入氨水调节溶液pH的范围为
(5)向滤液中加入Na2CO3溶液生成MgCO3 沉淀并用蒸馏水洗涤,检验沉淀是否洗净的操作是
(6)干燥时需低温干燥,温度较高时发生副反应,写出MgCO3·3H2O在323K温度时发生转化的化学方程式

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知甲、乙、丙分别代表中学化学中的常见物质,请根据题目要求回答下列问题:
(1)甲的化学式为RCl3,其溶液在加热蒸干并灼烧时可发生反应:
A 甲+H2O 乙+丙
乙+丙
B 乙 氧化物+H2O
氧化物+H2O
①若甲为某用途广泛的金属元素的氯化物,其溶液在上述变化中生成的氧化物为红棕色粉末,则该金属在周期表里的位置是_____________ 。
②若甲为某短周期金属元素的氯化物,则甲发生a反应的化学方程式为__________ 。
③将以上两种金属单质用导线连接,插入NaOH溶液构成原电池,则负极发生的电极反应为___________________________ 。
(2)若甲,乙、丙均是短周期中同一周期元素形成的单质或化合物,常温下乙为固体单质,甲和丙均为气态化合物,且可发生反应:甲+乙 丙。则:
丙。则:
①甲的结构式为_____________ 。
②写出在200mL 2mol/L的NaOH溶液中通入6.72L(标准状况)的气体甲发生完全反应的总离子方程式________________________ 。
(1)甲的化学式为RCl3,其溶液在加热蒸干并灼烧时可发生反应:
A 甲+H2O
 乙+丙
乙+丙B 乙
 氧化物+H2O
氧化物+H2O①若甲为某用途广泛的金属元素的氯化物,其溶液在上述变化中生成的氧化物为红棕色粉末,则该金属在周期表里的位置是
②若甲为某短周期金属元素的氯化物,则甲发生a反应的化学方程式为
③将以上两种金属单质用导线连接,插入NaOH溶液构成原电池,则负极发生的电极反应为
(2)若甲,乙、丙均是短周期中同一周期元素形成的单质或化合物,常温下乙为固体单质,甲和丙均为气态化合物,且可发生反应:甲+乙
 丙。则:
丙。则:①甲的结构式为
②写出在200mL 2mol/L的NaOH溶液中通入6.72L(标准状况)的气体甲发生完全反应的总离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】兴趣小组在课外实验中意外发现:将镁条放入 溶液中,快速产生较多气泡,有白色沉淀生成,小组同学对此进行了系列探究活动。
溶液中,快速产生较多气泡,有白色沉淀生成,小组同学对此进行了系列探究活动。
探究1:反应产生的气体是什么?
【作出猜想】
(1)小组同学经查阅资料和讨论,根据化学变化过程中元素不变,且反应物中含有___________ 三种元素,作出如下猜想:
①氢气;②二氧化碳;③氢气和二氧化碳。
【实验1】取适量镁条、 溶液于反应装置A中,按如图1所示方案进行实验,B中石灰水不变浑浊;C处气体燃烧,烧杯内壁有水珠。说明猜想①正确。
溶液于反应装置A中,按如图1所示方案进行实验,B中石灰水不变浑浊;C处气体燃烧,烧杯内壁有水珠。说明猜想①正确。
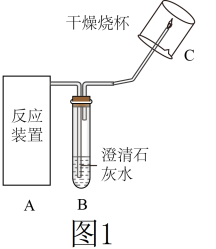
(2)反应装置A应选用图2中的___________ 装置(填写序号)。

(3)小组同学讨论认为,上述实验中“烧杯内壁有水珠”作为“反应产生的气体是氢气”的证据不可靠。为使这一证据可靠,且仍能一次性地验证三个猜想,只需在图1所示方案的基础上加以改进完善。你的改进方案是___________
探究II:快速产生气体的原因是什么?
【查阅资科】镁与水缓慢反应生成氢气: 溶液显碱性,其溶液中除
溶液显碱性,其溶液中除 、
、 外,还有
外,还有 。
。
【作出猜想】可能是 溶液中的某一种离子促进了镁与水的反应。
溶液中的某一种离子促进了镁与水的反应。
【实验2】按图3所示方案进行实验。G、I中缓慢产生气泡,H中快速产生较多气泡,说明是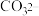 而不是
而不是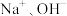 促进了镁与水的反应。
促进了镁与水的反应。
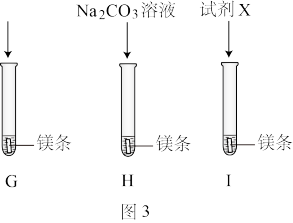
(4)G中实验的作用是___________ 。
(5)试剂X是___________ 溶液。
探究Ⅲ:反应产生的白色沉淀中是否含有 ?
?
【实验3】取实验1反应生成的沉淀于试管中,加入试剂Y,根据实验现象说明白色沉淀中含有 。
。
(6)试剂Y为___________ ,实验操作及现象为___________ ,写出 与试剂Y反应的化学方程式
与试剂Y反应的化学方程式___________ 。
反思交流与结论: 与
与 溶液反应产生氢气,白色沉淀中可能含有
溶液反应产生氢气,白色沉淀中可能含有 ,
, 溶液中
溶液中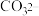 促进了镁与水的反应。
促进了镁与水的反应。
 溶液中,快速产生较多气泡,有白色沉淀生成,小组同学对此进行了系列探究活动。
溶液中,快速产生较多气泡,有白色沉淀生成,小组同学对此进行了系列探究活动。探究1:反应产生的气体是什么?
【作出猜想】
(1)小组同学经查阅资料和讨论,根据化学变化过程中元素不变,且反应物中含有
①氢气;②二氧化碳;③氢气和二氧化碳。
【实验1】取适量镁条、
 溶液于反应装置A中,按如图1所示方案进行实验,B中石灰水不变浑浊;C处气体燃烧,烧杯内壁有水珠。说明猜想①正确。
溶液于反应装置A中,按如图1所示方案进行实验,B中石灰水不变浑浊;C处气体燃烧,烧杯内壁有水珠。说明猜想①正确。
(2)反应装置A应选用图2中的

(3)小组同学讨论认为,上述实验中“烧杯内壁有水珠”作为“反应产生的气体是氢气”的证据不可靠。为使这一证据可靠,且仍能一次性地验证三个猜想,只需在图1所示方案的基础上加以改进完善。你的改进方案是
探究II:快速产生气体的原因是什么?
【查阅资科】镁与水缓慢反应生成氢气:
 溶液显碱性,其溶液中除
溶液显碱性,其溶液中除 、
、 外,还有
外,还有 。
。【作出猜想】可能是
 溶液中的某一种离子促进了镁与水的反应。
溶液中的某一种离子促进了镁与水的反应。【实验2】按图3所示方案进行实验。G、I中缓慢产生气泡,H中快速产生较多气泡,说明是
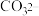 而不是
而不是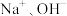 促进了镁与水的反应。
促进了镁与水的反应。
(4)G中实验的作用是
(5)试剂X是
探究Ⅲ:反应产生的白色沉淀中是否含有
 ?
?【实验3】取实验1反应生成的沉淀于试管中,加入试剂Y,根据实验现象说明白色沉淀中含有
 。
。(6)试剂Y为
 与试剂Y反应的化学方程式
与试剂Y反应的化学方程式反思交流与结论:
 与
与 溶液反应产生氢气,白色沉淀中可能含有
溶液反应产生氢气,白色沉淀中可能含有 ,
, 溶液中
溶液中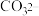 促进了镁与水的反应。
促进了镁与水的反应。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】氮化锶(Sr3N2)在工业上广泛用于生产荧光粉。已知:锶与镁位于同主族;锶与氮气在加热条件下可生成氮化锶,氮化锶遇水剧烈反应。
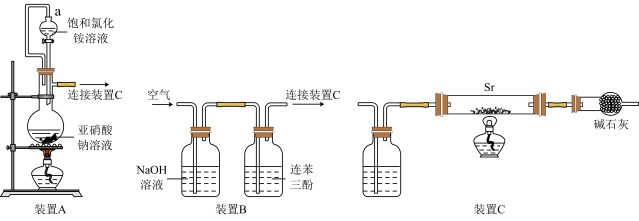
I.利用装置A和C制备Sr3N2
(1)写出由装置A制备N2的化学方程式_______ 。
(2)装置A中a导管的作用是_______ 。利用该套装置时,应先点燃装置A的酒精灯一段时间后,再点燃装置C的酒精灯,理由是__________ 。
II.利用装置B和C制备Sr3N2。利用装置B从空气中提纯N2(已知:氧气可被连苯三酚溶液定量吸收)
(3)写出装置B的NaOH溶液中发生反应的离子方程式_________ 。
(4)装置C中广口瓶盛放的试剂是_________ 。
III.测定Sr3N2产品的纯度
(5)取ag该产品,向其中加入适量的水,将生成的气体全部通入浓硫酸中,利用浓硫酸增重质量计算得到产品的纯度,该方法测得产品的纯度偏高,其原因是____ 。经改进后测得浓硫酸增重bg,则产品的纯度为_____ (用相关字母的代数式表示)。

I.利用装置A和C制备Sr3N2
(1)写出由装置A制备N2的化学方程式
(2)装置A中a导管的作用是
II.利用装置B和C制备Sr3N2。利用装置B从空气中提纯N2(已知:氧气可被连苯三酚溶液定量吸收)
(3)写出装置B的NaOH溶液中发生反应的离子方程式
(4)装置C中广口瓶盛放的试剂是
III.测定Sr3N2产品的纯度
(5)取ag该产品,向其中加入适量的水,将生成的气体全部通入浓硫酸中,利用浓硫酸增重质量计算得到产品的纯度,该方法测得产品的纯度偏高,其原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】氯元素可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备 和NaClO,并探究NaClO的性质。
和NaClO,并探究NaClO的性质。

回答下列问题:
(1)写出A中发生反应的化学方程式_______ 。
(2)B的作用是_______ 。
(3)写出C中反应的离子方程式_______ 。
(4)探究NaClO的性质:

①Ⅰ中液褪色的原因是_______ 。
②Ⅲ中产生黄绿色气体的原因是_______ (写离子方程式)。
③通过上述探究实验可知,影响氧化还原反应的因素是_______ 。
 和NaClO,并探究NaClO的性质。
和NaClO,并探究NaClO的性质。
回答下列问题:
(1)写出A中发生反应的化学方程式
(2)B的作用是
(3)写出C中反应的离子方程式
(4)探究NaClO的性质:

①Ⅰ中液褪色的原因是
②Ⅲ中产生黄绿色气体的原因是
③通过上述探究实验可知,影响氧化还原反应的因素是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某课外活动小组为了探究钠与 溶液的反应,设计如图装置(夹持装置省略)。首先在U形管内加入少量煤油和几粒金属钠,再从U形管左端加入
溶液的反应,设计如图装置(夹持装置省略)。首先在U形管内加入少量煤油和几粒金属钠,再从U形管左端加入 溶液,一段时间后加热铜丝。回答下列问题:
溶液,一段时间后加热铜丝。回答下列问题:
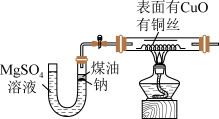
(1)从试剂瓶取出后剩余的 能否放回原试剂瓶?
能否放回原试剂瓶?_______ (填“能”或“否”)。
(2)U形管中出现的现象是_______;
(3)写出钠与 溶液反应的化学方程式:
溶液反应的化学方程式:_______ ;
(4)铜丝的变化现象是_______ ,写出化学反应方程式_______ 。
 溶液的反应,设计如图装置(夹持装置省略)。首先在U形管内加入少量煤油和几粒金属钠,再从U形管左端加入
溶液的反应,设计如图装置(夹持装置省略)。首先在U形管内加入少量煤油和几粒金属钠,再从U形管左端加入 溶液,一段时间后加热铜丝。回答下列问题:
溶液,一段时间后加热铜丝。回答下列问题:
(1)从试剂瓶取出后剩余的
 能否放回原试剂瓶?
能否放回原试剂瓶?(2)U形管中出现的现象是_______;
| A.有气泡生成,钠熔化成小球 | B.钠在煤油面上四处游动 |
| C.溶液中有银白色金属生成 | D.溶液变浑浊 |
 溶液反应的化学方程式:
溶液反应的化学方程式:(4)铜丝的变化现象是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】炼锌厂的铜镉废渣中含有铜、锌、镉( )、铁、砷(
)、铁、砷( )等元素,其含量依次减少。对这些元素进行提取分离能减少环境污染,同时制得
)等元素,其含量依次减少。对这些元素进行提取分离能减少环境污染,同时制得 实现资源的利用,其流程图如图。已知
实现资源的利用,其流程图如图。已知 难溶于水;
难溶于水; 易溶于水,难溶于酒精。
易溶于水,难溶于酒精。
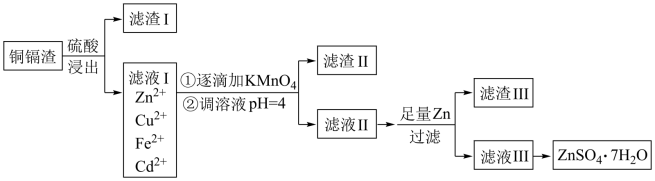
请回答下列问题:
(1)提高浸出率可以采用的方法是_______ (写出一点)。
(2)滤液Ⅰ中有少量的 ,若不除去,则
,若不除去,则 与
与 反应会产生一种有毒氢化物气体,该气体的分子式为
反应会产生一种有毒氢化物气体,该气体的分子式为_______ 。向滤液Ⅰ中逐滴滴入酸性 溶液可与
溶液可与 反应生成
反应生成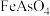 ,完成该反应的离子方程式:_______
,完成该反应的离子方程式:_______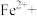 _______
_______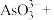 _______
_______ _______=_______
_______=_______ _______
_______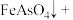 _______
_______
______
滴定终点的现象是_______ 。
(3)流程中②调节 时可选用的试剂为
时可选用的试剂为_______ ,滤渣Ⅱ的主要成分为_______ 。
(4)制得的 需洗涤,洗涤晶体时应选用试剂为
需洗涤,洗涤晶体时应选用试剂为_______ 。
 )、铁、砷(
)、铁、砷( )等元素,其含量依次减少。对这些元素进行提取分离能减少环境污染,同时制得
)等元素,其含量依次减少。对这些元素进行提取分离能减少环境污染,同时制得 实现资源的利用,其流程图如图。已知
实现资源的利用,其流程图如图。已知 难溶于水;
难溶于水; 易溶于水,难溶于酒精。
易溶于水,难溶于酒精。
| 金属离子 |  |  |  |  |  |
开始沉淀 | 2.7 | 6.5 | 7.7 | 5.2 | 6.9 |
沉淀完全 | 3.2 | 8.0 | 9.8 | 6.4 | 9.4 |
(1)提高浸出率可以采用的方法是
(2)滤液Ⅰ中有少量的
 ,若不除去,则
,若不除去,则 与
与 反应会产生一种有毒氢化物气体,该气体的分子式为
反应会产生一种有毒氢化物气体,该气体的分子式为 溶液可与
溶液可与 反应生成
反应生成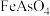 ,完成该反应的离子方程式:_______
,完成该反应的离子方程式:_______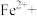 _______
_______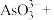 _______
_______ _______=_______
_______=_______ _______
_______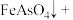 _______
_______滴定终点的现象是
(3)流程中②调节
 时可选用的试剂为
时可选用的试剂为(4)制得的
 需洗涤,洗涤晶体时应选用试剂为
需洗涤,洗涤晶体时应选用试剂为
您最近一年使用:0次



