N2+3H2 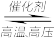 2NH3,是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是
2NH3,是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是
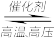 2NH3,是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是
2NH3,是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是| A.降低体系温度能加快反应速率 |
| B.使用恰当的催化剂能加快反应速率,又能提高N2的转化率 |
| C.达到反应限度时各组分含量之比一定等于3∶1∶2 |
| D.若在反应的密闭容器加入1mol N2和过量的H2,最后不能生成2mol NH3 |
更新时间:2019-02-26 11:21:42
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列有关化学反应速率的说法中,正确的是
| A.2mol/L盐酸与锌反应时,加入4mol/L的氯化钠溶液,生成氢气的速率加快 |
B.对于可逆反应2CO+2NO N2+2CO2,使用合适的催化剂,CO的生成速率和消耗速率都加快 N2+2CO2,使用合适的催化剂,CO的生成速率和消耗速率都加快 |
| C.工业上合成氨是放热反应,升高温度,正反应速率减慢 |
| D.在K2SO4和BaCl2两溶液反应时,增大压强,生成沉淀速率加快 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某实验小组用0.1
 溶液和0.1
溶液和0.1
 溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。下列说法错误的是
溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。下列说法错误的是
已知: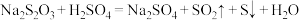

 溶液和0.1
溶液和0.1
 溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。下列说法错误的是
溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。下列说法错误的是已知:
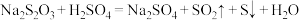
| 实验序号 | 温度 |  溶液 溶液 |  溶液 溶液 |  | 出现沉淀所需的时间 |
| I | 10℃ | 5 | 5 | 10 | 10s |
| Ⅱ | 10℃ | 5 | 10 | a | 8s |
| Ⅲ | 10℃ | 5 | 7 | 8 |  s s |
| Ⅳ | 30℃ | 5 | 5 | 10 | 3s |
A.实验Ⅱ中 |
B.实验Ⅲ中 |
| C.对比实验I、Ⅳ可得:浓度保持不变时,升高温度,化学反应速率增大 |
| D.对比实验I、Ⅱ、Ⅲ可得:温度相同时,增大反应物浓度,化学反应速率增大 |
您最近一年使用:0次
【推荐1】以下描述正确的是
| 选 项 | A | B | C | D |
| 装 置 图 |  |  |  | 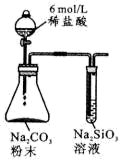 |
| 结 论 | 右边试管产生气泡 较快,说明催化活 性:Fe3+>Cu2+ | 左边棉球变棕黄色,右 边棉球变蓝色,说明氧 化性:Br2>I2 | 有气泡产生, 可用此装置制 备少量氧气 | 试管中液体变浑浊, 说明非金属性:C>Si |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下。下列说法错误的是


| A.总反应为放热反应 | B.第①步有C=O键断裂 |
| C.第②步有C-C键形成 | D.催化剂可有效提高化学反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】合成氨的热化学方程式为N2(g) +3H2(g) 2NH3(g) ∆H= -92.4 kJ/mol ,如图所示为相同温度下,在等量的不同催化剂作用下,某浓度氨气分解时对应生成氢气的初始速率,下列说法正确的是 ( )
2NH3(g) ∆H= -92.4 kJ/mol ,如图所示为相同温度下,在等量的不同催化剂作用下,某浓度氨气分解时对应生成氢气的初始速率,下列说法正确的是 ( )
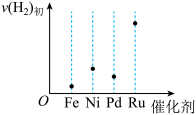
 2NH3(g) ∆H= -92.4 kJ/mol ,如图所示为相同温度下,在等量的不同催化剂作用下,某浓度氨气分解时对应生成氢气的初始速率,下列说法正确的是 ( )
2NH3(g) ∆H= -92.4 kJ/mol ,如图所示为相同温度下,在等量的不同催化剂作用下,某浓度氨气分解时对应生成氢气的初始速率,下列说法正确的是 ( )
| A.Fe作催化剂时,氨气分解反应活化能最小 |
| B.氨气分解达到平衡时,单位时间内N≡N键断裂数目和N —H键形成数目相同 |
| C.低压有利于提高N2和H2产率 |
| D.高温有利于提高工业合成氨产率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在工业生产硫酸的过程中,发生如下反应:2SO2(g)+O2(g) 2SO3(g)+Q,下列叙述中,不正确的是:
2SO3(g)+Q,下列叙述中,不正确的是:
 2SO3(g)+Q,下列叙述中,不正确的是:
2SO3(g)+Q,下列叙述中,不正确的是:| A.矿石粉碎的目的是使原料充分利用,并增大接触面使反应速率加快 |
| B.接触室中采用常压的主要原因是常压下SO2的转化率已经很高 |
| C.沸腾炉中出来的混合气需要洗涤,目的是防止催化剂中毒 |
| D.接触室采用450℃的温度是使催化剂活性最佳,提高平衡混和气中SO3的含量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法不正确 的是
| A.铅酸蓄电池属于二次电池,其充电过程是将电能转化为化学能 |
B.向密闭容器中充入64g 和48gO2,充分反应后生成的 和48gO2,充分反应后生成的 的分子数小于NA 的分子数小于NA |
| C.常温下可以用铁制或铝制容器盛装浓硫酸 |
D.粗盐中含有可溶性硫酸盐及 、 、 等杂质,可选用① 等杂质,可选用① 溶液、② 溶液、② 溶液、③ 溶液、③ 溶液、④稀盐酸去除。这些试剂在使用时的正确顺序可以是③①②④ 溶液、④稀盐酸去除。这些试剂在使用时的正确顺序可以是③①②④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】根据下列实验操作和现象得出的结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向0.1mol∙L-1的醋酸溶液中滴加等温、等浓度NaOH溶液至过量 | 溶液温度先升高后降低 | CH3COO-的水解反应为放热反应 |
| B | 室温下,用pH试纸分别测定NaF溶液和CH3COONa溶液的pH | pH:CH3COONa溶液>NaF溶液 | HF酸性强于CH3COOH |
| C | 取1mL1mol∙L-1KI溶液于试管中,加入5mL0.1mol∙L-1FeCl3溶液,将反应后的溶液分两份 | 一份滴KSCN溶液显红色,另一份滴淀粉溶液显蓝色 | KI与FeCl3的反应属于可逆反应 |
| D | 用铜电极电解稀硫酸 | 一个电极铜逐渐溶解,另一电极上产生无色气体 | H+的氧化性比Cu2+强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】设NA为阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,NA个分子所占的体积约为22.4L |
| B.18gH2O中含共用电子对数为2NA |
| C.1molHClO中含有H—Cl键数为NA |
| D.将标准状况下2.24LSO2通入水中完全溶解,溶液中H2SO3分子数为0.1NA |
您最近一年使用:0次




