KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表述为:2KClO3+4HCl(浓)===2KCl+2ClO2↑+Cl2↑+2H2O。
(1)请分析该反应中电子转移的情况(用双线桥法表示)___________________________ 。
(2)浓盐酸在反应中显示出来的性质是________
(3)若产生0.1 mol Cl2,则被氧化的HCl的物质的量为________ mol。
(1)请分析该反应中电子转移的情况(用双线桥法表示)
(2)浓盐酸在反应中显示出来的性质是
(3)若产生0.1 mol Cl2,则被氧化的HCl的物质的量为
更新时间:2019-02-19 10:44:38
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)下列反应中都有水参加:
A.Cl2+ H2O +Na2SO3=2HCl + Na2SO4
B.3NO2 + H2O = 2HNO3 + NO↑
C.NaH +H2O = NaOH + H2↑
D.2H2O电解2H2↑+ O2↑
其中,水只是氧化剂的是_________ ,水既不是氧化剂又不是还原剂的是_________ ;
(2)在3BrF3+5H2O=9HF+HBrO3+O2↑+Br2反应中,若有5.4gH2O被氧化,则被还原的BrF3共______________ mol,其中被水还原的BrF3是_______________ mol。
A.Cl2+ H2O +Na2SO3=2HCl + Na2SO4
B.3NO2 + H2O = 2HNO3 + NO↑
C.NaH +H2O = NaOH + H2↑
D.2H2O电解2H2↑+ O2↑
其中,水只是氧化剂的是
(2)在3BrF3+5H2O=9HF+HBrO3+O2↑+Br2反应中,若有5.4gH2O被氧化,则被还原的BrF3共
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图为铁及其化合物的“价-类”二维图。
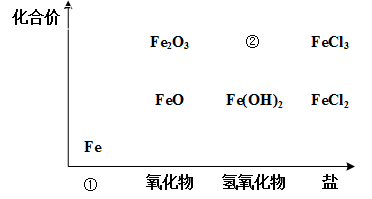
(1)填写二维图缺失的类别①___ 和化学式②___ 。
(2)某同学利用以下试剂研究FeCl3性质,进行了如下预测:
①Cl2②Fe ③NaOH ④H2SO4⑤AgNO3
从物质类别上看,FeCl3属于___ ,可能与___ 发生反应(填序号);
从化合价角度看,Fe3+具有___ 性,可能与___ 发生反应(填序号)。
(3)某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路,其化学原理为如下反应:Cu+2FeCl3=CuCl2+2FeCl2
①用单线桥表示电子转移。___ 。
②反应中FeCl3作___ 剂,理由是___ 。
③写出该反应的离子方程式___ 。

(1)填写二维图缺失的类别①
(2)某同学利用以下试剂研究FeCl3性质,进行了如下预测:
①Cl2②Fe ③NaOH ④H2SO4⑤AgNO3
从物质类别上看,FeCl3属于
从化合价角度看,Fe3+具有
(3)某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路,其化学原理为如下反应:Cu+2FeCl3=CuCl2+2FeCl2
①用单线桥表示电子转移。
②反应中FeCl3作
③写出该反应的离子方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如图所示是铁及其化合物的“价类”二维图。

(1)X、Y分别代表___________ 、___________ ;Z在空气中转化为W的化学方程式为___________ 。
(2)某小组研究 性质,预测
性质,预测 能与
能与___________ 发生氧化还原反应(填序号)。
①NaOH溶液 ②氯水 ③稀盐酸 ④酸性 溶液 ⑤
溶液 ⑤ 溶液 ⑥碳酸钠
溶液 ⑥碳酸钠
(3)铁盐溶液可用于金属刻蚀。如用 溶液刻蚀铜制电路板,
溶液刻蚀铜制电路板, 被
被___________ (填“还原”或“氧化”)为 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(4)为检验食品中的铁元素,可将菠菜剪碎、研磨、溶解、___________ ,然后取少许滤液于试管中进行实验。
(5)高铁酸钠是一种能杀菌、脱色、除臭的新型高效水处理剂。工业上可用NaClO氧化 的方法制备
的方法制备 ,其原理为
,其原理为 ,用
,用单线桥法 表示该反应的电子转移方向和数目。____________ 。

(1)X、Y分别代表
(2)某小组研究
 性质,预测
性质,预测 能与
能与①NaOH溶液 ②氯水 ③稀盐酸 ④酸性
 溶液 ⑤
溶液 ⑤ 溶液 ⑥碳酸钠
溶液 ⑥碳酸钠(3)铁盐溶液可用于金属刻蚀。如用
 溶液刻蚀铜制电路板,
溶液刻蚀铜制电路板, 被
被 ,该反应的离子方程式为
,该反应的离子方程式为(4)为检验食品中的铁元素,可将菠菜剪碎、研磨、溶解、
(5)高铁酸钠是一种能杀菌、脱色、除臭的新型高效水处理剂。工业上可用NaClO氧化
 的方法制备
的方法制备 ,其原理为
,其原理为 ,用
,用
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在反应2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O中,氧化剂是________ ,氧化产物是________ ,氧化产物与还原产物的物质的量之比为________ ,被氧化与未被氧化的HCl的质量之比为________ ,若有73 g HCl被氧化,电子转移的总数为________ (用NA表示阿伏加德罗),标准状况生成Cl2的体积为________ L。
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求回答下列问题:
(1)现有以下物质:①NaCl晶体 ②液态HCl ③CaCO3固体 ④熔融KCl ⑤蔗糖 ⑥铜 ⑦CO2 ⑧H2SO4 ⑨KOH固体
a. 以上物质中能导电的是________________________________ 。
b. 以上物质中属于电解质的是_______________________ ,属于非电解质的是_______________________ 。
c. 以上物质中,溶于水且能导电的物质是_______________________ 。
(2)胶体和溶液的本质区别是________________ ,鉴别胶体和溶液所采用的方法是观察是否能发生___________ 效应。
(3)下列3个反应,按要求填写相关量。
①2Na2O2+2H2O=4NaOH+ O2↑反应中,每消耗1 mol Na2O2生成_____ g O2。
②在NaHCO3的热分解反应中,每消耗168 g NaHCO3,标准状况下生成_____ L CO2。
③Cl2+H2O=HCl+HClO反应中,标准状况下每消耗22.4LCl2,转移_____ mol电子。
(4)在一个密闭容器中放入以下四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下:
①该变化的基本反应类型是_____ 反应;
②物质Q在反应中起的作用是_____ 。
(1)现有以下物质:①NaCl晶体 ②液态HCl ③CaCO3固体 ④熔融KCl ⑤蔗糖 ⑥铜 ⑦CO2 ⑧H2SO4 ⑨KOH固体
a. 以上物质中能导电的是
b. 以上物质中属于电解质的是
c. 以上物质中,溶于水且能导电的物质是
(2)胶体和溶液的本质区别是
(3)下列3个反应,按要求填写相关量。
①2Na2O2+2H2O=4NaOH+ O2↑反应中,每消耗1 mol Na2O2生成
②在NaHCO3的热分解反应中,每消耗168 g NaHCO3,标准状况下生成
③Cl2+H2O=HCl+HClO反应中,标准状况下每消耗22.4LCl2,转移
(4)在一个密闭容器中放入以下四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下:
| 物质 | M | N | Q | P |
| 反应前质量(g) | 50 | 1 | 3 | 12 |
| 反应后质量(g) | x | 26 | 3 | 30 |
②物质Q在反应中起的作用是
您最近半年使用:0次
【推荐3】《南村辍耕录》中记载:“杭人削松木为小片,其薄如纸,熔硫磺涂木片顶端分许,名曰发烛。”文中的“发烛”就是原始的火柴。 在工业中用作制造火柴头的氧化剂。
在工业中用作制造火柴头的氧化剂。
已知反应:K2Cr2O7+14HCl(浓)=2KCl+2CrCl3+3Cl2↑+7H2O
(1)___________ (填元素名称)元素被氧化,___________ (填化学式,下同)是氧化剂。
(2)___________ 是氧化产物,___________ 发生氧化反应。
(3)在参加反应的盐酸中,起还原剂(被氧化)作用的 与起酸作用的
与起酸作用的 的质量比为
的质量比为___________ 。
(4)该反应中每生成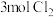 转移
转移___________  电子。
电子。
 在工业中用作制造火柴头的氧化剂。
在工业中用作制造火柴头的氧化剂。已知反应:K2Cr2O7+14HCl(浓)=2KCl+2CrCl3+3Cl2↑+7H2O
(1)
(2)
(3)在参加反应的盐酸中,起还原剂(被氧化)作用的
 与起酸作用的
与起酸作用的 的质量比为
的质量比为(4)该反应中每生成
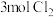 转移
转移 电子。
电子。
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】含氯物质在日常生活中具有许多重要用途,回答下列问题:
(1)亚氯酸钠 较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________(填标号)。
较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________(填标号)。
(2)我国从2000年起逐步用 替代氯气进行消毒,工业上常利用反应
替代氯气进行消毒,工业上常利用反应 制备
制备 ,
,________ 是还原剂,________ 是还原产物,用单线桥法表示反应中电子得失的方向和数目:___________ 。
(3)某温度下将 通入
通入 溶液里,反应后得到
溶液里,反应后得到 、
、 、
、 的混合溶液,其中
的混合溶液,其中 与
与 的个数之比为
的个数之比为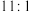 ,则
,则 与
与 反应时,被还原的氯原子和被氧化的氯原子的个数之比为
反应时,被还原的氯原子和被氧化的氯原子的个数之比为___________ 。
(1)亚氯酸钠
 较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________(填标号)。
较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________(填标号)。A. 、 、 | B. 、 、 |
C. 、 、 | D. 、 、 |
 替代氯气进行消毒,工业上常利用反应
替代氯气进行消毒,工业上常利用反应 制备
制备 ,
,(3)某温度下将
 通入
通入 溶液里,反应后得到
溶液里,反应后得到 、
、 、
、 的混合溶液,其中
的混合溶液,其中 与
与 的个数之比为
的个数之比为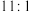 ,则
,则 与
与 反应时,被还原的氯原子和被氧化的氯原子的个数之比为
反应时,被还原的氯原子和被氧化的氯原子的个数之比为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】亚硝酸钠可使肉制品色泽粉红,外观上好看诱人,大量食用会致癌。
(1)NaNO2俗称“工业盐”,其外观食与盐相似,误食会中毒,可通过化学实验加以鉴别,如向NaNO2的酸性溶液中加入KI固体,析出的碘单质可以使淀粉溶液变蓝色,据此检验NaNO2。
①完成下列反应的化学方程式并配平:____ 。
_____NaNO2+_____KI+_____H2SO4=____Na2SO4+____K2SO4+____I2+___NO↑+_____
②该反应中被氧化的元素是___ 。
③标准状况下,该反应中每转移1mole-,生成气体的体积是___ 。
(2)硝酸工业生产中的尾气可用纯碱溶液吸收,有关的化学反应为:2NO2+Na2CO3=NaNO2+NaNO3+CO2↑,氧化剂与还原剂的物质的量之比为___ 。
(1)NaNO2俗称“工业盐”,其外观食与盐相似,误食会中毒,可通过化学实验加以鉴别,如向NaNO2的酸性溶液中加入KI固体,析出的碘单质可以使淀粉溶液变蓝色,据此检验NaNO2。
①完成下列反应的化学方程式并配平:
_____NaNO2+_____KI+_____H2SO4=____Na2SO4+____K2SO4+____I2+___NO↑+_____
②该反应中被氧化的元素是
③标准状况下,该反应中每转移1mole-,生成气体的体积是
(2)硝酸工业生产中的尾气可用纯碱溶液吸收,有关的化学反应为:2NO2+Na2CO3=NaNO2+NaNO3+CO2↑,氧化剂与还原剂的物质的量之比为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】完成下列小题
(1)下列变化需要加入还原剂才能实现的是_____ (填序号)。
①Fe2+→Fe②CO2→ ③
③ →Mn2+④SO2→SO3⑤KMnO4→MnO2⑥HCl→Cl2⑦
→Mn2+④SO2→SO3⑤KMnO4→MnO2⑥HCl→Cl2⑦ →SO2⑧
→SO2⑧ →NH3
→NH3
(2)黑火药是由硫黄、硝酸钾和木炭按一定比例混合而成,爆炸时的反应为S+2KNO3+3C K2S+N2↑+3CO2↑,反应中被还原的物质是
K2S+N2↑+3CO2↑,反应中被还原的物质是_____ (填化学式)。
(3)NaH可在野外作生氢剂,反应原理为NaH+H2O=NaOH+H2↑,该反应中氧化产物和还原产物的质量比为_____ 。
(4)2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,用单线桥标出电子转移的方向和数目_____ ;HCl表现出的性质是_____ 。
(1)下列变化需要加入还原剂才能实现的是
①Fe2+→Fe②CO2→
 ③
③ →Mn2+④SO2→SO3⑤KMnO4→MnO2⑥HCl→Cl2⑦
→Mn2+④SO2→SO3⑤KMnO4→MnO2⑥HCl→Cl2⑦ →SO2⑧
→SO2⑧ →NH3
→NH3(2)黑火药是由硫黄、硝酸钾和木炭按一定比例混合而成,爆炸时的反应为S+2KNO3+3C
 K2S+N2↑+3CO2↑,反应中被还原的物质是
K2S+N2↑+3CO2↑,反应中被还原的物质是(3)NaH可在野外作生氢剂,反应原理为NaH+H2O=NaOH+H2↑,该反应中氧化产物和还原产物的质量比为
(4)2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,用单线桥标出电子转移的方向和数目
您最近半年使用:0次



