下表为元素周期表的一部分,请参照元素①—⑩在表中的位置,
回答下列问题:
(1)⑩的离子结构示意图为______________ 。
(2)⑤⑥⑨⑩的离子半径由大到小的顺序为______________ (用离子符号表示)。
(3)④的氢化物沸点比⑨高,说明理由____________________________ 。
(4)上述元素构成的两个不同的10电子微粒,能反应生成两个相同的10电子微粒。写出二者反应的方程式为_________________________ 。
(5)由④⑤两种元素组成的一种化合物加入到硫酸亚铁溶液中,立即产生红褐色沉淀,但无气体产生,该化合物的电子式_____ ,该反应的离子方程式______________ 。
回答下列问题:
 族周期 族周期 | IA | 0 | ||||||
| 1 | ① | Ⅱ | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)⑩的离子结构示意图为
(2)⑤⑥⑨⑩的离子半径由大到小的顺序为
(3)④的氢化物沸点比⑨高,说明理由
(4)上述元素构成的两个不同的10电子微粒,能反应生成两个相同的10电子微粒。写出二者反应的方程式为
(5)由④⑤两种元素组成的一种化合物加入到硫酸亚铁溶液中,立即产生红褐色沉淀,但无气体产生,该化合物的电子式
10-11高三·重庆·阶段练习 查看更多[1]
(已下线)2012届重庆八中高三第二次月考理综试卷(化学部分)
更新时间:2016/12/09 02:09:00
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】高纯活性氧化锌可用于光催化、光电极、彩色显影等领域。以工业级氧化锌(含Fe2+、Mn2+、Cu2+、Ni2+、Cd2+等)为原料,用硫酸浸出法生产高纯活性氧化锌的工艺流程如下:
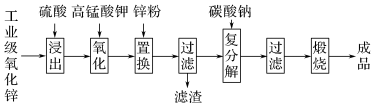
已知Ksp[Fe(OH)3]=8.0×10-38,回答下列问题:
(1)浸出时,为了提高浸出效率可采用的措施有(写一种既可)
(2)浸出步骤中发生主要反应的离子方程式为
(3)氧化时,加入KMnO4溶液是为了除去浸出液中的Fe2+和Mn2+(溶液中Mn全部转化为MnO2),请配平下列除去Fe2+的离子方程式:
□ +□Fe2++□___________=□MnO2↓+□Fe(OH)3↓+□H+
+□Fe2++□___________=□MnO2↓+□Fe(OH)3↓+□H+
(4)加入锌粉的目的是调节溶液pH除去Fe3+,和还原除去溶液中的
(5)已知H2SO4浸出液中,c(Fe2+)=50.4mg·L-1、c(Mn2+)=16.5mg·L-1,若要除尽1m3上述浸出液中的Fe2+和Mn2+,需加入
(6)若用酸性KMnO4标准溶液测定未知溶液中所含Fe2+的物质的量浓度(不含其他还原性粒子,MnO
 转化为Mn2+),不需要选取其他的指示剂,则滴定终点判断依据是
转化为Mn2+),不需要选取其他的指示剂,则滴定终点判断依据是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】为探究 溶液对氮氧化物
溶液对氮氧化物 的处理效果,进行如下实验:
的处理效果,进行如下实验: 具有强氧化性,且氧化性随着溶液的酸性增强而增强。
具有强氧化性,且氧化性随着溶液的酸性增强而增强。 和
和 反应的化学方程式为:
反应的化学方程式为: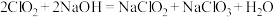 。
。 对氮氧化物具有强吸收效果。
对氮氧化物具有强吸收效果。
(1)“制气”阶段生成 和
和 。“制气”反应的化学方程式为
。“制气”反应的化学方程式为_______ 。
(2) 可以将
可以将 氧化为
氧化为 ,并进一步
,并进一步 氧化为
氧化为 ,
, 则被还原为
则被还原为 。吸收时,
。吸收时, 溶液从吸收器顶部喷淋,氮氧化物从吸收器底部通入(如图所示)。
溶液从吸收器顶部喷淋,氮氧化物从吸收器底部通入(如图所示)。 和
和 反应的离子方程式为
反应的离子方程式为_______ 。
②吸收器内装填碎瓷片填料的目的是_______ (填字母)。
A.增大氮氧化物的吸收速率 B.防止氮氧化物气体外逸
(3)通过加入盐酸或 调节
调节 溶液的
溶液的 ,测得不同
,测得不同 的
的 溶液对
溶液对 吸收率的影响如图所示。
吸收率的影响如图所示。 小于7时,
小于7时, 吸收率随
吸收率随 增大而减小的原因是
增大而减小的原因是_______ 。
②当 大于7时,
大于7时, 吸收率随
吸收率随 增大而增大的原因是
增大而增大的原因是_______ 。
 溶液对氮氧化物
溶液对氮氧化物 的处理效果,进行如下实验:
的处理效果,进行如下实验: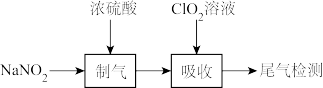
 具有强氧化性,且氧化性随着溶液的酸性增强而增强。
具有强氧化性,且氧化性随着溶液的酸性增强而增强。 和
和 反应的化学方程式为:
反应的化学方程式为: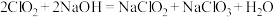 。
。 对氮氧化物具有强吸收效果。
对氮氧化物具有强吸收效果。(1)“制气”阶段生成
 和
和 。“制气”反应的化学方程式为
。“制气”反应的化学方程式为(2)
 可以将
可以将 氧化为
氧化为 ,并进一步
,并进一步 氧化为
氧化为 ,
, 则被还原为
则被还原为 。吸收时,
。吸收时, 溶液从吸收器顶部喷淋,氮氧化物从吸收器底部通入(如图所示)。
溶液从吸收器顶部喷淋,氮氧化物从吸收器底部通入(如图所示)。
 和
和 反应的离子方程式为
反应的离子方程式为②吸收器内装填碎瓷片填料的目的是
A.增大氮氧化物的吸收速率 B.防止氮氧化物气体外逸
(3)通过加入盐酸或
 调节
调节 溶液的
溶液的 ,测得不同
,测得不同 的
的 溶液对
溶液对 吸收率的影响如图所示。
吸收率的影响如图所示。
 小于7时,
小于7时, 吸收率随
吸收率随 增大而减小的原因是
增大而减小的原因是②当
 大于7时,
大于7时, 吸收率随
吸收率随 增大而增大的原因是
增大而增大的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】硫酸锰在电解锰、染料、造纸以及陶瓷等工业生产中有广泛的应用。工业上用软锰矿(主要成分为MnO2,含铁、铝的化合物等杂质)制得硫酸锰的流程如下:_______ 。此过程中,如果SO2废气中混有空气,有副反应发生,部分SO2被氧化为硫酸,致使浸出液的pH下降,这将不利于软锰矿浆继续吸收SO2,原因是_______ (用平衡移动原理结合化学方程式解释),欲消除生成的硫酸,试剂A最好是_______ 。
a.MnCO3 b.MnO2 c.CaO d.CaCO3
(2)SO2气体中混有空气,实验测得酸浸液中Mn2+、 的浓度随反应时间t变化如下图,产生该现象的原因是
的浓度随反应时间t变化如下图,产生该现象的原因是_______ 。_______ ;溶液的pH不能超过6的原因是_______ 。
(4)硫酸锰的溶解度曲线如下图所示,请设计由滤液制备MnSO4·H2O晶体的实验方案:_______ 。(实验中须用到的试剂:80~90℃的蒸馏水:除常用仪器外须使用的仪器:真空干燥箱。)

a.MnCO3 b.MnO2 c.CaO d.CaCO3
(2)SO2气体中混有空气,实验测得酸浸液中Mn2+、
 的浓度随反应时间t变化如下图,产生该现象的原因是
的浓度随反应时间t变化如下图,产生该现象的原因是
(4)硫酸锰的溶解度曲线如下图所示,请设计由滤液制备MnSO4·H2O晶体的实验方案:

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如图所示的装置进行实验。通入SO2气体,将带余烬的木条插入试管C中,木条复燃。
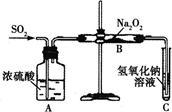
请回答下列问题:
(1)第一小组同学认为Na2O2与SO2反应生成了Na2SO3和O2,该反应的化学方程式是________________________ 。
(2)请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3__________ 。
(3)设计一种实验方案证明Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成。为检验是否由Na2SO4生成,他们设计了如下方案:

上述方案是否合理?________ (若不合理,请说明理由;若合理,以下不用回答)
①_______
②_______

请回答下列问题:
(1)第一小组同学认为Na2O2与SO2反应生成了Na2SO3和O2,该反应的化学方程式是
(2)请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3
(3)设计一种实验方案证明Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成。为检验是否由Na2SO4生成,他们设计了如下方案:

上述方案是否合理?
①
②
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】Na2O2可用作漂白剂和呼吸面具中的供氧剂。
(1)某学习小组发现:在盛有Na2O2的试管中加入足量水,立即产生大量气泡,当气泡消失后,向其中滴入1~2滴酚酞试液,溶液变红;将试管轻轻振荡,红色很快褪去;此时再向试管中加入少量MnO2粉末,又有气泡产生。
①使酚酞试液变红是因为____________________________________ ,红色褪去的可能原因是____________________________________________ 。
②加入MnO2反应的化学方程式为_______________________________ 。
(2)Na2O2有强氧化性,H2具有还原性,有同学猜想Na2O2与H2能反应。为了验证此猜想,该小组同学进行如下实验,实验步骤和现象如下。
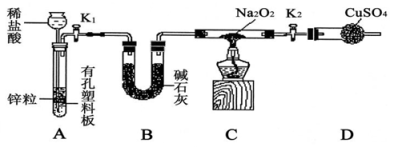
步骤1:按如图组装仪器(图中夹持仪器省略),检查气密性,装入药品;
步骤2:打开K1、K2,产生的氢气流经装有Na2O2的硬质玻璃管,一段时间后,没有任何现象;
步骤3:检验H2的纯度后,开始加热,观察到硬质玻璃管内Na2O2开始熔化,淡黄色的粉末变成了白色固体,干燥管内硫酸铜未变蓝色;
步骤4:反应后撤去酒精灯,待硬质玻璃管冷却后关闭K1。
①盛装稀盐酸的仪器名称___________ ;B装置的作用是______________ 。
②必须检验氢气纯度的原因是_________________ 。
③设置装置D的目的是___________________________ 。
(1)某学习小组发现:在盛有Na2O2的试管中加入足量水,立即产生大量气泡,当气泡消失后,向其中滴入1~2滴酚酞试液,溶液变红;将试管轻轻振荡,红色很快褪去;此时再向试管中加入少量MnO2粉末,又有气泡产生。
①使酚酞试液变红是因为
②加入MnO2反应的化学方程式为
(2)Na2O2有强氧化性,H2具有还原性,有同学猜想Na2O2与H2能反应。为了验证此猜想,该小组同学进行如下实验,实验步骤和现象如下。

步骤1:按如图组装仪器(图中夹持仪器省略),检查气密性,装入药品;
步骤2:打开K1、K2,产生的氢气流经装有Na2O2的硬质玻璃管,一段时间后,没有任何现象;
步骤3:检验H2的纯度后,开始加热,观察到硬质玻璃管内Na2O2开始熔化,淡黄色的粉末变成了白色固体,干燥管内硫酸铜未变蓝色;
步骤4:反应后撤去酒精灯,待硬质玻璃管冷却后关闭K1。
①盛装稀盐酸的仪器名称
②必须检验氢气纯度的原因是
③设置装置D的目的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下表为元素周期表的一部分,表中列出了10种元素,针对这些元素完成下列问题
(1)非金属性最强的元素是_______ (填元素名称);
(2)NaOH与Mg(OH)2中,碱性较强的是_______ ;
(3)第三周期这五种元素中,元素原子半径最大的是_______ (填元素符号);
(4)Ne原子的最外层电子数为_______ ;
(5)写出一种含有氮元素的化肥_______ (填化学式);
(6)有一种元素形成化合物种类最多,该元素最高价氧化物是_______ (填化学式);
(7)铝是一种重要的金属材料,其主要用于_______ (填一种用途);
(8)硫具有广泛的用途,主要用于制造硫酸等。写出硫在氧气中燃烧生成二氧化硫的化学方程式:_______ 。
(9)溴被称为“海洋元素”,从海水中提取溴,通常是将氯气通入含 的苦卤中置换出单质溴,则Cl2与Br2中氧化性较强的是Cl2,反应物中Cl2与
的苦卤中置换出单质溴,则Cl2与Br2中氧化性较强的是Cl2,反应物中Cl2与 物质的量比是
物质的量比是_______ (“1∶1”或“1∶2”)。
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | S | Cl | |||
| 4 | Br |
(2)NaOH与Mg(OH)2中,碱性较强的是
(3)第三周期这五种元素中,元素原子半径最大的是
(4)Ne原子的最外层电子数为
(5)写出一种含有氮元素的化肥
(6)有一种元素形成化合物种类最多,该元素最高价氧化物是
(7)铝是一种重要的金属材料,其主要用于
(8)硫具有广泛的用途,主要用于制造硫酸等。写出硫在氧气中燃烧生成二氧化硫的化学方程式:
(9)溴被称为“海洋元素”,从海水中提取溴,通常是将氯气通入含
 的苦卤中置换出单质溴,则Cl2与Br2中氧化性较强的是Cl2,反应物中Cl2与
的苦卤中置换出单质溴,则Cl2与Br2中氧化性较强的是Cl2,反应物中Cl2与 物质的量比是
物质的量比是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表是元素周期表的一部分,用化学用语回答下列问题:
(1)①-⑩号元素中元素的最高价氧化物对应的水化物中酸性最强的是_______ ,碱性最强的是_______ (均用化学式表示)。
(2)④⑤⑥⑦的简单离子半径由大到小的顺序为_______ (用离子符号和“>”表示)。
(3)②与④可以形成一种温室气体,用电子式表示其形成过程_______ 。
(4)由①③⑩三种元素形成的一种离子化合物的电子式_______ 。
(5)欲比较④和⑨两种元素的非金属性强弱,可以作为验证的证据是_______ (填字母)。
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气化合的难易
C.比较这两种元素的最高价氧化物对应水化物的酸性
(6)表中③和⑤可形成一种相对分子量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构简式为_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
| 4 |
(2)④⑤⑥⑦的简单离子半径由大到小的顺序为
(3)②与④可以形成一种温室气体,用电子式表示其形成过程
(4)由①③⑩三种元素形成的一种离子化合物的电子式
(5)欲比较④和⑨两种元素的非金属性强弱,可以作为验证的证据是
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气化合的难易
C.比较这两种元素的最高价氧化物对应水化物的酸性
(6)表中③和⑤可形成一种相对分子量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构简式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】元素周期表与元素周期律在学习、研究中有很重要的作用。下表所示为某5种元素的相关信息,已知W、X都位于第三周期。回答下列问题:
(1)W在元素周期表中的位置为______ ,X的最高价氧化物对应的水化物的电子式为_______ 。
(2)金属性:Y_____ X(填“>”或“<”)
(3)下列对于Z及其化合物的推断中正确的是___________(填标号)。
(4)将X元素的单质在Q元素的单质中点燃生成M,预测将M投入FeSO4溶液中,主要的反应现象是______ 。
| 元素 | 信息 |
| Q | 地壳中含量最高的元素 |
| W | 最高化合价为+7 |
| X | 最高价氧化物对应的水化物在本周期中碱性最强 |
| Y | 焰色试验(透过蓝色钴玻璃)的火焰呈紫色 |
| Z | 原子结构示意图为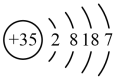 |
(2)金属性:Y
(3)下列对于Z及其化合物的推断中正确的是___________(填标号)。
| A.Z元素的化合价只有-1和+7 |
| B.Z的最高价氧化物对应水化物的酸性弱于W的最高价氧化物对应水化物的酸性 |
| C.Z的气态氢化物比W的气态氢化物稳定 |
| D.Z单质的熔沸点比W单质的熔沸点高 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下表是元素周期表的一部分,按要求填空
(1)①~⑧元素中金属性最强的元素是___________ (写元素符号),画出⑨的原子结构示意图___________ 。
(2)①~⑧元素中,最高价氧化物水化物酸性最强的物质是___________ (写化学式)。
(3)⑤⑥⑦⑧四种元素中,离子半径最小的是___________ (填离子符号)。
(4)⑧的一种含氧酸具有强氧化性,常用于杀菌、消毒、漂白,请用写出该化合物的电子式___________ 。
(5)将54.4 g铁粉和氧化铁的混合物中加入200 mL的稀硫酸,恰好完全反应,放出氢气4.48 L(标准状况)反应后的溶液中滴加KSCN不显红色。求:
I. 混合物中氧化铁是___________ g。
II. 原稀硫酸的物质的量浓度___________ mol·L-1。
周期 族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)①~⑧元素中,最高价氧化物水化物酸性最强的物质是
(3)⑤⑥⑦⑧四种元素中,离子半径最小的是
(4)⑧的一种含氧酸具有强氧化性,常用于杀菌、消毒、漂白,请用写出该化合物的电子式
(5)将54.4 g铁粉和氧化铁的混合物中加入200 mL的稀硫酸,恰好完全反应,放出氢气4.48 L(标准状况)反应后的溶液中滴加KSCN不显红色。求:
I. 混合物中氧化铁是
II. 原稀硫酸的物质的量浓度
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】随着原子序数的递增,8种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示。
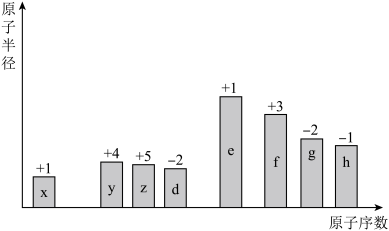
请用化学用语回答下列问题:
(1)f在元素周期表中的位置是_______ 。
(2)比较d、e常见离子的半径,半径大的是:_______ (用化学式表示,下同);g、h的最高价氧化物的水化物中酸性强的是:_______ 。
(3)d、g的单质分别与x的单质化合时,较容易的是_______ (用化学式表示,下同),形成的化合物热稳定性较差的是_______ 。x2d、x2g沸点较高的是_______ ,原因是_______ 。
(4)任选上述元素形成一种四原子共价化合物,写出其电子式:_______ 。

请用化学用语回答下列问题:
(1)f在元素周期表中的位置是
(2)比较d、e常见离子的半径,半径大的是:
(3)d、g的单质分别与x的单质化合时,较容易的是
(4)任选上述元素形成一种四原子共价化合物,写出其电子式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子,B元素的原子半径是其所在主族元素原子中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层电子数多4;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族。请用化学用语完成下列问题:
(1)D在周期表中的位置为_____ ;B的原子结构示意图为_______ 。
(2)含有10个中子的C的原子是:_______ 。
(3)E元素形成的最高价氧化物对应水化物的化学式为_______ 。
(4)元素C、D、E的原子半径大小关系是________ (用元素符号表示)。
(5)化合物D2C2与A2C反应的离子方程式是________ 。
(1)D在周期表中的位置为
(2)含有10个中子的C的原子是:
(3)E元素形成的最高价氧化物对应水化物的化学式为
(4)元素C、D、E的原子半径大小关系是
(5)化合物D2C2与A2C反应的离子方程式是
您最近一年使用:0次



