苯甲醛在浓氢氧化钾溶液中发生Cannizzaro反应,反应方程式如下,可用于制备苯甲酸和苯甲醇。
2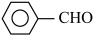 +KOH
+KOH
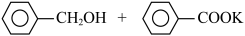 \
\
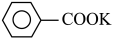 +HCl
+HCl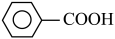
已知:
①乙醚微溶于水,是有机物良好的溶剂,沸点34.6℃,极易挥发,在空气中的沸点160℃。
②苯甲酸在水中的溶解度0.17g(25℃),0.95g(50℃),6.8g(95℃)
实验步骤:
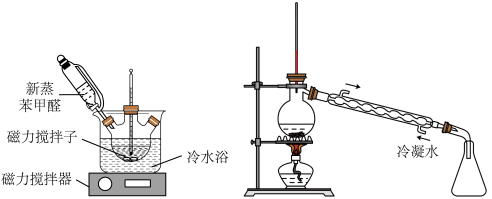
①在50mL三口瓶中加入4.5g KOH和4.5mL水,将装置置于冷水浴中,打开磁力搅拌器,分批加入5mL 新蒸苯甲醛(密度1.04g/mL),使反应物充分混合(如上左图),最后成为白色糊状物,放置24h以上。
②向反应混合物中逐渐加入足量水并振荡,使其完全溶解后倒入_____ (填装置名称)中,用10mL 乙醚萃取3次,合并乙醚萃取液,并依次用3mL饱和亚硫酸氢钠、5mL 10% Na2CO3溶液及5mL水洗涤,分出的乙醚层用无水Na2CO3干燥。
③干燥后的乙醚溶液在水浴中蒸去乙醚,然后适当调整和改造装置(如上右图),继续加热蒸馏,收集198℃~204℃的苯甲醇馏分,产量为2.16g。
④乙醚萃取后的水溶液(水层),用浓盐酸酸化并充分冷却,使苯甲酸完全析出,过滤,粗产品用水重结晶得到苯甲酸,产量是2g。
(1)不断搅拌然后放置24h的目的是____________________________________
(2)步骤②横线处装置名称是___________________________
(3)萃取液共洗涤了3次,其中10% 碳酸钠溶液欲除去的杂质是_______ (填化学式)

(4)使用水浴蒸去乙醚的优点是_____________
(5)蒸去乙醚后适当的调整和改造装置,应将上右图虚线框中的装置换为________ 。
(6)苯甲酸重结晶时,常用冷水洗涤固体,其目的是______ ;苯甲酸重结晶时所需的玻璃仪器有__________________
①烧杯 ②试管 ③锥形瓶 ④酒精灯 ⑤量筒 ⑥短颈玻璃漏斗 ⑦玻璃棒
(7)该实验中Cannizzaro反应的转化率是_____ %(保留1位小数)。通常,该实验中苯甲酸的产率会比苯甲醇更低,但若是某次实验中并未塞紧瓶塞,导致苯甲酸的产率明显偏高,分析可能的原因是__________ 。
2
 +KOH
+KOH
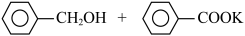 \
\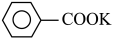 +HCl
+HCl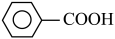

已知:
①乙醚微溶于水,是有机物良好的溶剂,沸点34.6℃,极易挥发,在空气中的沸点160℃。
②苯甲酸在水中的溶解度0.17g(25℃),0.95g(50℃),6.8g(95℃)
实验步骤:
①在50mL三口瓶中加入4.5g KOH和4.5mL水,将装置置于冷水浴中,打开磁力搅拌器,分批加入5mL 新蒸苯甲醛(密度1.04g/mL),使反应物充分混合(如上左图),最后成为白色糊状物,放置24h以上。
②向反应混合物中逐渐加入足量水并振荡,使其完全溶解后倒入
③干燥后的乙醚溶液在水浴中蒸去乙醚,然后适当调整和改造装置(如上右图),继续加热蒸馏,收集198℃~204℃的苯甲醇馏分,产量为2.16g。
④乙醚萃取后的水溶液(水层),用浓盐酸酸化并充分冷却,使苯甲酸完全析出,过滤,粗产品用水重结晶得到苯甲酸,产量是2g。
(1)不断搅拌然后放置24h的目的是
(2)步骤②横线处装置名称是
(3)萃取液共洗涤了3次,其中10% 碳酸钠溶液欲除去的杂质是

(4)使用水浴蒸去乙醚的优点是
(5)蒸去乙醚后适当的调整和改造装置,应将上右图虚线框中的装置换为
(6)苯甲酸重结晶时,常用冷水洗涤固体,其目的是
①烧杯 ②试管 ③锥形瓶 ④酒精灯 ⑤量筒 ⑥短颈玻璃漏斗 ⑦玻璃棒
(7)该实验中Cannizzaro反应的转化率是
更新时间:2019-04-03 15:07:47
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】高氯酸铜晶体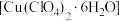 易溶于水,120℃开始分解,常用于生产电极和燃烧的催化剂等.实验室以硫酸铜为原料制备少量高氯酸铜晶体的步骤如下:
易溶于水,120℃开始分解,常用于生产电极和燃烧的催化剂等.实验室以硫酸铜为原料制备少量高氯酸铜晶体的步骤如下:
Ⅰ.称取12.5g 和9.6g
和9.6g ,混合研细后,投入100mL70~80℃热水,快速搅拌,静置得绿色沉淀
,混合研细后,投入100mL70~80℃热水,快速搅拌,静置得绿色沉淀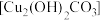 ;
;
Ⅱ.冷却,过滤,用少量蒸馏水洗涤沉淀2~3次;
Ⅲ.在沉淀中慢慢滴加70% 溶液,适度加热搅拌至不再产生气体;
溶液,适度加热搅拌至不再产生气体;
Ⅳ.过滤,得蓝色高氯酸铜溶液;
Ⅴ.在通风橱中蒸发至不再产生白雾,继续蒸发至有晶膜出现,冷却、结晶、过滤、洗涤,得蓝色晶体;
Ⅵ.60℃下,在烘箱中干燥2h,得16.695g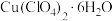 晶体。
晶体。
回答下列问题:
(1)“步骤Ⅰ”中研磨用到的仪器名称是________ ,“步骤Ⅴ”中蒸发需要用到下列仪器中的________ (填字母序号). 和
和 研细的目的是
研细的目的是________________ ,写出它们在溶液中反应生成 的离子方程式:
的离子方程式:________________ ,实际操作中 与
与 的物质的量之比大于
的物质的量之比大于 ,原因是
,原因是________________ 。
(3)“步骤Ⅱ”中检验沉淀是否洗净所需试剂为________ 。
(4)“步骤Ⅴ”在通风橱中进行的原因是________________ 。
(5)某温度下,高氯酸铜同时按以下两种方式分解:(A)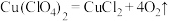 ;(B)
;(B)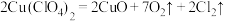 ,若测得
,若测得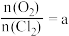 ,则按(A)式分解的高氯酸铜的质量分数为
,则按(A)式分解的高氯酸铜的质量分数为________ (用含a的代数式表示)。
(6)上述过程中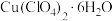 的产率为
的产率为________ 。
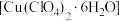 易溶于水,120℃开始分解,常用于生产电极和燃烧的催化剂等.实验室以硫酸铜为原料制备少量高氯酸铜晶体的步骤如下:
易溶于水,120℃开始分解,常用于生产电极和燃烧的催化剂等.实验室以硫酸铜为原料制备少量高氯酸铜晶体的步骤如下:Ⅰ.称取12.5g
 和9.6g
和9.6g ,混合研细后,投入100mL70~80℃热水,快速搅拌,静置得绿色沉淀
,混合研细后,投入100mL70~80℃热水,快速搅拌,静置得绿色沉淀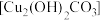 ;
;Ⅱ.冷却,过滤,用少量蒸馏水洗涤沉淀2~3次;
Ⅲ.在沉淀中慢慢滴加70%
 溶液,适度加热搅拌至不再产生气体;
溶液,适度加热搅拌至不再产生气体;Ⅳ.过滤,得蓝色高氯酸铜溶液;
Ⅴ.在通风橱中蒸发至不再产生白雾,继续蒸发至有晶膜出现,冷却、结晶、过滤、洗涤,得蓝色晶体;
Ⅵ.60℃下,在烘箱中干燥2h,得16.695g
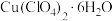 晶体。
晶体。回答下列问题:
(1)“步骤Ⅰ”中研磨用到的仪器名称是
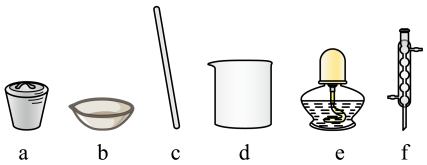
 和
和 研细的目的是
研细的目的是 的离子方程式:
的离子方程式: 与
与 的物质的量之比大于
的物质的量之比大于 ,原因是
,原因是(3)“步骤Ⅱ”中检验沉淀是否洗净所需试剂为
(4)“步骤Ⅴ”在通风橱中进行的原因是
(5)某温度下,高氯酸铜同时按以下两种方式分解:(A)
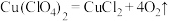 ;(B)
;(B)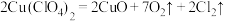 ,若测得
,若测得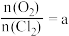 ,则按(A)式分解的高氯酸铜的质量分数为
,则按(A)式分解的高氯酸铜的质量分数为(6)上述过程中
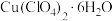 的产率为
的产率为
您最近一年使用:0次
【推荐2】(1)根据下图回答相关问题:

该图所示进行的是过滤操作,图中还缺少的仪器是________ ,其作用是___________ 。
(2)填写仪器名称:
①制取蒸馏水的受热容器是________ 。
②石油蒸馏装置中通水冷却的仪器是____________ 。
③用于分液的关键仪器是____________ 。
(3)已知,NaBiO3是一种不溶于水的固体,将其加入含有Mn2+的酸性溶液中,溶液变为紫红色,Bi元素变为无色的Bi3+。写出该反应的离子反应方程式_____________________ 。
(4)比较酸性强弱:H2SO4______ HClO4(填“>”、“=”或“<”)。已知,次氯酸的酸性介于碳酸和碳酸氢根之间,比较ClO-、 结合氢离子的强弱
结合氢离子的强弱____________ 。

该图所示进行的是过滤操作,图中还缺少的仪器是
(2)填写仪器名称:
①制取蒸馏水的受热容器是
②石油蒸馏装置中通水冷却的仪器是
③用于分液的关键仪器是
(3)已知,NaBiO3是一种不溶于水的固体,将其加入含有Mn2+的酸性溶液中,溶液变为紫红色,Bi元素变为无色的Bi3+。写出该反应的离子反应方程式
(4)比较酸性强弱:H2SO4
 结合氢离子的强弱
结合氢离子的强弱
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某校学习小组的同学设计用分子筛催化CH4还原NO2并检验还原产物。回答下列问题:
(1)甲组同学设计用如图所示装置分别制备CH4和NO2。

①在加热条件下,无水CH3 COONa与NaOH(CaO为催化剂)生成CH4和Na2CO3的化学方程式为___________ 。
②仪器a的名称为__________ ,仪器a中的药品是__________ (填名称)。__________ (填“能”或“不能”)用铁代替圆底烧瓶中的铜。
(2)乙组同学利用甲组制得的干燥气体并利用下列装置用CH4还原NO2

①C装置的作用是______________ (列举2点)。
②D装置反应管中盛放玻璃丝的目的是___________ ;CH4与NO2生成N2和CO2的化学方程式为_____________ 。
③E装置中澄清石灰水未变浑浊,F装置中澄清石灰水变浑浊,其原因可能是__________ 。
(1)甲组同学设计用如图所示装置分别制备CH4和NO2。

①在加热条件下,无水CH3 COONa与NaOH(CaO为催化剂)生成CH4和Na2CO3的化学方程式为
②仪器a的名称为
(2)乙组同学利用甲组制得的干燥气体并利用下列装置用CH4还原NO2

①C装置的作用是
②D装置反应管中盛放玻璃丝的目的是
③E装置中澄清石灰水未变浑浊,F装置中澄清石灰水变浑浊,其原因可能是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】镍目前有广泛的用途,不仅可以用于不锈钢的制取中,目前也是三元锂电池中的重要元素。由红土镍矿(主要成分为NiO,还含有少量 、
、 以及铁的氧化物等)可以制取黄钠铁矾
以及铁的氧化物等)可以制取黄钠铁矾 和
和 。
。
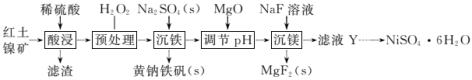
(1)为加快红土镍矿的溶解,在酸浸步骤中可以采取的措施是_______ (任写一条即可);“预处理”中,发生的离子方程式可能为_______ 。
(2)“沉铁”中若采用 作为除铁所需钠源,
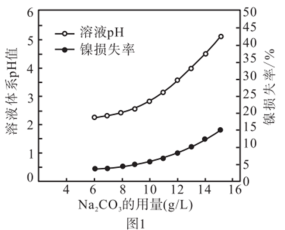
作为除铁所需钠源, 溶液的用量对体系pH和镍的损失影响如图1所示。当
溶液的用量对体系pH和镍的损失影响如图1所示。当 溶液的用量超过6 g/L时,镍的损失率会增大,其可能的原因是
溶液的用量超过6 g/L时,镍的损失率会增大,其可能的原因是_______ 。( 、
、 开始沉淀的pH分别为2.2、7.5)
开始沉淀的pH分别为2.2、7.5)
(3)若溶液中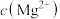 为0.1 mol/L,溶液的体积为1 L,则要使溶液中
为0.1 mol/L,溶液的体积为1 L,则要使溶液中 mol/L,则应加入固体NaF为
mol/L,则应加入固体NaF为_______ mol[忽略体积的变化,已知 ]。“沉镁”时应保证MgO已将溶液的pH调节至5.5~6.0的原因是
]。“沉镁”时应保证MgO已将溶液的pH调节至5.5~6.0的原因是_______ 。
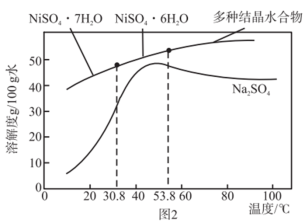
(4)硫酸钠与硫酸镍晶体溶解度曲线图如图2所示,请设计由滤液Y制备 的实验方案:边搅拌边向滤液Y中滴加
的实验方案:边搅拌边向滤液Y中滴加_______ 至沉淀完全,过滤;用蒸馏水洗涤固体至最后一次洗涤滤液加_______ 无沉淀出现;将所得固体分批加入足量稀硫酸,搅拌使其完全溶解;稍低于53.8℃减压蒸发浓缩,降温至稍高于_______ ℃,趁热过滤。[填试剂,可选用的试剂:稀硫酸,NaOH溶液、 溶液、
溶液、 、蒸馏水]
、蒸馏水]
 、
、 以及铁的氧化物等)可以制取黄钠铁矾
以及铁的氧化物等)可以制取黄钠铁矾 和
和 。
。
(1)为加快红土镍矿的溶解,在酸浸步骤中可以采取的措施是
(2)“沉铁”中若采用
 作为除铁所需钠源,
作为除铁所需钠源, 溶液的用量对体系pH和镍的损失影响如图1所示。当
溶液的用量对体系pH和镍的损失影响如图1所示。当 溶液的用量超过6 g/L时,镍的损失率会增大,其可能的原因是
溶液的用量超过6 g/L时,镍的损失率会增大,其可能的原因是 、
、 开始沉淀的pH分别为2.2、7.5)
开始沉淀的pH分别为2.2、7.5)
(3)若溶液中
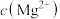 为0.1 mol/L,溶液的体积为1 L,则要使溶液中
为0.1 mol/L,溶液的体积为1 L,则要使溶液中 mol/L,则应加入固体NaF为
mol/L,则应加入固体NaF为 ]。“沉镁”时应保证MgO已将溶液的pH调节至5.5~6.0的原因是
]。“沉镁”时应保证MgO已将溶液的pH调节至5.5~6.0的原因是(4)硫酸钠与硫酸镍晶体溶解度曲线图如图2所示,请设计由滤液Y制备
 的实验方案:边搅拌边向滤液Y中滴加
的实验方案:边搅拌边向滤液Y中滴加 溶液、
溶液、 、蒸馏水]
、蒸馏水]
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室需要0.2 mol/L NaOH溶液 480 mL。根据该溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是_______ (填仪器名称)。

(2)实验步骤如下:
①计算:需要NaOH固体质量为_______ g。
②称量:用托盘天平称取NaOH固体,称量时注意要装在_______ (填仪器名称)里称量
③溶解:用量筒量取蒸馏水注入烧杯里,玻璃棒作用:_______
④冷却:将溶液冷却至室温。
⑤移液:将冷却溶液用玻璃棒引流到容量瓶中。
⑥洗涤:用适量蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液注入容量瓶里。
⑦振荡:手持容量瓶轻轻振荡,使溶液充分混合均匀。
⑧定容:继续加蒸馏水至距刻度线凹液面2~3cm处,然后改用_______ (填仪器名称)滴加蒸馏水正好至刻度线。
⑨摇匀:盖好玻璃塞,反复上下颠倒,使溶液均匀。
(3)在配制NaOH溶液时:
①若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度_______ (填“偏大”“偏小”或“无影响”);
②定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水_______ (填“偏大”“偏小”或“无影响”)。
(1)如图所示的仪器中配制溶液肯定不需要的是

(2)实验步骤如下:
①计算:需要NaOH固体质量为
②称量:用托盘天平称取NaOH固体,称量时注意要装在
③溶解:用量筒量取蒸馏水注入烧杯里,玻璃棒作用:
④冷却:将溶液冷却至室温。
⑤移液:将冷却溶液用玻璃棒引流到容量瓶中。
⑥洗涤:用适量蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液注入容量瓶里。
⑦振荡:手持容量瓶轻轻振荡,使溶液充分混合均匀。
⑧定容:继续加蒸馏水至距刻度线凹液面2~3cm处,然后改用
⑨摇匀:盖好玻璃塞,反复上下颠倒,使溶液均匀。
(3)在配制NaOH溶液时:
①若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度
②定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】海带中含有丰富的碘。为了从海中提取碘,某研究性学习小姐设计并进行了以下实验,请填写下列空白:
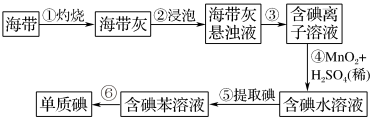
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是___ (用标号字母填写在空白处)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是___ ,步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是__ 。
(3)步骤④反应的离子方程式是___ 。
(4)步骤⑤中,某学生选择用苯来提取碘的理由是__ 、___ 。
(5)请设计一种检验提取碘后的水溶液中是否还有单质碘的简单方法:___ 。

(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是
(3)步骤④反应的离子方程式是
(4)步骤⑤中,某学生选择用苯来提取碘的理由是
(5)请设计一种检验提取碘后的水溶液中是否还有单质碘的简单方法:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】下图为实验室制乙烯(A)、硝基苯(B)和石油分馏(C)的装置:

(1)写出制取乙烯、硝基苯的化学方程式:___________ 、_________ 。
(2)在A和 C实验中需加碎瓷片,其目的是_______________ 。
(3)分离实验B中硝基苯的方法是__________ 。
(4)在石油分馏实验中,冷凝水的流向应是_______ 进______ 出(填字母a、b)。
(5)实验室制乙烯时,常伴随有刺激性气味的气体产生,为消除其对乙烯性质实验的干扰,可将气体通过_______ 溶液除去。若反应没有及时升温至170℃,可能带来的主要副产物是____ (填名称)。

(1)写出制取乙烯、硝基苯的化学方程式:
(2)在A和 C实验中需加碎瓷片,其目的是
(3)分离实验B中硝基苯的方法是
(4)在石油分馏实验中,冷凝水的流向应是
(5)实验室制乙烯时,常伴随有刺激性气味的气体产生,为消除其对乙烯性质实验的干扰,可将气体通过
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】实验室用不同的实验装置研究苯与液溴的反应并制取少量溴苯。试回答下列问题:

(1)若采用图甲装置进行实验,装置A中应预先需加入的试剂是____ ,E装置的作用是___ 。
(2)若采用图乙装置进行实验,C中盛放的CCl4的作用是____________ 。
(3)若使用图乙装置,实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,然后用___ (填仪器名称)分离出溴苯(仍含有少量苯)。写出有关的离子反应方程式__________ 。
(4)反应完毕后,向试管D中滴加AgNO3溶液,若有_______ (填现象)生成,说明这种获得溴苯的反应属于______ (填有机反应类型)。

(1)若采用图甲装置进行实验,装置A中应预先需加入的试剂是
(2)若采用图乙装置进行实验,C中盛放的CCl4的作用是
(3)若使用图乙装置,实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,然后用
(4)反应完毕后,向试管D中滴加AgNO3溶液,若有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】实验室制备1,2—二溴乙烷,可用足量的乙醇先制备乙烯,再用乙烯和少量的溴制备1,2—二溴乙烷,装置如图所示。有关数据列表如表所示。回答下列问题:

(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是__ 。
a.引发反应 b.加快反应速度
c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置A中除了浓硫酸和乙醇外,还应加入__ ,其目的是__ 。装置A中生成副产物乙醚的化学反应方程式为__ 。
(3)实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的SO2,为了验证SO2的存在并除去SO2对后续反应的干扰,某同学在A和D之间加入了B、C两个装置,其中B和C中可分别盛放___ 。
a.酸性KMnO4和水 b.品红和NaOH溶液
c.酸性KMnO4和NaOH溶液 d.品红和酸性KMnO4
(4)甲、乙两装置均可用作实验室由无水乙醇制取乙烯,乙图采用甘油浴加热(甘油沸点290℃,熔点18.17℃),当甘油温度达到反应温度时,将盛有无水乙醇和浓硫酸混合液的烧瓶放入甘油中,很快达到反应温度。甲、乙两装置相比较,乙装置有哪些优点__ ,写出该实验中由无水乙醇制取乙烯的化学方程式___ 。

(5)将1,2—二溴乙烷粗产品置于分液漏斗中加水,振荡后静置后,产物应在__ 层;若产物中有少量副产物乙醚。可用__ 的方法除去。

| 乙醇 | 1,2—二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
a.引发反应 b.加快反应速度
c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置A中除了浓硫酸和乙醇外,还应加入
(3)实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的SO2,为了验证SO2的存在并除去SO2对后续反应的干扰,某同学在A和D之间加入了B、C两个装置,其中B和C中可分别盛放
a.酸性KMnO4和水 b.品红和NaOH溶液
c.酸性KMnO4和NaOH溶液 d.品红和酸性KMnO4
(4)甲、乙两装置均可用作实验室由无水乙醇制取乙烯,乙图采用甘油浴加热(甘油沸点290℃,熔点18.17℃),当甘油温度达到反应温度时,将盛有无水乙醇和浓硫酸混合液的烧瓶放入甘油中,很快达到反应温度。甲、乙两装置相比较,乙装置有哪些优点

(5)将1,2—二溴乙烷粗产品置于分液漏斗中加水,振荡后静置后,产物应在
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
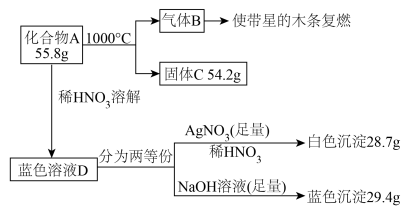
【推荐1】固体化合物A由3种中学常见元素组成,常温下难溶于水但能溶于硝酸,某学习小组开展如图所示探究实验。
请回答下列问题。
(1)化合物A的3种元素是______ 。
(2)往蓝色溶液D中通入 刚开始产生无色气体在空气中变红棕色,①写出其产生无色气体的离子方程式:
刚开始产生无色气体在空气中变红棕色,①写出其产生无色气体的离子方程式:______ ;②设计实验验证该氧化还原反应的氧化产物:______ 。
(3)固体C的化学式是______ ;化合物A与稀硝酸反应的离子方程式是______ 。

请回答下列问题。
(1)化合物A的3种元素是
(2)往蓝色溶液D中通入
 刚开始产生无色气体在空气中变红棕色,①写出其产生无色气体的离子方程式:
刚开始产生无色气体在空气中变红棕色,①写出其产生无色气体的离子方程式:(3)固体C的化学式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线:
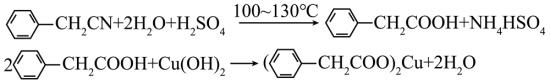
制备苯乙酸的装置示意图如图所示(加热和夹持装置等略)。
已知:苯乙酸的熔点为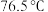 ,微溶于冷水,溶于乙醇。
,微溶于冷水,溶于乙醇。
回答下列问题:

(1)将a中的溶液加热至 ,缓缓滴加
,缓缓滴加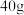 苯乙腈到硫酸溶液中,然后升温至
苯乙腈到硫酸溶液中,然后升温至 继续反应.在装置中,仪器c的名称是
继续反应.在装置中,仪器c的名称是_____________ ,其作用是________________________ 。
(2)反应结束后加适量冷水,再分离出苯乙酸粗品.加入冷水的目的是____________________ 。
(3)分离苯乙酸粗品的方法是_________________ ,提纯粗苯乙酸的方法是_______________ 。最终得到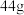 纯品,则苯乙酸的产率是
纯品,则苯乙酸的产率是______________ (保留两位有效数字)。
(4)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入 搅拌
搅拌 ,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是
,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是________________ 。

制备苯乙酸的装置示意图如图所示(加热和夹持装置等略)。
已知:苯乙酸的熔点为
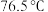 ,微溶于冷水,溶于乙醇。
,微溶于冷水,溶于乙醇。回答下列问题:

(1)将a中的溶液加热至
 ,缓缓滴加
,缓缓滴加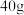 苯乙腈到硫酸溶液中,然后升温至
苯乙腈到硫酸溶液中,然后升温至 继续反应.在装置中,仪器c的名称是
继续反应.在装置中,仪器c的名称是(2)反应结束后加适量冷水,再分离出苯乙酸粗品.加入冷水的目的是
(3)分离苯乙酸粗品的方法是
 纯品,则苯乙酸的产率是
纯品,则苯乙酸的产率是(4)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入
 搅拌
搅拌 ,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是
,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】碘酸钙是食品及饲料添加剂中补碘补钙的常用试剂,微溶于水。实验室制备碘酸钙的实验流程如下:
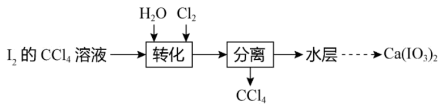
已知:碘酸易溶于水,不溶于有机溶剂。
(1)转化
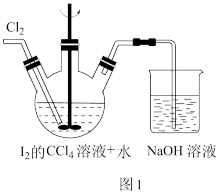
①用图1所示的装置制得碘酸。CCl4的作用_______ ;
②实验中判断碘反应完全的实验现象是_______ 。
③三颈烧瓶中发生的离子方程式_______ 。
(2)分离:
除去HIO3溶液中少量的I2的实验方法为_______ ,直至用淀粉溶液检验不出碘单质的存在。
(3)制取碘酸钙
已知:①本实验中水溶液中分离出Ca(IO3)2•6H2O;
②M[Ca(IO3)2]=390g•mol-1;
③Ca(IO3)2•6H2O是一种难溶于水的白色固体,在碱性条件下不稳定;
④Ca(IO3)2•6H2O加热升温过程中剩余固体的质量分数w随温度变化的关系如图2所示。
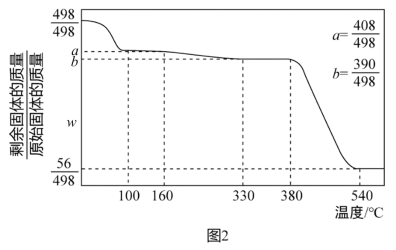
请结合上述信息,以除碘并煮沸后的水层为原料,制取Ca(IO3)2的实验方案:向水层中_______ [实验中须使用的试剂:Ca(OH)2粉末、AgNO3溶液]。
(4)测定产品纯度:
取0.5000g产品,酸化溶解,配成250mL溶液,取25.00mL上述溶液于锥形瓶中,加入足量的KI溶液充分反应,用0.04000mol/L硫代硫酸钠溶液滴定,消耗30.00mL硫代硫酸钠溶液,试求该产品的纯度____ 。(写出计算过程)(已知:2Na2S2O3+I2=Na2S4O6+2NaI)

已知:碘酸易溶于水,不溶于有机溶剂。
(1)转化

①用图1所示的装置制得碘酸。CCl4的作用
②实验中判断碘反应完全的实验现象是
③三颈烧瓶中发生的离子方程式
(2)分离:
除去HIO3溶液中少量的I2的实验方法为
(3)制取碘酸钙
已知:①本实验中水溶液中分离出Ca(IO3)2•6H2O;
②M[Ca(IO3)2]=390g•mol-1;
③Ca(IO3)2•6H2O是一种难溶于水的白色固体,在碱性条件下不稳定;
④Ca(IO3)2•6H2O加热升温过程中剩余固体的质量分数w随温度变化的关系如图2所示。

请结合上述信息,以除碘并煮沸后的水层为原料,制取Ca(IO3)2的实验方案:向水层中
(4)测定产品纯度:
取0.5000g产品,酸化溶解,配成250mL溶液,取25.00mL上述溶液于锥形瓶中,加入足量的KI溶液充分反应,用0.04000mol/L硫代硫酸钠溶液滴定,消耗30.00mL硫代硫酸钠溶液,试求该产品的纯度
您最近一年使用:0次



