(1)常温下,0.05mol/L硫酸溶液中,c(H+)=_______ mol/L,pH值为_____ ,水电离的c(H+)=_______ mol/L
(2)某温度下,纯水中c(H+)=2×10-7mol/L,则纯水中c(OH-)=_________ mol/L,滴入盐酸使c(H+) =5×10-6mol/L,则c(OH-) =_________ mol/L
(2)某温度下,纯水中c(H+)=2×10-7mol/L,则纯水中c(OH-)=
11-12高二上·陕西咸阳·期中 查看更多[2]
更新时间:2011-11-14 15:02:35
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】某温度(t℃)时,测得0.01mol/L的NaOH溶液的pH为11,则该温度下水的Kw=________ ,该温度________ 25℃(填“大于”“小于”或“等于”),其理由是________________________________________________________________________ ;
此温度下,将pH=a的NaOH溶液Va L与pH=b的H2SO4溶液Vb L混合,通过计算填写以下不同情况时两溶液的体积比:
(1) 若所得溶液为中性,且a=12,b=2,则Va∶Vb=____________ ;
(2) 若所得溶液为中性,且a+b=12,则Va∶Vb=________ ;
(3) 若所得溶液的pH=10,且a=12,b=2,则Va∶Vb=______________ 。
此温度下,将pH=a的NaOH溶液Va L与pH=b的H2SO4溶液Vb L混合,通过计算填写以下不同情况时两溶液的体积比:
(1) 若所得溶液为中性,且a=12,b=2,则Va∶Vb=
(2) 若所得溶液为中性,且a+b=12,则Va∶Vb=
(3) 若所得溶液的pH=10,且a=12,b=2,则Va∶Vb=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)常温下0.01 mol·L-1HCl溶液:
①由水电离出的c(H+)=________ ;
②pH=________ ;
③加水稀释100倍,pH=________ 。
(2)常温下0.01 mol·L-1NaOH溶液:
①pH=________ ;
②加水稀释100倍,pH=________ 。
①由水电离出的c(H+)=
②pH=
③加水稀释100倍,pH=
(2)常温下0.01 mol·L-1NaOH溶液:
①pH=
②加水稀释100倍,pH=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)写出下列盐水解的离子方程式:
NaClO________________ 。
(NH4)2SO4________________ 。
Na2SO3________________ 。
AlCl3________________ 。
(2)25 ℃,将0.2 mol·L-1 HA溶液与0.2 mol·L-1 NaOH溶液等体积混合,测得混合溶液中c(Na+)>c(A-),则:(下列空白填“>”“<”或“=”)
①混合溶液中,c(HA)________ c(A-)。水电离产生的c(OH-) _____ 10-7 mol·L-1
②混合溶液中,c(HA)+c(A-)________ 0.1 mol·L-1。
③混合溶液中,由水电离出的c(OH-)___ 原0.2 mol·L-1 HA溶液中由水电离出的c(H+)。
④25 ℃时,如果取0.2 mol·L-1 HA溶液与0.1 mol·L-1 NaOH溶液等体积混合,测得混合溶液的pH<7,则HA的电离程度______ NaA的水解程度。
NaClO
(NH4)2SO4
Na2SO3
AlCl3
(2)25 ℃,将0.2 mol·L-1 HA溶液与0.2 mol·L-1 NaOH溶液等体积混合,测得混合溶液中c(Na+)>c(A-),则:(下列空白填“>”“<”或“=”)
①混合溶液中,c(HA)
②混合溶液中,c(HA)+c(A-)
③混合溶液中,由水电离出的c(OH-)
④25 ℃时,如果取0.2 mol·L-1 HA溶液与0.1 mol·L-1 NaOH溶液等体积混合,测得混合溶液的pH<7,则HA的电离程度
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】25℃时,有0.10mol·L 的下列4种溶液①氨水②盐酸③醋酸溶液④氢氧化钠溶液。
的下列4种溶液①氨水②盐酸③醋酸溶液④氢氧化钠溶液。
回答下列相关问题
(1)③中溶液的pH_____ 1(填“>”、“<”或“=”),请用电离方程式解释_____
(2)②中溶液的
_____ ,则溶液由水电离出的
_____ mol/L。②与④混合后 ,则盐酸和氢氧化钠体积比为
,则盐酸和氢氧化钠体积比为_____ 。
(3)向溶液①中加入等体积水稀释,稀释后溶液中的 比稀释前
比稀释前_____ (填“增大”“减小”或“不变”),原因_____ 。(用化学用语表示)
(4)25℃时,取20mL溶液③,向其中逐滴滴入溶液④,过程中pH随溶液④体积的变化如下图所示。下列说法正确的是_____ 。
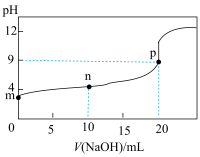
a.点m溶液中离子浓度关系: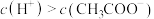
b.点n溶液中存在如下关系:
c.点p溶液反应的离子方程式:
d.点p溶液中,由水电离出的 是
是 mol⋅L
mol⋅L
 的下列4种溶液①氨水②盐酸③醋酸溶液④氢氧化钠溶液。
的下列4种溶液①氨水②盐酸③醋酸溶液④氢氧化钠溶液。回答下列相关问题
(1)③中溶液的pH
(2)②中溶液的


 ,则盐酸和氢氧化钠体积比为
,则盐酸和氢氧化钠体积比为(3)向溶液①中加入等体积水稀释,稀释后溶液中的
 比稀释前
比稀释前(4)25℃时,取20mL溶液③,向其中逐滴滴入溶液④,过程中pH随溶液④体积的变化如下图所示。下列说法正确的是

a.点m溶液中离子浓度关系:
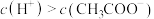
b.点n溶液中存在如下关系:

c.点p溶液反应的离子方程式:

d.点p溶液中,由水电离出的
 是
是 mol⋅L
mol⋅L
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】在不同温度下的水溶液中,c(H+)和c(OH-)的关系如图所示:

(1)A点水的离子积为_____________ ,C点水的离子积为_____________ ,对纯水由25℃升高温度至100℃时水的离子积__________ (填“增大”、“减小”或“不变”),各离子浓度由______ 点(填A、B、C、D)变为______ 点(填A、B、C、D)。
(2)100 ℃时,若向B点溶液中滴加硫酸,体系将由B点移向_____ 点(填C或D),为什么_____________________________________ 。
(3)25 ℃时,0.001mol/L的盐酸溶液pH=_______ ;0.001mol/L的氢氧化钠溶液pH=_________ ;若将二者温度都升高至100 ℃,________________ (填“盐酸”、“氢氧化钠”或“盐酸和氢氧化钠”)的pH会改变。

(1)A点水的离子积为
(2)100 ℃时,若向B点溶液中滴加硫酸,体系将由B点移向
(3)25 ℃时,0.001mol/L的盐酸溶液pH=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】室温下有5种稀溶液:①HCl、②H2SO4、③CH3COOH、④氨水、⑤NaOH,回答下列问题:
(1)若溶液①②③④⑤浓度均为0.01mol/L,pH由大到小的顺序是___________ 。(用序号填写,下同)
(2)中和等体积、pH相同的①②③溶液消耗NaOH最多的是___________ 。
(3)pH相同的④⑤溶液,则溶液的离子总浓度④___________ ⑤(填“>,<或=”)。
(4)常温下,pH=3的②溶液中水电离出的 ___________mol/L。
___________mol/L。
(1)若溶液①②③④⑤浓度均为0.01mol/L,pH由大到小的顺序是
(2)中和等体积、pH相同的①②③溶液消耗NaOH最多的是
(3)pH相同的④⑤溶液,则溶液的离子总浓度④
(4)常温下,pH=3的②溶液中水电离出的
 ___________mol/L。
___________mol/L。A.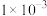 | B.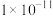 | C. | D. |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】测量家中一些物品(可自行增减、更换)的pH,并计算其c(H+),填入下表。
| 物品 | 醋 | 酱油 | 酒 | 洗涤灵 | “84”消毒液 | 洗发液 | 洁厕灵 | 洗衣液 | 柔软剂 |
| pH | |||||||||
| c(H+) |
您最近一年使用:0次

 的颜色是
的颜色是 固体中混有
固体中混有 的方法(用化学方程式表示)
的方法(用化学方程式表示)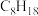 )完全燃烧生成液态水放出的热量为5518kJ(298K、
)完全燃烧生成液态水放出的热量为5518kJ(298K、 时测定)。写出该条件下,辛烷燃烧的热化学方程式
时测定)。写出该条件下,辛烷燃烧的热化学方程式 ,则柠檬水中
,则柠檬水中
 。
。


