25℃时,有0.10mol·L 的下列4种溶液①氨水②盐酸③醋酸溶液④氢氧化钠溶液。
的下列4种溶液①氨水②盐酸③醋酸溶液④氢氧化钠溶液。
回答下列相关问题
(1)③中溶液的pH_____ 1(填“>”、“<”或“=”),请用电离方程式解释_____
(2)②中溶液的
_____ ,则溶液由水电离出的
_____ mol/L。②与④混合后 ,则盐酸和氢氧化钠体积比为
,则盐酸和氢氧化钠体积比为_____ 。
(3)向溶液①中加入等体积水稀释,稀释后溶液中的 比稀释前
比稀释前_____ (填“增大”“减小”或“不变”),原因_____ 。(用化学用语表示)
(4)25℃时,取20mL溶液③,向其中逐滴滴入溶液④,过程中pH随溶液④体积的变化如下图所示。下列说法正确的是_____ 。
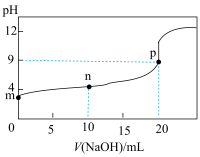
a.点m溶液中离子浓度关系: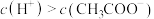
b.点n溶液中存在如下关系:
c.点p溶液反应的离子方程式:
d.点p溶液中,由水电离出的 是
是 mol⋅L
mol⋅L
 的下列4种溶液①氨水②盐酸③醋酸溶液④氢氧化钠溶液。
的下列4种溶液①氨水②盐酸③醋酸溶液④氢氧化钠溶液。回答下列相关问题
(1)③中溶液的pH
(2)②中溶液的


 ,则盐酸和氢氧化钠体积比为
,则盐酸和氢氧化钠体积比为(3)向溶液①中加入等体积水稀释,稀释后溶液中的
 比稀释前
比稀释前(4)25℃时,取20mL溶液③,向其中逐滴滴入溶液④,过程中pH随溶液④体积的变化如下图所示。下列说法正确的是

a.点m溶液中离子浓度关系:
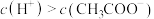
b.点n溶液中存在如下关系:

c.点p溶液反应的离子方程式:

d.点p溶液中,由水电离出的
 是
是 mol⋅L
mol⋅L
更新时间:2023-12-18 13:44:15
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】常温下,等体积、等pH的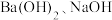 和
和 三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为
三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为 ,则三者的大小关系为
,则三者的大小关系为________ 。
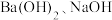 和
和 三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为
三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为 ,则三者的大小关系为
,则三者的大小关系为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】水溶液中的离子反应在许多领域都有广泛的应用,请回答下列问题。
(1)在配制氯化铁溶液时,常常会出现浑浊,可以加入少量的__________ 防止上述问题。
(2)明矾具有净水的作用,原因是:___________________________ (用离子方程式表示)。
(3)将25 ℃时pH=12的NaOH溶液a L与pH=1的HCl溶液b L混合。若所得混合液为中性,则a∶b=______________ 。
(4)加热蒸干AlCl3溶液并灼烧所得固体,最终得到的产物是______________
(5)常温下,已知Ksp[M(OH)3] =1.0×10−38,要使溶液中的M3+降至10−5mol/L,则应调节溶液pH=________ 。
(1)在配制氯化铁溶液时,常常会出现浑浊,可以加入少量的
(2)明矾具有净水的作用,原因是:
(3)将25 ℃时pH=12的NaOH溶液a L与pH=1的HCl溶液b L混合。若所得混合液为中性,则a∶b=
(4)加热蒸干AlCl3溶液并灼烧所得固体,最终得到的产物是
(5)常温下,已知Ksp[M(OH)3] =1.0×10−38,要使溶液中的M3+降至10−5mol/L,则应调节溶液pH=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
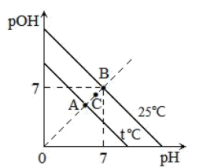
【推荐1】已知pOH也可以用来表示溶液的酸碱度,规定pOH=−lgc平(OH-)。不同温度下,水溶液中pOH与pH的关系如图所示。
回答下列问题:
(1)t___________ 25(填“>”或“<”),图中A、B、C三点对应水的电离程度由大到小的顺序是___________ 。
(2)25℃时,向 溶液中逐滴加入等浓度的
溶液中逐滴加入等浓度的 溶液至
溶液至 恰好沉淀完全。
恰好沉淀完全。
①此过程中水的电离平衡___________ (填“正向”、“逆向”或“不”)移动。
②写出该过程发生反应的离子方程式___________ ;若反应前后溶液体积的变化忽略不计,则反应后所得溶液的pH值为___________ (已知 )。
)。
(3)已知80℃时,水的离子积常数 。该温度下,0.1mol/L某一元酸(HA)溶液中
。该温度下,0.1mol/L某一元酸(HA)溶液中 ,该溶液中由水电离的c平(H+)为
,该溶液中由水电离的c平(H+)为___________ ,用电离方程式表示该溶液中存在的电离平衡___________ 。

回答下列问题:
(1)t
(2)25℃时,向
 溶液中逐滴加入等浓度的
溶液中逐滴加入等浓度的 溶液至
溶液至 恰好沉淀完全。
恰好沉淀完全。①此过程中水的电离平衡
②写出该过程发生反应的离子方程式
 )。
)。(3)已知80℃时,水的离子积常数
 。该温度下,0.1mol/L某一元酸(HA)溶液中
。该温度下,0.1mol/L某一元酸(HA)溶液中 ,该溶液中由水电离的c平(H+)为
,该溶液中由水电离的c平(H+)为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】已知水在25 ℃和95 ℃时,其电离平衡曲线如图所示:
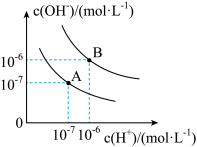
(1)25 ℃时水的电离平衡曲线应为___________ (填“A”或“B”),请说明理由_________________ 。25 ℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为___________ 。
(2)95 ℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则a与b之间满足的关系是___________ 。
(3)曲线A所对应的温度下,pH=2的HCl溶液和pH=11的某BOH溶液中,若水的电离程度分别用γ1、γ2表示,则γ1___________ (填“大于”“小于”“等于”或“无法确定”)γ2。

(1)25 ℃时水的电离平衡曲线应为
(2)95 ℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则a与b之间满足的关系是
(3)曲线A所对应的温度下,pH=2的HCl溶液和pH=11的某BOH溶液中,若水的电离程度分别用γ1、γ2表示,则γ1
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】下表是25℃时三种弱酸的电离平衡常数
(1)用离子方程式表示NaNO2溶液呈碱性的原因__________ 。
(2)NaHCO3的电离方程式是____________ 。
(3)A-、CO 、HCO
、HCO 在水中结合H+的能力由大到小的顺序为
在水中结合H+的能力由大到小的顺序为____________ 。
(4)写出NaA溶液中通少量CO2的离子方程式________________ 。
(5)某同学用Na2CO3和NaHCO3溶液进行如下图所示实验。
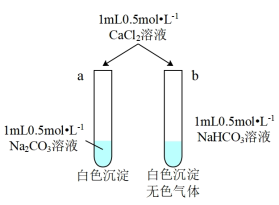
①充分反应后a试管中大量存在的离子是__________ 。
②用离子方程式表示b试管中发生的反应__________ 。
| 化学式 | HA(A代表某种酸根) | HNO2 | H2CO3 |
| Ka | Ka=4.910-10 | Ka=4.610-4 | Ka1=4.110-7 Ka2=5.610-11 |
(1)用离子方程式表示NaNO2溶液呈碱性的原因
(2)NaHCO3的电离方程式是
(3)A-、CO
 、HCO
、HCO 在水中结合H+的能力由大到小的顺序为
在水中结合H+的能力由大到小的顺序为(4)写出NaA溶液中通少量CO2的离子方程式
(5)某同学用Na2CO3和NaHCO3溶液进行如下图所示实验。

①充分反应后a试管中大量存在的离子是
②用离子方程式表示b试管中发生的反应
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】请回答下列问题:
(1)在常温常压下, 完全燃烧生成液态水,放出142.9kJ热量。则
完全燃烧生成液态水,放出142.9kJ热量。则 燃烧热的热化学方程式为
燃烧热的热化学方程式为___________ 。
(2)25℃时将 的稀硫酸
的稀硫酸 与
与 的苛性钠溶液
的苛性钠溶液 混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的
混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的 ,则
,则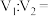
___________ 。
(3)浓度均为 的盐酸和
的盐酸和 溶液各1mL,加入等体积的水稀释后则
溶液各1mL,加入等体积的水稀释后则
___________ 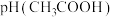 (填“>”或“<”或“=”)。
(填“>”或“<”或“=”)。
(4)根据下表提供的数据,写出往 溶液中通入少量
溶液中通入少量 的离子方程式
的离子方程式___________ 。
(1)在常温常压下,
 完全燃烧生成液态水,放出142.9kJ热量。则
完全燃烧生成液态水,放出142.9kJ热量。则 燃烧热的热化学方程式为
燃烧热的热化学方程式为(2)25℃时将
 的稀硫酸
的稀硫酸 与
与 的苛性钠溶液
的苛性钠溶液 混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的
混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的 ,则
,则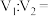
(3)浓度均为
 的盐酸和
的盐酸和 溶液各1mL,加入等体积的水稀释后则
溶液各1mL,加入等体积的水稀释后则
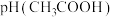 (填“>”或“<”或“=”)。
(填“>”或“<”或“=”)。(4)根据下表提供的数据,写出往
 溶液中通入少量
溶液中通入少量 的离子方程式
的离子方程式| 化学式 | 电离常数 |
 | 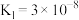 |
 |   |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】常温下,有0.1 mol∙L−1的四种溶液:
①NaOH ②Na2CO3 ③NaHSO4 ④NH4Cl
(1)任选上述一种酸性溶液,用化学用语解释其呈酸性的原因:___________ 。
(2)溶液①中由水电离出的氢氧根浓度为___________ 。
(3)溶液①、③等体积混合后,溶液中c(H+)___________ c(OH-)(填“>”、“<”或“=”)。
(4)溶液④中各离子浓度从大到小的顺序是___________ 。
(5)热的②溶液可以去油污,原因是___________ (用化学用语解释)
①NaOH ②Na2CO3 ③NaHSO4 ④NH4Cl
(1)任选上述一种酸性溶液,用化学用语解释其呈酸性的原因:
(2)溶液①中由水电离出的氢氧根浓度为
(3)溶液①、③等体积混合后,溶液中c(H+)
(4)溶液④中各离子浓度从大到小的顺序是
(5)热的②溶液可以去油污,原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】I.根据表中数据(常温下),完成下列填空。
(1)常温下,NaCN溶液呈____ (填“酸”、“碱”或“中”)性,其原因是____ (用离子方程式表示)。
(2)常温下,浓度均为0.1 mol∙L−1的下列4种溶液:①CH3COONa溶液,②NaCN溶液,③NaHCO3溶液,④NaClO溶液;这4种溶液pH由大到小的顺序是____ (填序号)。
(3)常温下,向NaClO溶液中通入少量CO2,发生反应的离子方程式为____ 。
(4)常温下,Na2SO3溶液中c(OH-)−c(H+)=c(HSO )+
)+____ 。
II.我国《生活饮用水卫生标准》中规定生活用水中镉的排放量不超过0.005mg∙L−1。处理含镉废水可采用化学沉淀法。Ksp(CdCO3)=4.0×10−12,Ksp(CdS)=8.0×10−27;回答下列问题:
(5)向某含镉废水中加入Na2S,当S2−浓度达到8.0×10−8 mol∙L−1时,废水中Cd2+的浓度为____ mol∙L−1,此时是否符合生活饮用水卫生标准?____ (填“是”或“否”)。
(6)室温下,反应CdCO3(s)+S2−(aq) CdS(s)+CO
CdS(s)+CO (aq)达到平衡,该反应的平衡常数K=
(aq)达到平衡,该反应的平衡常数K=____ (结果保留两位有效数字)
| 物质 | CH3COOH | NH3∙H2O | HCN | HClO | H2CO3 | H2SO3 |
| 电离常数(Ka) | 1.7×10−5 | 1.7×10−5 | 4.9×10−10 | 3×10−8 | Ka1=4.3×10−7 Ka2=5.6×10−11 | Ka1=1.5×10−2 Ka2=1.0×10−7 |
(2)常温下,浓度均为0.1 mol∙L−1的下列4种溶液:①CH3COONa溶液,②NaCN溶液,③NaHCO3溶液,④NaClO溶液;这4种溶液pH由大到小的顺序是
(3)常温下,向NaClO溶液中通入少量CO2,发生反应的离子方程式为
(4)常温下,Na2SO3溶液中c(OH-)−c(H+)=c(HSO
 )+
)+II.我国《生活饮用水卫生标准》中规定生活用水中镉的排放量不超过0.005mg∙L−1。处理含镉废水可采用化学沉淀法。Ksp(CdCO3)=4.0×10−12,Ksp(CdS)=8.0×10−27;回答下列问题:
(5)向某含镉废水中加入Na2S,当S2−浓度达到8.0×10−8 mol∙L−1时,废水中Cd2+的浓度为
(6)室温下,反应CdCO3(s)+S2−(aq)
 CdS(s)+CO
CdS(s)+CO (aq)达到平衡,该反应的平衡常数K=
(aq)达到平衡,该反应的平衡常数K=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】氧族元素及其化合物在生产、生活中发挥着重要的作用。回答下列问题:
(1)工业上常用硫化物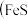 等
等 作沉淀剂除去废水中的
作沉淀剂除去废水中的 等重金属离子。已知常温下
等重金属离子。已知常温下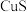 饱和溶液中,
饱和溶液中,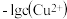 和
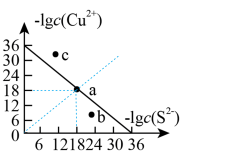
和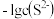 关系如图所示,
关系如图所示,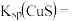
___________ ;图中a、b、c三点对应的溶液中,一定存在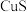 沉淀的是
沉淀的是___________ (填字母)。
(2)工业上将含硒工业废料处理得到亚硒酸 和硒酸
和硒酸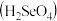 ,进而制备单质硒。亚硒酸
,进而制备单质硒。亚硒酸 在溶液中存在多种微粒形态,
在溶液中存在多种微粒形态, 时各微粒的分布系数
时各微粒的分布系数 与溶液
与溶液 的关系如图所示。(分布系数即各组分的平衡浓度占总浓度的分数)
的关系如图所示。(分布系数即各组分的平衡浓度占总浓度的分数)
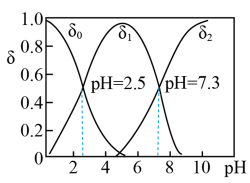
①将 溶液滴入
溶液滴入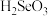 溶液中,当
溶液中,当 时发生反应的离子方程式为
时发生反应的离子方程式为___________ 。
②由图可知, 时
时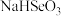 溶液的pH
溶液的pH___________ 7。
③已知硒酸的电离方程式为: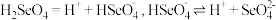 。
。 时,下列关于
时,下列关于 溶液的说法错误的是
溶液的说法错误的是___________ 。
A.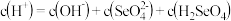
B.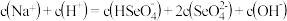
C.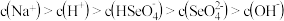
D. 溶液一定呈酸性
溶液一定呈酸性
(1)工业上常用硫化物
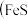 等
等 作沉淀剂除去废水中的
作沉淀剂除去废水中的 等重金属离子。已知常温下
等重金属离子。已知常温下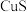 饱和溶液中,
饱和溶液中,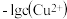 和
和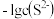 关系如图所示,
关系如图所示,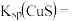
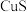 沉淀的是
沉淀的是
(2)工业上将含硒工业废料处理得到亚硒酸
 和硒酸
和硒酸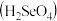 ,进而制备单质硒。亚硒酸
,进而制备单质硒。亚硒酸 在溶液中存在多种微粒形态,
在溶液中存在多种微粒形态, 时各微粒的分布系数
时各微粒的分布系数 与溶液
与溶液 的关系如图所示。(分布系数即各组分的平衡浓度占总浓度的分数)
的关系如图所示。(分布系数即各组分的平衡浓度占总浓度的分数)
①将
 溶液滴入
溶液滴入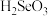 溶液中,当
溶液中,当 时发生反应的离子方程式为
时发生反应的离子方程式为②由图可知,
 时
时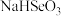 溶液的pH
溶液的pH③已知硒酸的电离方程式为:
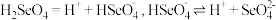 。
。 时,下列关于
时,下列关于 溶液的说法错误的是
溶液的说法错误的是A.
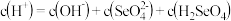
B.
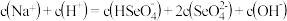
C.
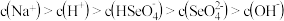
D.
 溶液一定呈酸性
溶液一定呈酸性
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】在一定温度下,有三种酸溶液:a、盐酸 b、硫酸 c、醋酸。
(1)若三者溶液pH相同时,溶质的物质的量浓度由大到小的顺序是___________ (用a、b、c填空,下同)。
(2)若三者溶液同体积、同物质的量浓度时,溶液中 由大到小的顺序是
由大到小的顺序是___________ ,中和上述三种酸,消耗NaOH的物质的量由大到小的顺序是___________ 。
(3)若将pH相同的三种酸均加水稀释至原来的100倍后, 由大到小的顺序是
由大到小的顺序是___________ 。
(4)在0.2 与0.1
与0.1 醋酸中,
醋酸中, 之比为
之比为___________ 2∶1(填>、<、=)。
(5)在0.1 醋酸溶液中,
醋酸溶液中,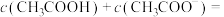
___________  (填数值)。
(填数值)。
(1)若三者溶液pH相同时,溶质的物质的量浓度由大到小的顺序是
(2)若三者溶液同体积、同物质的量浓度时,溶液中
 由大到小的顺序是
由大到小的顺序是(3)若将pH相同的三种酸均加水稀释至原来的100倍后,
 由大到小的顺序是
由大到小的顺序是(4)在0.2
 与0.1
与0.1 醋酸中,
醋酸中, 之比为
之比为(5)在0.1
 醋酸溶液中,
醋酸溶液中,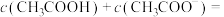
 (填数值)。
(填数值)。
您最近一年使用:0次



