硅及其化合物有许多用途,回答下列问题:
(1)基态Si原子价层电子的排布图(轨道表达式)为_________ ,含有长硅链的化合物不是氢化物,而是氯化物。主要原因是F比H多了一种形状的原子轨道,该原子轨道的形状为___________ 。
(2)SiF4分子的立体构型为_______ 形,SiCl4的熔、沸点均高于SiF4,主要原因是________________ 。
(3)SiF4可KF反应得K2SiF6晶体,该晶体可用于制取高纯硅,K2SiF6晶体中微观粒子之间的作用力有______ 。
a.离子键 b.共价键 c.配位键 d.分子间作用力 e.氢键

(4)H4SiO4的结构简式如图(1),中心原子Si的轨道杂化类型为_________ ,H4SiO4在常温下能稳定存在,但H4CO4不能,会迅速脱水生成H2CO3,最终生成CO2,主要原因是___________ 。
(5)硅的晶胞结构如图(2)所示,若该立方晶胞的边长为a nm,阿伏伽德罗常数的数值为NA,则距离最近的两个硅原子间的距离为_____ nm,晶体硅密度的计算表达式为_____ g/cm3。
(1)基态Si原子价层电子的排布图(轨道表达式)为
(2)SiF4分子的立体构型为
(3)SiF4可KF反应得K2SiF6晶体,该晶体可用于制取高纯硅,K2SiF6晶体中微观粒子之间的作用力有
a.离子键 b.共价键 c.配位键 d.分子间作用力 e.氢键

(4)H4SiO4的结构简式如图(1),中心原子Si的轨道杂化类型为
(5)硅的晶胞结构如图(2)所示,若该立方晶胞的边长为a nm,阿伏伽德罗常数的数值为NA,则距离最近的两个硅原子间的距离为
更新时间:2019-04-26 15:16:33
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A~D 是原子序数在 20 以内的元素,其性质或结构信息如下表:

请根据表中的信息回答下列问题:
(1)C 离子的结构示意图:_____________ ,B 原子的电子式:______________ 。
(2)写出和 B 的氢化物所含电子数相同的 3 种复杂微粒,这三种微粒分别是: 阴离子:_____ ,阳离子____________ ,电中性微粒:_____________ 。
(3)A 元素与 D 元素组成的化合物有非常重要的用途,写出实验室制备该气体的化学方程式:______________ 。

请根据表中的信息回答下列问题:
(1)C 离子的结构示意图:
(2)写出和 B 的氢化物所含电子数相同的 3 种复杂微粒,这三种微粒分别是: 阴离子:
(3)A 元素与 D 元素组成的化合物有非常重要的用途,写出实验室制备该气体的化学方程式:
您最近一年使用:0次
【推荐2】W、X、Y、Z四种短周期元素的原子序数W>X>Z>Y。X原子的最外层没有p电子,Y原子最外层s电子与p电子数之比为1∶1,W与Z原子核外s电子与p电子数之比均为1∶1。则:
(1)写出各元素的元素符号:W:________ 、X:________ 、Y:________ 、Z:________ 。
(2)四种元素原子半径大小顺序依次为____________________________________ 。
(3)W、X元素最高价氧化物对应水化物的碱性强弱为________________________ (用化学式表示)。
(1)写出各元素的元素符号:W:
(2)四种元素原子半径大小顺序依次为
(3)W、X元素最高价氧化物对应水化物的碱性强弱为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】X、T、Y、Z为1﹣36号元素,且原子序数依次增大,四种元素的性质或结构信息如表。请根据信息回答下列问题。
(1)写出元素T的离子结构示意图___________ ;写出元素X的气态氢化物的电子式___________ ;写出Z元素原子的外围电子排布式___________ ;元素Y的原子核外共有___________ 种形状不同的电子云。
(2)Y元素原子的第一电离能___________ 镁(填“>”“<”“=”),从结构上分析,其理由是:___________ 。
(3)元素T与氟元素相比,非金属性较强的是___________ (用元素符号表示),下列表述中能证明这一事实的是___________ (填序号字母)。
a.常温下氟气的颜色比T单质的颜色深
b.氟气与T的氢化物剧烈反应,产生T的单质
c.氟与T形成的化合物中T元素呈正价态
d.比较两元素的单质与氢气化合时得电子的数目
| 元素 | T | X | Y | Z |
| 性质结构信息 | 人体内含量最多的元素,且其单质是最常见的助燃剂。 | 单质为双原子分子,分子中含有3对共用电子对,常温下单质性质稳定,但其原子较活泼。 | 第3周期元素的简单离子中半径最小。 | 第4周期元素,M电子层为全充满状态,最外层只有二个电子的原子。 |
(2)Y元素原子的第一电离能
(3)元素T与氟元素相比,非金属性较强的是
a.常温下氟气的颜色比T单质的颜色深
b.氟气与T的氢化物剧烈反应,产生T的单质
c.氟与T形成的化合物中T元素呈正价态
d.比较两元素的单质与氢气化合时得电子的数目
您最近一年使用:0次
【推荐1】I 锰元素的化合物在多个领域中均有重要应用。
(1)Mn2+基态核外电子排布式为___ ,SO32-分子的空间构型为____ 。
(2)二价锰的3种离子化合物MnCl2、MnS、MnO中晶格能最大的是___ 。
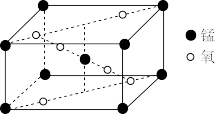
(3)某锰氧化物的晶胞结构如图所示,该氧化物的化学式为___ 。
(4)在配离子[Mn(CN)6]3-中存在的作用力有___ (填字母)。
a. 离子键 b. 共价键 c. 配位键 d. 氢键
II 铜是人类最早使用的金属之一,铜的化合物丰富多彩。
(1)铜与N2O4在一定条件下可制备无水Cu(NO3)2。
①基态Cu的电子排布式为___ 。
②与NO3-互为等电子体的一种分子为__ (填化学式)。
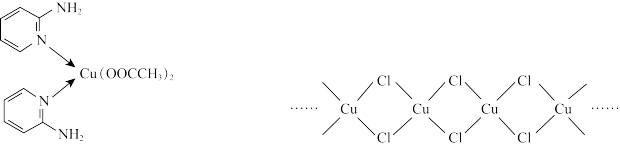
(2)邻氨基吡啶(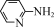 )的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。
)的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。
①C、N、O三种元素的第一电离能由大到小的顺序为___ 。
②邻氨基吡啶的铜配合物中,C原子轨道杂化类型为___ 。
③1mol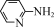 中含有σ键的数目为
中含有σ键的数目为___ mol。
(1)Mn2+基态核外电子排布式为
(2)二价锰的3种离子化合物MnCl2、MnS、MnO中晶格能最大的是
(3)某锰氧化物的晶胞结构如图所示,该氧化物的化学式为

(4)在配离子[Mn(CN)6]3-中存在的作用力有
a. 离子键 b. 共价键 c. 配位键 d. 氢键
II 铜是人类最早使用的金属之一,铜的化合物丰富多彩。
(1)铜与N2O4在一定条件下可制备无水Cu(NO3)2。
①基态Cu的电子排布式为
②与NO3-互为等电子体的一种分子为
(2)邻氨基吡啶(
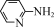 )的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。
)的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。
①C、N、O三种元素的第一电离能由大到小的顺序为
②邻氨基吡啶的铜配合物中,C原子轨道杂化类型为
③1mol
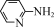 中含有σ键的数目为
中含有σ键的数目为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐2】贝凡洛尔是一种用于治疗高血压的药物,其中间体F的一种合成路线如下:
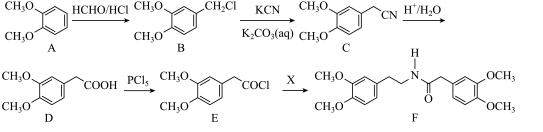
(1)B中官能团名称为_______ 。
(2)A→B的反应中有一种分子式为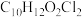 的副产物生成,该副产物的结构简式为
的副产物生成,该副产物的结构简式为_______ 。
(3)在Ni催化下C与 反应可得X,X的分子式为
反应可得X,X的分子式为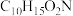 。C→X的反应中,—CN中碳原子的杂化轨道类型变化为
。C→X的反应中,—CN中碳原子的杂化轨道类型变化为_______ 。
(4)写出同时满足下列条件的E的一种同分异构体的结构简式_______ 。
①属于芳香化合物,能发生银镜反应;
②碱性条件下水解,含有苯环的产物分子中只有3种不同化学环境的氢。
(5)请以 和HCN为原料制备
和HCN为原料制备 ,写出该制备的合成路线流程图(其他无机试剂任用,合成路线流程图示例见本题题干)。
,写出该制备的合成路线流程图(其他无机试剂任用,合成路线流程图示例见本题题干)。_______

(1)B中官能团名称为
(2)A→B的反应中有一种分子式为
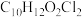 的副产物生成,该副产物的结构简式为
的副产物生成,该副产物的结构简式为(3)在Ni催化下C与
 反应可得X,X的分子式为
反应可得X,X的分子式为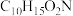 。C→X的反应中,—CN中碳原子的杂化轨道类型变化为
。C→X的反应中,—CN中碳原子的杂化轨道类型变化为(4)写出同时满足下列条件的E的一种同分异构体的结构简式
①属于芳香化合物,能发生银镜反应;
②碱性条件下水解,含有苯环的产物分子中只有3种不同化学环境的氢。
(5)请以
 和HCN为原料制备
和HCN为原料制备 ,写出该制备的合成路线流程图(其他无机试剂任用,合成路线流程图示例见本题题干)。
,写出该制备的合成路线流程图(其他无机试剂任用,合成路线流程图示例见本题题干)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】 广泛应用于太阳能电池领域,可以
广泛应用于太阳能电池领域,可以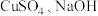 和抗坏血酸为原料制备
和抗坏血酸为原料制备 。
。
(1) 基态核外电子排布式为
基态核外电子排布式为_______ 。
(2)向 溶液中逐滴加入过量氨水,先产生蓝色沉淀后沉淀溶解变成蓝色溶液,生成
溶液中逐滴加入过量氨水,先产生蓝色沉淀后沉淀溶解变成蓝色溶液,生成 ,此过程涉及的离子方程式为
,此过程涉及的离子方程式为_______ ;形成的配合物 中的中心离子是
中的中心离子是_______ ,配体是_______ ,配位数是_______ 。
(3)图1分子中碳原子的轨道杂化类型为_______ 和_______ 。
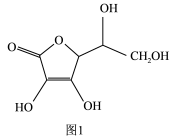
(4)一个 晶胞(见图2)中,氧离子的数目为
晶胞(见图2)中,氧离子的数目为_______ 。

 广泛应用于太阳能电池领域,可以
广泛应用于太阳能电池领域,可以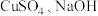 和抗坏血酸为原料制备
和抗坏血酸为原料制备 。
。(1)
 基态核外电子排布式为
基态核外电子排布式为(2)向
 溶液中逐滴加入过量氨水,先产生蓝色沉淀后沉淀溶解变成蓝色溶液,生成
溶液中逐滴加入过量氨水,先产生蓝色沉淀后沉淀溶解变成蓝色溶液,生成 ,此过程涉及的离子方程式为
,此过程涉及的离子方程式为 中的中心离子是
中的中心离子是(3)图1分子中碳原子的轨道杂化类型为

(4)一个
 晶胞(见图2)中,氧离子的数目为
晶胞(见图2)中,氧离子的数目为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】某大学教授课题研究组首次合成了石墨二炔—氧化铟(GDY—IO)纳米复合材料,并将其应用于气相光催化还原 制得
制得 碳氢化合物。
碳氢化合物。______ 。
(2)石墨二炔可以被看作是石墨烯中三分之一的C—C中插入两个 (二炔或乙炔)键,石墨二炔(GDY)中C原子的杂化轨道类型有
(二炔或乙炔)键,石墨二炔(GDY)中C原子的杂化轨道类型有______ 。
(3)石墨能与熔融金属钾作用,形成石墨间隙化合物,钾原子填充在石墨各层原子中。较常见的石墨间隙化合物是青铜色的化合物,其化学式可写为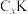 ,其平面图形如图1所示,x的值为
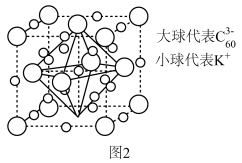
,其平面图形如图1所示,x的值为______ ;在石墨片层结构中,碳原子、C—C键、六元环的个数之比为______ 。 易与铁触媒作用导致其失去催化活性:
易与铁触媒作用导致其失去催化活性: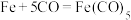 ,
, 又名羟基铁,常温下为黄色油状液体,则
又名羟基铁,常温下为黄色油状液体,则 的晶体类型是
的晶体类型是______ 。
(5)乙烯分子中碳碳双键与碳氢键间的键角大于碳氢键之间的键角,原因是____________ 。
(6)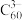 与
与 能形成图2中的超分子加合物,已知晶胞参数为
能形成图2中的超分子加合物,已知晶胞参数为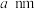 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶胞的密度为
,则该晶胞的密度为______  (列出计算表达式)。
(列出计算表达式)。
 制得
制得 碳氢化合物。
碳氢化合物。
(2)石墨二炔可以被看作是石墨烯中三分之一的C—C中插入两个
 (二炔或乙炔)键,石墨二炔(GDY)中C原子的杂化轨道类型有
(二炔或乙炔)键,石墨二炔(GDY)中C原子的杂化轨道类型有(3)石墨能与熔融金属钾作用,形成石墨间隙化合物,钾原子填充在石墨各层原子中。较常见的石墨间隙化合物是青铜色的化合物,其化学式可写为
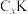 ,其平面图形如图1所示,x的值为
,其平面图形如图1所示,x的值为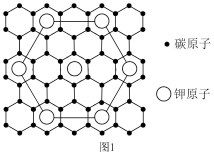
 易与铁触媒作用导致其失去催化活性:
易与铁触媒作用导致其失去催化活性: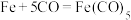 ,
, 又名羟基铁,常温下为黄色油状液体,则
又名羟基铁,常温下为黄色油状液体,则 的晶体类型是
的晶体类型是(5)乙烯分子中碳碳双键与碳氢键间的键角大于碳氢键之间的键角,原因是
(6)
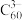 与
与 能形成图2中的超分子加合物,已知晶胞参数为
能形成图2中的超分子加合物,已知晶胞参数为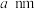 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶胞的密度为
,则该晶胞的密度为 (列出计算表达式)。
(列出计算表达式)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】锡酸钠 在电镀、印染、纺织、陶瓷等工业中具有重要作用。一种以含铅、锑、锡的复合渣(主要成分为
在电镀、印染、纺织、陶瓷等工业中具有重要作用。一种以含铅、锑、锡的复合渣(主要成分为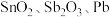 及
及 等)为原料制备锡酸钠晶体
等)为原料制备锡酸钠晶体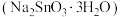 的工艺流程如下:
的工艺流程如下:
②锡酸钠晶体易溶于水,难溶于乙醇。
回答下列问题:
(1) 元素在周期表中的位置为
元素在周期表中的位置为___________ 。
(2)“高温真空蒸发”控制温度在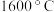 左右,目的是
左右,目的是___________ 。
(3)“高温碱熔”时,单质 与
与 和
和 反应生成
反应生成 的化学方程式为
的化学方程式为___________ 。
(4)已知“溶浸”后溶液中的阴离子主要为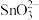 和少量
和少量 ,“沉铅”时发生反应的离子方程式为
,“沉铅”时发生反应的离子方程式为___________ 。
(5)获得锡酸钠晶体的“系列操作”是蒸发浓缩、冷却结晶、过滤、___________ (填试剂名称)洗涤、___________ (填“低温”或“高温”)干燥。
(6)利用焦炭在 高温下还原
高温下还原 可制得单质
可制得单质 。
。 存在白锡、灰锡和脆锡三种同素异形体,其中灰锡的晶体结构与金刚石相似。若晶胞参数为
存在白锡、灰锡和脆锡三种同素异形体,其中灰锡的晶体结构与金刚石相似。若晶胞参数为 ,则最近的两个锡原子间的距离为
,则最近的两个锡原子间的距离为___________  。
。
 在电镀、印染、纺织、陶瓷等工业中具有重要作用。一种以含铅、锑、锡的复合渣(主要成分为
在电镀、印染、纺织、陶瓷等工业中具有重要作用。一种以含铅、锑、锡的复合渣(主要成分为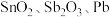 及
及 等)为原料制备锡酸钠晶体
等)为原料制备锡酸钠晶体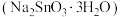 的工艺流程如下:
的工艺流程如下: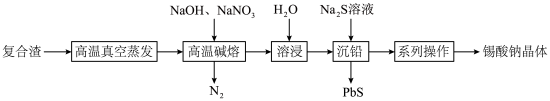
| 物质 |  |  |  |  |
沸点 | 1800 | 2260 | 1550 | 1740 |
回答下列问题:
(1)
 元素在周期表中的位置为
元素在周期表中的位置为(2)“高温真空蒸发”控制温度在
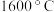 左右,目的是
左右,目的是(3)“高温碱熔”时,单质
 与
与 和
和 反应生成
反应生成 的化学方程式为
的化学方程式为(4)已知“溶浸”后溶液中的阴离子主要为
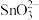 和少量
和少量 ,“沉铅”时发生反应的离子方程式为
,“沉铅”时发生反应的离子方程式为(5)获得锡酸钠晶体的“系列操作”是蒸发浓缩、冷却结晶、过滤、
(6)利用焦炭在
 高温下还原
高温下还原 可制得单质
可制得单质 。
。 存在白锡、灰锡和脆锡三种同素异形体,其中灰锡的晶体结构与金刚石相似。若晶胞参数为
存在白锡、灰锡和脆锡三种同素异形体,其中灰锡的晶体结构与金刚石相似。若晶胞参数为 ,则最近的两个锡原子间的距离为
,则最近的两个锡原子间的距离为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】I.含VIA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
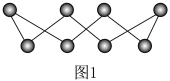
(1)S单质的常见形式为S8,其环状结构如图1所示,S原子采用的轨道杂化方式是_____ 。
(2)H2SeO4比H2SeO3酸性强的原因:_________ 。
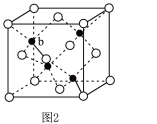
(3)ZnS在光导体材料、荧光体、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如图2所示,其晶胞边长为a pm,密度为______ g⋅cm−3。(用含a和NA的表达式填空)
II.氮及其化合物与人类生产、生活息息相关。化肥(NH4)2SO4中会含有N4H4(SO4)2,该物质在水中电离出SO42-和N4H44+,N4H44+遇到碱性溶液会生成一种形似白磷(P4)的N4分子。请回答下列问题:
(4)N4分子中的氮氮键的键角为____ ,1molN4分子中含有的氮氮键的数目为____ 。
(5)N4比P4的沸点____ (填“高”或“低”),原因为________ 。
(1)S单质的常见形式为S8,其环状结构如图1所示,S原子采用的轨道杂化方式是

(2)H2SeO4比H2SeO3酸性强的原因:
(3)ZnS在光导体材料、荧光体、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如图2所示,其晶胞边长为a pm,密度为

II.氮及其化合物与人类生产、生活息息相关。化肥(NH4)2SO4中会含有N4H4(SO4)2,该物质在水中电离出SO42-和N4H44+,N4H44+遇到碱性溶液会生成一种形似白磷(P4)的N4分子。请回答下列问题:
(4)N4分子中的氮氮键的键角为
(5)N4比P4的沸点
您最近一年使用:0次



