硫酸工业中废渣的成分为SiO2、Fe2O3、Al2O3、MgO。 某探究性学习小组的同学设计以下实验方案,将硫酸渣中金属元素分别转化为氢氧化物沉淀而分离开来。
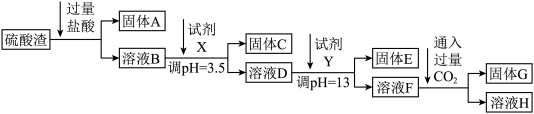
已知常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
(1)工业上用固体A作原料制取水玻璃的化学方程式为_______ 。
(2)固体E的化学式为_______ 。
(3)实验室用11.9mol/L的浓盐酸配制250mL3.0mol/L的稀盐酸,所用的玻璃仪器除烧杯、玻璃棒和量筒外,还需要_______ 。
(4)上述流程中的试剂Y最好选用下列中的_______ (选填字母编号)。
A.水 B.硫酸 C.氨水 D.氢氧化钠
(5)写出反应F→H的离子方程式_______ 。

已知常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
| 阳离子 | Fe3+ | Al3+ | Mg2+ |
| 开始沉淀时pH | 1.9 | 3.7 | 9.6 |
| 完全沉淀时pH | 3.2 | 5.2 | 11.0 |
(2)固体E的化学式为
(3)实验室用11.9mol/L的浓盐酸配制250mL3.0mol/L的稀盐酸,所用的玻璃仪器除烧杯、玻璃棒和量筒外,还需要
(4)上述流程中的试剂Y最好选用下列中的
A.水 B.硫酸 C.氨水 D.氢氧化钠
(5)写出反应F→H的离子方程式
更新时间:2019-05-26 10:37:18
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】锂在新能源等领域应用广泛。从粉煤灰(含Al2O3、Fe2O3、Li2O、SiO2等)中回收提取铝、锂元素的化合物的流程如图所示:

已知:碳酸锂的溶解度(g·L-1)见表。
回答下列问题
(1)“粉碎”的目的是___________ ,滤渣1的成分主要是___________ 。(填化学式)
(2)“调pH”的目的是沉淀Fe3+、Al3+。当离子浓度≤1.0×10-5mol·L-1时表示该离子沉淀完全。常温下,如果溶液pH=4,Fe3+、Al3+___________ (填“能”或“否”)均沉淀完全,此时溶液中c(Fe3+)、c(Al3+)之比为___________ 。(已知:Ksp[Fe(OH)3]=8.0×10-38,Ksp[Al(OH)3]=2.0×10-33)
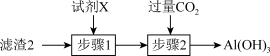
(3)从滤渣2中分离出Al(OH)3,可用如图所示方法,试剂X是___________ ,“步骤2”中主要发生的离子反应方程式有OH-+CO2=HCO 、
、___________ 。
(4)“沉锂”中的“一系列操作”依次为蒸发浓缩、___________ 、洗涤、干燥。检验母液主要溶质的阴离子所用的试剂为___________ 。母液的用途___________ (任写一种)。
(5)太阳能路灯蓄电池是磷酸铁锂电池,其工作原理如图所示。电池总反应式为LixC6 + Li1−xFePO4 LiFePO4 + 6C。试写出充电时,该电池正极材料上的反应式:
LiFePO4 + 6C。试写出充电时,该电池正极材料上的反应式:___________ 。


已知:碳酸锂的溶解度(g·L-1)见表。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
| Li2CO3 | 1.54 | 1.43 | 1.33 | 1.25 | 1.17 | 1.08 | 1.01 | 0.85 | 0.72 |
(1)“粉碎”的目的是
(2)“调pH”的目的是沉淀Fe3+、Al3+。当离子浓度≤1.0×10-5mol·L-1时表示该离子沉淀完全。常温下,如果溶液pH=4,Fe3+、Al3+
(3)从滤渣2中分离出Al(OH)3,可用如图所示方法,试剂X是
 、
、
(4)“沉锂”中的“一系列操作”依次为蒸发浓缩、
(5)太阳能路灯蓄电池是磷酸铁锂电池,其工作原理如图所示。电池总反应式为LixC6 + Li1−xFePO4
 LiFePO4 + 6C。试写出充电时,该电池正极材料上的反应式:
LiFePO4 + 6C。试写出充电时,该电池正极材料上的反应式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
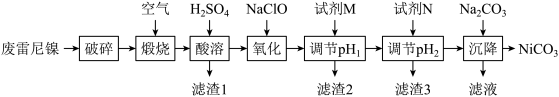
【推荐2】雷尼镍是有机合成中常用的一种加氢催化剂,使用一定周期后会失活。现欲利用图示工艺流程回收某废雷尼镍催化剂(主要为铝镍合金,还含有NiO、Al2O3、FeO、SiO2及有机物等)中的金属资源:
已知金属离子沉淀的pH:
回答下列问题:
(1)“破碎”的目的为______________ ;“滤渣1”的成分为_______ 。
(2)“氧化”时发生反应的离子方程式为______________ 。
(3)调节pH的范围为___________ ;试剂M可选用__________ (填序号)。
a.FeO b.Fe2O3 c.Al2O3 d. NiO
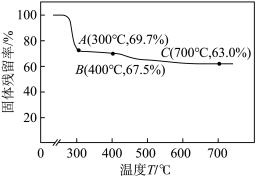
(4)“沉降”后所得NiCO3沉淀在空气中热分解时,固体残留率(固体残留率= ×100%)与温度(T)的关系如图所示(已知当NiCO3加热至300℃ 时已完全失去碳元素)。
×100%)与温度(T)的关系如图所示(已知当NiCO3加热至300℃ 时已完全失去碳元素)。 加热至A点过程中反应的化学方程式为
加热至A点过程中反应的化学方程式为________________ 。
(5)该回收工艺中可回收的金属化合物有 、
、_______ 。

已知金属离子沉淀的pH:
| Ni2+ | Fe2+ | Fe3+ | Al3+ | |
| 开始沉淀的pH | 6.9 | 6.3 | 1.5 | 3.4 |
| 沉淀完全的pH | 8.9 | 8.3 | 2.8 | 4.7 |
回答下列问题:
(1)“破碎”的目的为
(2)“氧化”时发生反应的离子方程式为
(3)调节pH的范围为
a.FeO b.Fe2O3 c.Al2O3 d. NiO
(4)“沉降”后所得NiCO3沉淀在空气中热分解时,固体残留率(固体残留率=
 ×100%)与温度(T)的关系如图所示(已知当NiCO3加热至300℃ 时已完全失去碳元素)。
×100%)与温度(T)的关系如图所示(已知当NiCO3加热至300℃ 时已完全失去碳元素)。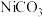 加热至A点过程中反应的化学方程式为
加热至A点过程中反应的化学方程式为
(5)该回收工艺中可回收的金属化合物有
 、
、
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品,工业上常用铝土矿(主要成分为Al2O3和少量SiO2、Fe2O3杂质)生产铵明矾晶体NH4Al(SO4)2•12H2O,其工艺流程图如图:
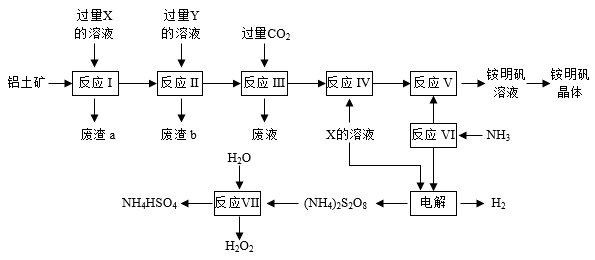
(1)为加快铝土矿的溶解可采用的方法是__________ (任写一点即可),废渣a的化学式______________
(2)流程图中X的化学式为_______________ 。
(3)反应Ⅲ的离子方程式为_________ ,从铵明矾溶液中获得铵明矾晶体的操作依次为________ (填操作名称)、冷却结晶、过滤洗涤。
(4)反应Ⅶ的化学方程式为______________ 。
(5)向硫酸铝铵溶液中逐滴加入氢氧化钡溶液,不可能发生的离子反应是______ 。(填选项字母)
A.NH + SO
+ SO + Ba2+ + OH— = BaSO4↓+ NH3·H2O
+ Ba2+ + OH— = BaSO4↓+ NH3·H2O
B.2Al3+ + 3SO + 3Ba2+ + 6OH— = 3BaSO4↓+ 2Al(OH)3↓
+ 3Ba2+ + 6OH— = 3BaSO4↓+ 2Al(OH)3↓
C.Al3+ + 2SO + 2Ba2+ + 4OH— = 2BaSO4↓+ AlO2—+ 2H2O
+ 2Ba2+ + 4OH— = 2BaSO4↓+ AlO2—+ 2H2O
D.NH + Al3+ + 2SO
+ Al3+ + 2SO + 2Ba2+ + 4OH— = 2BaSO4↓+ Al(OH)3↓+ NH3·H2O
+ 2Ba2+ + 4OH— = 2BaSO4↓+ Al(OH)3↓+ NH3·H2O

(1)为加快铝土矿的溶解可采用的方法是
(2)流程图中X的化学式为
(3)反应Ⅲ的离子方程式为
(4)反应Ⅶ的化学方程式为
(5)向硫酸铝铵溶液中逐滴加入氢氧化钡溶液,不可能发生的离子反应是
A.NH
 + SO
+ SO + Ba2+ + OH— = BaSO4↓+ NH3·H2O
+ Ba2+ + OH— = BaSO4↓+ NH3·H2OB.2Al3+ + 3SO
 + 3Ba2+ + 6OH— = 3BaSO4↓+ 2Al(OH)3↓
+ 3Ba2+ + 6OH— = 3BaSO4↓+ 2Al(OH)3↓C.Al3+ + 2SO
 + 2Ba2+ + 4OH— = 2BaSO4↓+ AlO2—+ 2H2O
+ 2Ba2+ + 4OH— = 2BaSO4↓+ AlO2—+ 2H2OD.NH
 + Al3+ + 2SO
+ Al3+ + 2SO + 2Ba2+ + 4OH— = 2BaSO4↓+ Al(OH)3↓+ NH3·H2O
+ 2Ba2+ + 4OH— = 2BaSO4↓+ Al(OH)3↓+ NH3·H2O
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】Ⅰ.如下图所示是实验中常用的几种仪器:
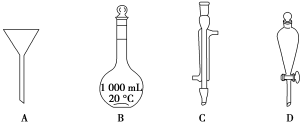
写出各字母所代表的仪器的名称:A________ ;B________ ;C________ ;D________ 。
Ⅱ.实验室要配制500 mL 0.2 mol/L NaOH溶液,请回答下列问题:
(1)配制过程中不需要使用的化学仪器有________ (填字母)。
A.烧杯
B.500 mL容量瓶
C.漏斗
D.胶头滴管
E.玻璃棒
(2)用托盘天平称取氢氧化钠,其质量为________ g。
(3)下列主要操作步骤的正确顺序是________ (填序号)。
①称取一定质量的氢氧化钠,放入烧杯中,用适量蒸馏水溶解;
②加水至液面离容量瓶瓶颈刻度线下1~2 cm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③待冷却至室温后,将溶液转移到500 mL容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
(4)如果实验过程中缺少步骤⑤,会使配制出的NaOH溶液浓度________ (填“偏高”“偏低”或“不变”)。

写出各字母所代表的仪器的名称:A
Ⅱ.实验室要配制500 mL 0.2 mol/L NaOH溶液,请回答下列问题:
(1)配制过程中不需要使用的化学仪器有
A.烧杯
B.500 mL容量瓶
C.漏斗
D.胶头滴管
E.玻璃棒
(2)用托盘天平称取氢氧化钠,其质量为
(3)下列主要操作步骤的正确顺序是
①称取一定质量的氢氧化钠,放入烧杯中,用适量蒸馏水溶解;
②加水至液面离容量瓶瓶颈刻度线下1~2 cm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③待冷却至室温后,将溶液转移到500 mL容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
(4)如果实验过程中缺少步骤⑤,会使配制出的NaOH溶液浓度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室欲配制 240mL 0.2 mol·L-1 的碳酸钠溶液,回答下列问题:
(1)通过计算可知,应用托盘天平称取______ g Na2CO3 固体。
(2)配制过程必需的仪器有: 胶头滴管、托盘天平、药匙、烧杯、玻璃棒,还缺少的仪器是______ 。
(3)在配制过程中,下列操作中会引起误差且使浓度偏小的是___ (填序号)。
①没有洗涤烧杯和玻璃棒 ② 容量瓶不干燥,含有少量蒸馏水
③未冷却到室温就将溶液转移到容量瓶并定容 ④定容时仰视刻度线
(1)通过计算可知,应用托盘天平称取
(2)配制过程必需的仪器有: 胶头滴管、托盘天平、药匙、烧杯、玻璃棒,还缺少的仪器是
(3)在配制过程中,下列操作中会引起误差且使浓度偏小的是
①没有洗涤烧杯和玻璃棒 ② 容量瓶不干燥,含有少量蒸馏水
③未冷却到室温就将溶液转移到容量瓶并定容 ④定容时仰视刻度线
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】在学习了硝酸的强氧化性后,某学习小组进行了浓硝酸和硫单质反应的实验探究。他们根据氧化还原反应原理推测硫的氧化产物,提出三种假设:
Ⅰ.只有H2SO4; Ⅱ.只有SO2; Ⅲ.SO2和H2SO4都有。
为了探究是哪一种情况,他们设计了下列实验流程及步骤:
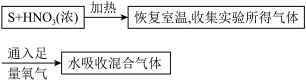
①实验所得气体折算成标准状况为1.792 L。
②混合气体用水吸收后,测得无含硫、含氮化合物逸出,并将吸收液配成100.00 mL溶液。
③取②中所得溶液20.00 mL,加足量BaCl2溶液得白色沉淀0.466 g。
④再取20.00 mL②中所得溶液,用NaOH溶液中和,恰好用去0.6 mol·L-1 NaOH溶液30.00 mL。
请回答下列问题:
(1)混合气体中NO2气体被水充分吸收的化学方程式为______________________________ 。
(2)②中配制溶液所用到的玻璃仪器除烧杯、量筒外还有______________________________ 。
(3)收集到的气体中含有__________________ ,假设____________ (填“Ⅰ”“Ⅱ”或“Ⅲ”)成立。
(4)配制的100.00 mL溶液中H+的物质的量浓度是_______________ ,该实验中S与浓HNO3反应的化学方程式为__________________________________________________ 。
Ⅰ.只有H2SO4; Ⅱ.只有SO2; Ⅲ.SO2和H2SO4都有。
为了探究是哪一种情况,他们设计了下列实验流程及步骤:

①实验所得气体折算成标准状况为1.792 L。
②混合气体用水吸收后,测得无含硫、含氮化合物逸出,并将吸收液配成100.00 mL溶液。
③取②中所得溶液20.00 mL,加足量BaCl2溶液得白色沉淀0.466 g。
④再取20.00 mL②中所得溶液,用NaOH溶液中和,恰好用去0.6 mol·L-1 NaOH溶液30.00 mL。
请回答下列问题:
(1)混合气体中NO2气体被水充分吸收的化学方程式为
(2)②中配制溶液所用到的玻璃仪器除烧杯、量筒外还有
(3)收集到的气体中含有
(4)配制的100.00 mL溶液中H+的物质的量浓度是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】海洋是一座资源的宝库,化学工业中的许多基础原料都来自海洋,以下是利用海洋资源生产卤素单质 Cl2、Br2、I2的工艺流程。回答下列问题:

注:i.同温同浓度下的氧化性:Cl2 > IO > I2
> I2
ii.25℃时,I2在水中与CCl4中的溶解度如下表:
(1)物质A在常温常压下为气体,其化学式为_______ 。
(2)步骤Ⅰ不需要用到下列仪器中的_______ (填标号),步骤Ⅱ的操作名称为_______ 。
a.酒精灯 b.玻璃棒 c.坩埚 d.泥三角
(3)步骤Ⅲ中氧化I-为I2时,需要严格控制Cl2的用量,目的是_______ 。
(4)在步骤Ⅳ能利用CCl4从水溶液中提取I2的原因是_______ 。
(5)通过步骤Ⅴ已获得Br2,步骤Ⅵ中又利用SO2将Br2还原为Br-的目的是_______ ,有关反应的化学方程式为_______ 。

注:i.同温同浓度下的氧化性:Cl2 > IO
 > I2
> I2ii.25℃时,I2在水中与CCl4中的溶解度如下表:
| 溶剂 | 溶解度 |
| H2O | 0.034g/100g |
| CCl4 | 2.9g/100g |
(2)步骤Ⅰ不需要用到下列仪器中的
a.酒精灯 b.玻璃棒 c.坩埚 d.泥三角
(3)步骤Ⅲ中氧化I-为I2时,需要严格控制Cl2的用量,目的是
(4)在步骤Ⅳ能利用CCl4从水溶液中提取I2的原因是
(5)通过步骤Ⅴ已获得Br2,步骤Ⅵ中又利用SO2将Br2还原为Br-的目的是
您最近一年使用:0次
【推荐2】在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采用如图所示的工艺流程生产单质碘:
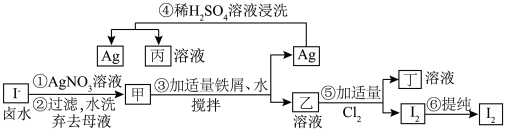
试回答:(1)乙、丁中溶质的化学式:乙____ ,丁_____ 。
(2)第④步操作中用稀H2SO4浸洗的目的是_____ (填写字母编号)。
a.除去未反应的NO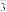 b.除去未反应的I-
b.除去未反应的I-
c.除去未反应的Fe d.除去碱性物质
(3)第⑥步操作可供提纯的方法是_____ (操作名称)。
(4)实验室检验I2的试剂是_______ 。
(5)甲物质见光易变黑,其原因是______ (用化学方程式表示)。

试回答:(1)乙、丁中溶质的化学式:乙
(2)第④步操作中用稀H2SO4浸洗的目的是
a.除去未反应的NO
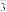 b.除去未反应的I-
b.除去未反应的I-c.除去未反应的Fe d.除去碱性物质
(3)第⑥步操作可供提纯的方法是
(4)实验室检验I2的试剂是
(5)甲物质见光易变黑,其原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】发电玻璃——碲化镉玻璃中主要含有CdTe(其中含有少量Fe、Ni、Mg、Si、O等元素组成的化合物),工业上利用废弃碲化镉(CdTe)玻璃回收其中金属的工艺流程如下。

已知:①常温时,有关物质的 如下表。
如下表。
②当溶液中离子浓度小于 时,可认为沉淀完全。
时,可认为沉淀完全。
回答下列问题:
(1)在“焙烧”中,将废弃碲化镉玻璃粉碎的目的是___________ 。“高温尾气”中含 ,Te的基态原子的价层电子排布式是
,Te的基态原子的价层电子排布式是___________ 。
(2)在“烧渣浸取”中得到的浸渣经灼烧后的主要成分是___________ (填化学式)。
(3)在“氧化除铁”中,写出加入 将
将 氧化成
氧化成 的离子方程式:
的离子方程式:___________ 。
(4)在“沉镁”中,测得“氧化除铁”滤液中 浓度为
浓度为 ,取
,取 滤液,则至少加入
滤液,则至少加入___________ g 固体才能使
固体才能使 沉淀完全。
沉淀完全。
(5)“操作A”需要的玻璃仪器有___________ 。获得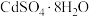 的“操作B”依次为
的“操作B”依次为___________ 、过滤、洗涤、干燥。

已知:①常温时,有关物质的
 如下表。
如下表。 |  |  |  |  |
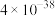 | 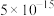 | 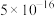 |  | 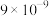 |
 时,可认为沉淀完全。
时,可认为沉淀完全。回答下列问题:
(1)在“焙烧”中,将废弃碲化镉玻璃粉碎的目的是
 ,Te的基态原子的价层电子排布式是
,Te的基态原子的价层电子排布式是(2)在“烧渣浸取”中得到的浸渣经灼烧后的主要成分是
(3)在“氧化除铁”中,写出加入
 将
将 氧化成
氧化成 的离子方程式:
的离子方程式:(4)在“沉镁”中,测得“氧化除铁”滤液中
 浓度为
浓度为 ,取
,取 滤液,则至少加入
滤液,则至少加入 固体才能使
固体才能使 沉淀完全。
沉淀完全。(5)“操作A”需要的玻璃仪器有
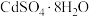 的“操作B”依次为
的“操作B”依次为
您最近一年使用:0次



