硒(Se)和铜(Cu)在生产生活中有广泛的应用。硒可以用作光敏材料、电解锰行业的催化剂,也是动物体必需的营养元素和对植物有益的营养元素等。氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下所示:
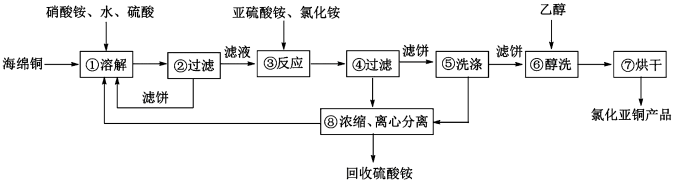
请回答下列问题:
(1)若步骤①中得到的氧化产物只有一种,则它的化学式是____________ 。
(2)写出步骤③中主要反应的离子方程式:_________ 。
(3)步骤⑤包括用pH=2的溶液酸洗、水洗两步操作,酸洗采用的酸是_______ (写酸的名称)。
(4)上述工艺中,步骤⑥和⑦的作用是__________ 。
(5)Se为ⅥA族元素,用乙二胺四乙酸铜阴离子水溶液和硒代硫酸钠(Na2SeSO3)溶液反应可获得纳米硒化铜,硒代硫酸钠还可用于Se的精制,写出硒代硫酸钠(Na2SeSO3)与H2SO4溶液反应得到精硒的化学方程式:______________ 。
(6)氯化亚铜产率与温度、溶液pH关系如下图所示。据图分析,流程化生产氯化亚铜的过程中,温度过低影响CuCl产率的原因是_________ ;温度过高、pH过大也会影响CuCl产率的原因是____________ 。


请回答下列问题:
(1)若步骤①中得到的氧化产物只有一种,则它的化学式是
(2)写出步骤③中主要反应的离子方程式:
(3)步骤⑤包括用pH=2的溶液酸洗、水洗两步操作,酸洗采用的酸是
(4)上述工艺中,步骤⑥和⑦的作用是
(5)Se为ⅥA族元素,用乙二胺四乙酸铜阴离子水溶液和硒代硫酸钠(Na2SeSO3)溶液反应可获得纳米硒化铜,硒代硫酸钠还可用于Se的精制,写出硒代硫酸钠(Na2SeSO3)与H2SO4溶液反应得到精硒的化学方程式:
(6)氯化亚铜产率与温度、溶液pH关系如下图所示。据图分析,流程化生产氯化亚铜的过程中,温度过低影响CuCl产率的原因是

更新时间:2019-06-01 17:40:16
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学研究性学习小组设计实验探究铜的常见化学性质,过程设计如下所示:
【提出猜想】
问题1:在周期表中,铜与铝的位置很靠近,铜不如铝活泼,氢氧化铝具有两性。那么,氢氧化铜也具有两性吗?
问题2:铁和铜都有变价,一般情况下,正二价铁的稳定性小于正三价铁的稳定性。那么,正一价铜的稳定性也小于正二价铜的稳定性吗?
问题3:氧化铜具有氧化性,能被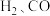 还原。那么,氧化铜也能被氮的某种气态氢化物还原吗?
还原。那么,氧化铜也能被氮的某种气态氢化物还原吗?
【实验探究】
Ⅰ.解决问题1
(1)需用到的药品除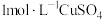 溶液、稀硫酸外,还需
溶液、稀硫酸外,还需____________ (填试剂的化学式)溶液。
(2)为达到本实验目的,你认为应进行的相关实验是(填实验内容):
①__________________ ;②__________________ 。
Ⅱ.解决问题2
取一定量制得的氢氧化铜固体,于坩埚中灼烧,当温度达到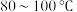 时得到黑色固体粉末;继续加热至
时得到黑色固体粉末;继续加热至 以上,黑色粉末全部变成红色粉末氧化亚铜;取适量红色氧化亚铜粉末于洁浄试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液,同时观察到试管底部还有红色固体存在。根据以上实验现象回答问题:
以上,黑色粉末全部变成红色粉末氧化亚铜;取适量红色氧化亚铜粉末于洁浄试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液,同时观察到试管底部还有红色固体存在。根据以上实验现象回答问题:
(3)写出氧化亚铜与稀硫酸(或盐酸)反应的离子方程式:______________________________ 。
(4)从实验Ⅱ可得出的结论是:__________________________________________ 。
(5)往蓝色溶液中逐滴加入过量的氨水,发生反应的离子方程式为:______________ 、______________ 。
Ⅲ.解决问题3
设计如图装置(夹持装置未画出):

当氮的某种气态氢化物(X)缓缓通过灼热的氧化铜时,观察到氧化铜由黑色变成了红色,无水 变成了蓝色,生成物中还有一种无污染的单质气体Y;将X通入灼热的
变成了蓝色,生成物中还有一种无污染的单质气体Y;将X通入灼热的 燃烧管完全反应后,消耗
燃烧管完全反应后,消耗 ,测得B装置增重
,测得B装置增重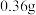 ,并收集到
,并收集到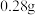 单质气体Y。
单质气体Y。
(6)C装置中发生反应的化学方程式为________________________________ 。
【提出猜想】
问题1:在周期表中,铜与铝的位置很靠近,铜不如铝活泼,氢氧化铝具有两性。那么,氢氧化铜也具有两性吗?
问题2:铁和铜都有变价,一般情况下,正二价铁的稳定性小于正三价铁的稳定性。那么,正一价铜的稳定性也小于正二价铜的稳定性吗?
问题3:氧化铜具有氧化性,能被
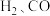 还原。那么,氧化铜也能被氮的某种气态氢化物还原吗?
还原。那么,氧化铜也能被氮的某种气态氢化物还原吗?【实验探究】
Ⅰ.解决问题1
(1)需用到的药品除
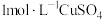 溶液、稀硫酸外,还需
溶液、稀硫酸外,还需(2)为达到本实验目的,你认为应进行的相关实验是(填实验内容):
①
Ⅱ.解决问题2
取一定量制得的氢氧化铜固体,于坩埚中灼烧,当温度达到
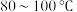 时得到黑色固体粉末;继续加热至
时得到黑色固体粉末;继续加热至 以上,黑色粉末全部变成红色粉末氧化亚铜;取适量红色氧化亚铜粉末于洁浄试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液,同时观察到试管底部还有红色固体存在。根据以上实验现象回答问题:
以上,黑色粉末全部变成红色粉末氧化亚铜;取适量红色氧化亚铜粉末于洁浄试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液,同时观察到试管底部还有红色固体存在。根据以上实验现象回答问题:(3)写出氧化亚铜与稀硫酸(或盐酸)反应的离子方程式:
(4)从实验Ⅱ可得出的结论是:
(5)往蓝色溶液中逐滴加入过量的氨水,发生反应的离子方程式为:
Ⅲ.解决问题3
设计如图装置(夹持装置未画出):

当氮的某种气态氢化物(X)缓缓通过灼热的氧化铜时,观察到氧化铜由黑色变成了红色,无水
 变成了蓝色,生成物中还有一种无污染的单质气体Y;将X通入灼热的
变成了蓝色,生成物中还有一种无污染的单质气体Y;将X通入灼热的 燃烧管完全反应后,消耗
燃烧管完全反应后,消耗 ,测得B装置增重
,测得B装置增重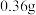 ,并收集到
,并收集到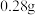 单质气体Y。
单质气体Y。(6)C装置中发生反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解结晶水合物CuCl·2H2O制备CuCl,并进行相关探究。
查阅资料:CuCl2•2H2O CuCl2
CuCl2  CuCl+Cl2;CuCl2•2H2O
CuCl+Cl2;CuCl2•2H2O Cu2(OH)2Cl2
Cu2(OH)2Cl2 CuO
CuO
(实验探究)该小组用下图所示装置进行实验(夹持仪器略)。

请回答下列问题:
(1)仪器X的名称是___ ;装置D中倒扣的三角漏斗的作用是_____ ;
(2)实验操作的先后顺序是a→____ →____ →____ →e (填操作的编号)。
a.检查装置的气密性后加入药品 b.熄灭酒精灯,冷却 c.在“气体入口”处通入干燥HCl d.点燃酒精灯,加热 e.停止通入HCl,然后通入N2
(3)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是____ ;
(4)装置D中发生的氧化还原反应的离子方程式是_____ ;
(5)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质,根据资料信息分析:
①若杂质是CuCl2,则产生的原因是____ ;
②若杂质是CuO,则产生的原因是____ 。
查阅资料:CuCl2•2H2O
 CuCl2
CuCl2  CuCl+Cl2;CuCl2•2H2O
CuCl+Cl2;CuCl2•2H2O Cu2(OH)2Cl2
Cu2(OH)2Cl2 CuO
CuO(实验探究)该小组用下图所示装置进行实验(夹持仪器略)。

请回答下列问题:
(1)仪器X的名称是
(2)实验操作的先后顺序是a→
a.检查装置的气密性后加入药品 b.熄灭酒精灯,冷却 c.在“气体入口”处通入干燥HCl d.点燃酒精灯,加热 e.停止通入HCl,然后通入N2
(3)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是
(4)装置D中发生的氧化还原反应的离子方程式是
(5)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质,根据资料信息分析:
①若杂质是CuCl2,则产生的原因是
②若杂质是CuO,则产生的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】辉铜矿石主要含有硫化亚铜(Cu2S)及少量脉石(SiO2)。一种以辉铜矿石为原料制备硝酸铜的工艺流程如下:
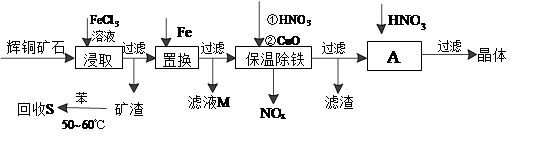
(1)写出浸取过程中Cu2S溶解的离子方程式____________ 。
(2)回收S过程中温度控制在50℃~60℃之间,不宜过高或过低的原因是_________ 、__________ 。
(3)保温除铁过程中加入CuO的目的是____________ 。
(4)A步操作为____________ 要用硝酸调节溶液的pH,其理由是____________ 。

(1)写出浸取过程中Cu2S溶解的离子方程式
(2)回收S过程中温度控制在50℃~60℃之间,不宜过高或过低的原因是
(3)保温除铁过程中加入CuO的目的是
(4)A步操作为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。回答下列问题:

(1)A中发生反应的化学方程式是_______
(2)B中加入的物质是_______ ,其作用是_______
(3)实验时在C中观察到的现象是_______ ,发生反应的化学方程式是_______
(4)实验时在D中观察到的现象是_______ ,收集到的物质是_______

(1)A中发生反应的化学方程式是
(2)B中加入的物质是
(3)实验时在C中观察到的现象是
(4)实验时在D中观察到的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】医用氯化钙可用于补钙抗过敏等,以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)生产医用二水合氯化钙(CaCl2 ·2H2O的质量分数为97.3—103.0%),工艺流程为:

(1)CaCO3与盐酸反应的离子方程式__________________________ 。
(2)过滤时需用的玻璃仪器除烧杯、玻璃棒外还有______ 。滤渣主要成分的化学式___________________ 。
(3)酸化时加盐酸的目的为:
①___________________________________ ,
②防止Ca2+ 在蒸发时发生水解。
(4)为什么蒸发结晶要保持在160℃:_______________________ 。
(5)为测定样品中CaCl2 ·2H2O的含量,称取0.7522g样品并配成250mL溶液,分别取该溶液25.00mL于三个锥形瓶中,用0.04mol/LAgNO3溶液进行三次滴定,消耗 AgNO3溶液的平均体积为20.39mL。
①通过计算,样品中含CaCl2 ·2H2O的质量分数______ 。
②若所测样品 CaCl2 ·2H2O的质量分数偏高(忽略其它实验误差),可能的原因之一为_______________ 。

(1)CaCO3与盐酸反应的离子方程式
(2)过滤时需用的玻璃仪器除烧杯、玻璃棒外还有
(3)酸化时加盐酸的目的为:
①
②防止Ca2+ 在蒸发时发生水解。
(4)为什么蒸发结晶要保持在160℃:
(5)为测定样品中CaCl2 ·2H2O的含量,称取0.7522g样品并配成250mL溶液,分别取该溶液25.00mL于三个锥形瓶中,用0.04mol/LAgNO3溶液进行三次滴定,消耗 AgNO3溶液的平均体积为20.39mL。
①通过计算,样品中含CaCl2 ·2H2O的质量分数
②若所测样品 CaCl2 ·2H2O的质量分数偏高(忽略其它实验误差),可能的原因之一为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】某混合物甲中含有明矾[KAl(SO4)2·12H2O]、Al2O3和Fe2O3。在一定条件下由甲可实现下图所示的物质之间的转化。
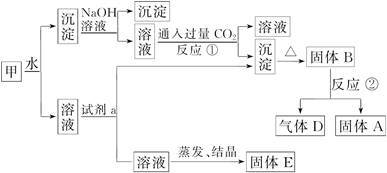
请回答下列问题:
(1)写出A、B、的化学式:A______________ 、B______________
(2)试剂a最好选用___________ (选填A、B、C、D)。
A.NaOH溶液 B.稀盐酸
C.二氧化碳 D.氨水
(3)写出Al2O3 与NaOH反应方程式:______________________
(4)写出少量明矾加入氢氧化钡溶液中与反应方程式:___________________
(5)写出反应①的方程式:_________________________
(6)固体E可以作为复合性的化学肥料,E中所含物质的化学式为_________________

请回答下列问题:
(1)写出A、B、的化学式:A
(2)试剂a最好选用
A.NaOH溶液 B.稀盐酸
C.二氧化碳 D.氨水
(3)写出Al2O3 与NaOH反应方程式:
(4)写出少量明矾加入氢氧化钡溶液中与反应方程式:
(5)写出反应①的方程式:
(6)固体E可以作为复合性的化学肥料,E中所含物质的化学式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】Ⅰ.某化学兴趣小组为测定葡萄酒中 的含量,通过适当的方法使所含
的含量,通过适当的方法使所含 全部逸出并用
全部逸出并用 将其全部氧化为
将其全部氧化为 ,然后用NaOH标准溶液进行滴定。回答下列问题:
,然后用NaOH标准溶液进行滴定。回答下列问题:
(1)写出 气体与
气体与 溶液反应的化学方程式
溶液反应的化学方程式___________ 。
(2)滴定前应先排出管内气泡,图中操作和仪器选择均正确的是___________(填字母)。
(3)若用50 mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积___________(填字母)。
(4)上述滴定实验中,选用酚酞作指示剂,判断反应达到终点的现象是___________ 。
Ⅱ.加热 饱和溶液,测得该溶液的pH发生如下变化:
饱和溶液,测得该溶液的pH发生如下变化:
(5)甲同学认为:该溶液被pH升高的原因是HCO 的水解程度增大,碱性增强。
的水解程度增大,碱性增强。
乙同学认为:该溶液pH升高的原因是 受热分解,生成了
受热分解,生成了 ,并推断
,并推断 的水解程度
的水解程度___________ (填“>”或“<”)  的水解程度。
的水解程度。
(6)丙同学认为:甲、乙的判断都不充分,还需要进一步补做实验来验证。
①将加热煮沸后的溶液冷却到10℃,若溶液的pH___________ (填“>”“<”或“=”)8.3,则甲的判断正确。
②在查阅资料,发现 的分解温度为150℃,丙断言
的分解温度为150℃,丙断言___________ (填“甲”或“乙”)的判断是错误的,理由是___________ 。
 的含量,通过适当的方法使所含
的含量,通过适当的方法使所含 全部逸出并用
全部逸出并用 将其全部氧化为
将其全部氧化为 ,然后用NaOH标准溶液进行滴定。回答下列问题:
,然后用NaOH标准溶液进行滴定。回答下列问题:(1)写出
 气体与
气体与 溶液反应的化学方程式
溶液反应的化学方程式(2)滴定前应先排出管内气泡,图中操作和仪器选择均正确的是___________(填字母)。
A. | B. | C. | D. |
| A.=10 mL | B.=40 mL | C.<10 mL | D.>40 mL |
Ⅱ.加热
 饱和溶液,测得该溶液的pH发生如下变化:
饱和溶液,测得该溶液的pH发生如下变化:| 温度 | 10℃ | 20℃ | 30℃ | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
 的水解程度增大,碱性增强。
的水解程度增大,碱性增强。乙同学认为:该溶液pH升高的原因是
 受热分解,生成了
受热分解,生成了 ,并推断
,并推断 的水解程度
的水解程度 的水解程度。
的水解程度。(6)丙同学认为:甲、乙的判断都不充分,还需要进一步补做实验来验证。
①将加热煮沸后的溶液冷却到10℃,若溶液的pH
②在查阅资料,发现
 的分解温度为150℃,丙断言
的分解温度为150℃,丙断言
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某校化学兴趣小组同学取锌粒与浓H2SO4充分反应制取SO2气体,待锌粒全部溶解后,同学们准备用收集到的气体(X)做实验,但是老师说收集到的气体(X)可能含有杂质。
(1)该化学兴趣小组制得的气体(X)中混有的主要杂质气体可能是___ (填化学式)。
(2)为证实相关分析,该小组的同学设计了如图所示的实验装置,对此气体(X)取样进行认真研究(遇有气体吸收过程,可视为全吸收)。
①酸性KMnO4溶液的作用是___ ;
②B中添加的试剂是___ 。
(1)该化学兴趣小组制得的气体(X)中混有的主要杂质气体可能是
(2)为证实相关分析,该小组的同学设计了如图所示的实验装置,对此气体(X)取样进行认真研究(遇有气体吸收过程,可视为全吸收)。

①酸性KMnO4溶液的作用是
②B中添加的试剂是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】硫酸亚铁(FeSO4)和硫酸亚铁铵[(NH4)2Fe(SO4)2]都是在生产、生活中有重要用途的亚铁盐,探究其饱和溶液稳定性的实验如下:先分别配制FeSO4、(NH4)2Fe(SO4)2饱和溶液,测定pH分别为4.46、4.22,后续实验如图所示。
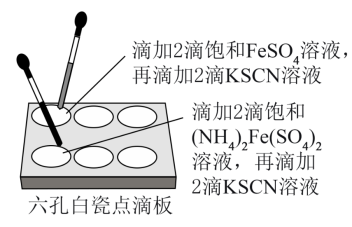
实验结果如表:
回答下列问题:
(1)用白瓷点滴板做上述对比实验的主要优点是____ (答出两条)。
(2)由该实验可以得出两种饱和溶液的稳定性:FeSO4____ (NH4)2Fe(SO4)2(填“大于”“小于”或“等于”,下同),物质的量浓度:FeSO4____ (NH4)2Fe(SO4)2。
(3)FeSO4饱和溶液需要新配制,若久置会发黄、变浑浊,且pH减小,发生反应的离子方程式为____ 。
(4)影响溶液中Fe2+稳定性的因素可提出3种假设。
假设1: 的存在使溶液中Fe2+稳定性增强。
的存在使溶液中Fe2+稳定性增强。
假设2:_____ 使溶液中Fe2+稳定性增强。
假设3:H+浓度增大使溶液中Fe2+稳定性增强。
假设1的依据是 具有一定的还原性,对Fe2+有保护作用,判断该观点是否合理并说明理由
具有一定的还原性,对Fe2+有保护作用,判断该观点是否合理并说明理由____ 。
(5)实验测得相同浓度的FeSO4溶液在不同pH条件下,Fe2+的损耗量%与pH的关系及Fe2+的氧化速率与时间的关系如图(实验过程中溶液温度几乎无变化)。
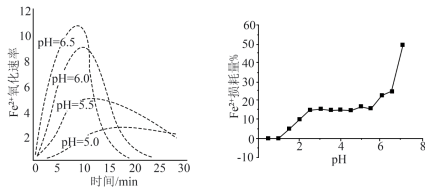
据图分析,开始时Fe2+氧化速率较小,随着产物的生成,速率明显加快,说明产物对反应有催化作用,起催化作用的产物是____ (填化学式),其催化活性最强的pH范围是____ (填标号)。
A.0~1 B.2~2.4 C.2.4~5.5 D.5.5~7
从趋势上看,pH越小,Fe2+损耗量越小的原因是____ 。

实验结果如表:
| 硫酸亚铁和硫酸亚铁铵饱和溶液稳定性对比实验研究 | |||||||
| 溶质 | 0min | 1min | 15min | 60min | 3h | 5h | 24h |
| FeSO4 | 淡淡的桔黄色 | 桔红色 | 红色 | 红色 | 深红 | 深红 | 深红 |
| (NH4)2Fe(SO4)2 | 几乎无色 | 米色 | 米色 | 浅黄 | 黄色 | 桔红 | 桔红 |
(1)用白瓷点滴板做上述对比实验的主要优点是
(2)由该实验可以得出两种饱和溶液的稳定性:FeSO4
(3)FeSO4饱和溶液需要新配制,若久置会发黄、变浑浊,且pH减小,发生反应的离子方程式为
(4)影响溶液中Fe2+稳定性的因素可提出3种假设。
假设1:
 的存在使溶液中Fe2+稳定性增强。
的存在使溶液中Fe2+稳定性增强。假设2:
假设3:H+浓度增大使溶液中Fe2+稳定性增强。
假设1的依据是
 具有一定的还原性,对Fe2+有保护作用,判断该观点是否合理并说明理由
具有一定的还原性,对Fe2+有保护作用,判断该观点是否合理并说明理由(5)实验测得相同浓度的FeSO4溶液在不同pH条件下,Fe2+的损耗量%与pH的关系及Fe2+的氧化速率与时间的关系如图(实验过程中溶液温度几乎无变化)。

据图分析,开始时Fe2+氧化速率较小,随着产物的生成,速率明显加快,说明产物对反应有催化作用,起催化作用的产物是
A.0~1 B.2~2.4 C.2.4~5.5 D.5.5~7
从趋势上看,pH越小,Fe2+损耗量越小的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某兴趣小组利用下列装置制得了纯度高的NaClO溶液。

已知:Cl2O是棕黄色气体,是HClO的酸酐,沸点约3.8°C,42°C以上分解生成Cl2和O2。通入的空气不参与化学反应。回答下列问题:
(1)装置的连接顺序是A→___________ →___________ →C→___________ ,Cl2O和Cl2在CCl4中的溶解度较大的是___________ 。
(2)装置A中发生反应的离子方程式为___________ ,D的作用是___________ ,E中发生的化学反应方程式为___________ 。
(3)实验时装置B应置于水浴中加热,其水浴温度应___________ ,实验开始后观察到B中有大量的棕黄色气体产生,B中反应的离子方程式为___________ 。
(4)测定所制得的次氯酸钠的物质的量浓度:量取10.0mL实验制得的次氯酸钠溶液,并稀释至100mL,再从其中取出10.00mL于锥形瓶中,加入10.00mL0.5000mol/L的Na2SO3溶液,充分反应后,用0.1000mol/L碘水滴定过量Na2SO3溶液至终点,平行滴定三次,消耗碘水溶液平均体积20.00mL,滴定时所选指示剂是___________ ,终点时的现象为___________ ,所制得次氯酸钠溶液的浓度为___________ (氧化性:ClO-> ,还原性:
,还原性: >I-)。
>I-)。

已知:Cl2O是棕黄色气体,是HClO的酸酐,沸点约3.8°C,42°C以上分解生成Cl2和O2。通入的空气不参与化学反应。回答下列问题:
(1)装置的连接顺序是A→
(2)装置A中发生反应的离子方程式为
(3)实验时装置B应置于水浴中加热,其水浴温度应
(4)测定所制得的次氯酸钠的物质的量浓度:量取10.0mL实验制得的次氯酸钠溶液,并稀释至100mL,再从其中取出10.00mL于锥形瓶中,加入10.00mL0.5000mol/L的Na2SO3溶液,充分反应后,用0.1000mol/L碘水滴定过量Na2SO3溶液至终点,平行滴定三次,消耗碘水溶液平均体积20.00mL,滴定时所选指示剂是
 ,还原性:
,还原性: >I-)。
>I-)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某同学类比镁在二氧化碳中的燃烧反应,认为钠和二氧化碳也可以发生反应,他在实验室中选择以下装置对该反应能否发生进行了实验探究。
依据要求回答问题:
(1)二氧化碳的发生装置应选用上述装置中的______ (填装置下方对应字母),反应的化学方程式为________________ 。
(2)为达到实验目的,选择上图中的装置,其连接顺序为:二氧化碳的发生装置→_____________ 。(按气流方向,用小写字母表示)。
(3)检查装置气密性良好,装好药品后,打开弹簧夹,待装置中的空气排净后才能点燃酒精灯。能说明装置中空气已经排净的现象是_____________ 。
(4)该同学在制取CO2的过程中,向装置B中加入某酸后,发现固体与酸没有接触,为使反应顺利进行,下列可再加入的试剂是_____________ 。
A.稀硝酸 B.H2SO4溶液 C.苯 D. CCl4
(5)若反应过程中CO2足量,反应结束后,该同学对硬质玻璃管中生成的固体提出了以下猜想:①生成的固体物质为Na2CO3 ② 生成的固体物质为Na2CO3和C的混合物 ③生成的固体物质为Na2CO3和Na2O的混合物 ④生成的固体物质为Na2O和C的混合物。报告给老师后,老师认为可以排除其中的3种情况,老师排除的理由是________ ;则钠与CO2反应的化学方程式为____________ 。
(6)该同学经过反思,认为上述实验设计中存在缺陷。他查阅资料后得知,PdCl2溶液可以吸收CO,同时得到黑色的Pd。于是他在装置后加装一个盛PdCl2溶液的吸收装置,该装置中发生反应的化学方程式为____________ 。
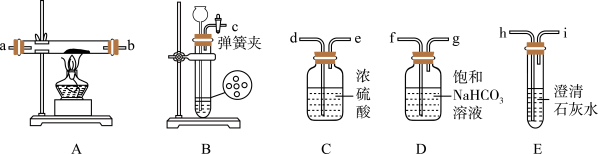
依据要求回答问题:
(1)二氧化碳的发生装置应选用上述装置中的
(2)为达到实验目的,选择上图中的装置,其连接顺序为:二氧化碳的发生装置→
(3)检查装置气密性良好,装好药品后,打开弹簧夹,待装置中的空气排净后才能点燃酒精灯。能说明装置中空气已经排净的现象是
(4)该同学在制取CO2的过程中,向装置B中加入某酸后,发现固体与酸没有接触,为使反应顺利进行,下列可再加入的试剂是
A.稀硝酸 B.H2SO4溶液 C.苯 D. CCl4
(5)若反应过程中CO2足量,反应结束后,该同学对硬质玻璃管中生成的固体提出了以下猜想:①生成的固体物质为Na2CO3 ② 生成的固体物质为Na2CO3和C的混合物 ③生成的固体物质为Na2CO3和Na2O的混合物 ④生成的固体物质为Na2O和C的混合物。报告给老师后,老师认为可以排除其中的3种情况,老师排除的理由是
(6)该同学经过反思,认为上述实验设计中存在缺陷。他查阅资料后得知,PdCl2溶液可以吸收CO,同时得到黑色的Pd。于是他在装置后加装一个盛PdCl2溶液的吸收装置,该装置中发生反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。回答下列问题:
(1)KIO3的化学名称是_____ 。
(2)利用“KClO3氧化法”制备KIO3工艺流程如下图所示:

“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是_____ 。“滤液”中的溶质主要是
_____ 。“调pH”中发生反应的化学方程式为_____ 。
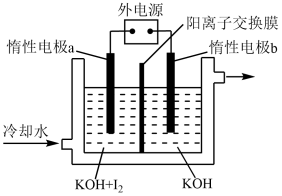
(3)KIO3也可采用“电解法”制备,装置如图所示。
①写出电解时阴极的电极反应式_____ 。
②电解过程中通过阳离子交换膜的离子主要为_____ ,其迁移方向是_____ 。
③与“电解法”相比,“KClO3氧化法”的主要不足之处有_____ (写出一点)。
(1)KIO3的化学名称是
(2)利用“KClO3氧化法”制备KIO3工艺流程如下图所示:

“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是
(3)KIO3也可采用“电解法”制备,装置如图所示。
①写出电解时阴极的电极反应式
②电解过程中通过阳离子交换膜的离子主要为
③与“电解法”相比,“KClO3氧化法”的主要不足之处有
您最近一年使用:0次



