中学化学中几种常见物质的转化关系如下图(部分严物未列出》。A是一种金属单质,D是一种非金属固体单质。

请回答下列问题:
(1)A、C、E的化学式分别为A________ C________ E________ 。
(2)F的浓溶液与A反应过程中,F体现的性质与下列反应中H2SO4体现的性质完全相同的是___________ 。
A.C+2H2SO4(浓) CO2↑+ 2SO2↑+2H2O
CO2↑+ 2SO2↑+2H2O
B.Fe + H2SO4=FeSO4+H2↑
C.Cu+ 2H2SO4(浓)=CuSO4+ SO2↑+2H2O
D.FeO+ H2SO4=FeSO4+H2O
(3)写出反应E+H2O2→F的化学方程式:_____________ 。
(4)若反应F+D→E转移电子数为3.01×1023,,则消耗D的质量为__________ 。

请回答下列问题:
(1)A、C、E的化学式分别为A
(2)F的浓溶液与A反应过程中,F体现的性质与下列反应中H2SO4体现的性质完全相同的是
A.C+2H2SO4(浓)
 CO2↑+ 2SO2↑+2H2O
CO2↑+ 2SO2↑+2H2OB.Fe + H2SO4=FeSO4+H2↑
C.Cu+ 2H2SO4(浓)=CuSO4+ SO2↑+2H2O
D.FeO+ H2SO4=FeSO4+H2O
(3)写出反应E+H2O2→F的化学方程式:
(4)若反应F+D→E转移电子数为3.01×1023,,则消耗D的质量为
2017·全国·二模 查看更多[3]
吉林汪清县汪清第六中学2021-2022学年高三下学期二诊模拟考试化学试题(已下线)5.1.3 不同价态含硫物质的转化(基础过关)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)全国名校大联考2018届高三上学期第二次联考化学试题
更新时间:2017-11-24 21:53:56
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】A、B、C、D是中学化学常见的三种物质,它们之间的相互转化关系如下(反应条件及部分产物已略去):

(1)若A是一种黄色固体单质,则反应②③的化学方程式分别为:___________ ;___________ 。
(2)若A是一种金属单质,C是淡黄色固体,则反应③的化学方程式为:___________ 。

(1)若A是一种黄色固体单质,则反应②③的化学方程式分别为:
(2)若A是一种金属单质,C是淡黄色固体,则反应③的化学方程式为:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】有关物质存在如图所示的转化关系(部分产物已省略)。通常C为气体单质,G为紫黑色固体单质。实验室中,常用固体E在B的催化下加热制取气体单质H。

请回答下列问题:
(1)反应①的化学方程式为_______
(2)反应②的离子方程式为_______
(3)写出另外一种实验室制取H的化学方程式_______

请回答下列问题:
(1)反应①的化学方程式为
(2)反应②的离子方程式为
(3)写出另外一种实验室制取H的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】A是用途最广的金属,B、C是两种常见气体单质,E溶液为常见强酸,D溶液中滴加KSCN溶液显血红色,它们相互转化关系如图所示。

请回答:
(1)写出A与B反应的化学方程式:______________________ 。
(2)写出第④步反应的离子方程式为______________________ 。
(3)写出向F溶液中通入B时发生反应的离子方程式________________ 。
(4)写出Cu与D溶液反应的离子方程式___________________________ 。
(5)用离子方程式表示D溶液中滴加KSCN溶液显红色的原因__________________ 。
(6)向F溶液中滴入NaOH溶液过程中发生的氧化还原反应化学方程式为_______________ 。

请回答:
(1)写出A与B反应的化学方程式:
(2)写出第④步反应的离子方程式为
(3)写出向F溶液中通入B时发生反应的离子方程式
(4)写出Cu与D溶液反应的离子方程式
(5)用离子方程式表示D溶液中滴加KSCN溶液显红色的原因
(6)向F溶液中滴入NaOH溶液过程中发生的氧化还原反应化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】实验室常用下列装置来进行铜跟浓硫酸反应等一系列实验。
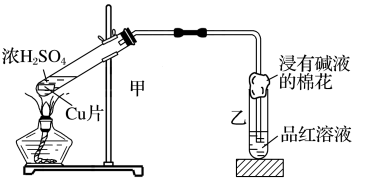
(1)判断铜跟浓硫酸反应有SO2生成所依据的现象是_______ ,甲装置中发生的主要反应的化学方程式是_______ ,该反应中若有3.2g Cu参加反应,则被还原的H2SO4的物质的量为_______ mol。
(2)在装置乙的试管口放有一团浸有碱液的棉花,棉花中通常浸有饱和碳酸钠溶液或氢氧化钠溶液,其目的是:_______ 。
(3)欲观察生成的 溶液的颜色,应采取的操作是
溶液的颜色,应采取的操作是_______ 。
(4)若铜片还有剩余,硫酸_______ (填“有”或“没有”)消耗完毕。其理由是_______ 。

(1)判断铜跟浓硫酸反应有SO2生成所依据的现象是
(2)在装置乙的试管口放有一团浸有碱液的棉花,棉花中通常浸有饱和碳酸钠溶液或氢氧化钠溶液,其目的是:
(3)欲观察生成的
 溶液的颜色,应采取的操作是
溶液的颜色,应采取的操作是(4)若铜片还有剩余,硫酸
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】某小组同学用如图所示装置进行铜与浓硫酸的反应,并探究产物的性质(夹持装置已略去)。
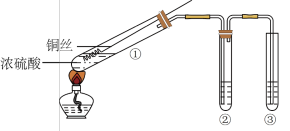
(1)试管①中反应的化学方程式是___________ ;浓硫酸表现出了___________ 性和___________ 性。
(2)若试管②中的试剂为品红溶液,实验中观察到的现象是___________ ;若试管②中的试剂为酸性KMnO4溶液,实验时,观察到溶液褪色,则说明生成的气体具有___________ 性;若试管②中的试剂为新制氯水,则对应的离子方程式为___________ 。
(3)试管③中的试剂为NaOH溶液,其作用是___________ 。

(1)试管①中反应的化学方程式是
(2)若试管②中的试剂为品红溶液,实验中观察到的现象是
(3)试管③中的试剂为NaOH溶液,其作用是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】大气污染物SO2是一种无色刺激性气味气体,A装置可产生SO2,某学习小组利用如图所示装置探究SO2的相关性质(装置A加热装置略):

回答下列问题:
(1)实验开始时,先打开分液漏斗的_______ (填“玻璃塞a”或“活塞b”,下同),再打开_______ ,逐滴加入浓硫酸;
(2)一段时间后,装置B中出现的现象是_______ ,可证明SO2具有_______ (填“氧化性”或“还原性”);
(3)充分反应后取装置C中溶液,加热出现的现象是_______ 。
(4)装置D中发生反应的离子方程式是_______ 。

回答下列问题:
(1)实验开始时,先打开分液漏斗的
(2)一段时间后,装置B中出现的现象是
(3)充分反应后取装置C中溶液,加热出现的现象是
(4)装置D中发生反应的离子方程式是
您最近一年使用:0次
【推荐1】利用太阳能分解水制备氢气的示意图如图。

回答下列问题:
(1)基态硫原子核外电子占据的原子轨道数为___ 。
(2)碘与氯同主族,碘元素在周期表中的位置是___ 。
(3)写出反应I的离子方程式:__ 。
(4)I2在CCl4中的溶解度比在水中的大,其原因是___ 。
(5)常温下,可用干燥的铁制容器储运浓硫酸,原因是__ 。这是利用了浓硫酸的___ (填“脱水”“酸”或“强氧化”)性。

回答下列问题:
(1)基态硫原子核外电子占据的原子轨道数为
(2)碘与氯同主族,碘元素在周期表中的位置是
(3)写出反应I的离子方程式:
(4)I2在CCl4中的溶解度比在水中的大,其原因是
(5)常温下,可用干燥的铁制容器储运浓硫酸,原因是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】已知A、B、C均为单质, A是生产生活中用量最大的金属,室温下B是一种黄绿色气体,C是最轻的无色气体、也是一种良好的高能燃料,在合适的反应条件下,它们可以按下列框图进行反应。又知E溶液是无色的。
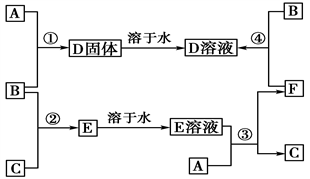
请回答:
(1)试写出下列物质的化学式:
A_____________ ,B_______________ ,C________________ 。
(2)反应①的化学方程式:__________________________ 。
(3)反应②的化学方程式:__________________________ 。
(4)反应③的化学方程式:__________________________ 。

请回答:
(1)试写出下列物质的化学式:
A
(2)反应①的化学方程式:
(3)反应②的化学方程式:
(4)反应③的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】A、B、C为中学化学中的常见物质,它们存在如下转化关系:

回答下列问题:
(1)若B是一种无色气体单质。
①反应Ⅰ是在加热条件下进行,则A的化学式为________ 。
②反应Ⅰ是在常温条件下进行,则A的化学式为________ ,反应Ⅱ的化学方程式为________ 。
(2)若B是一种黄绿色气体,则在加热的条件下反应Ⅰ的离子方程式为________ ,A在该反应中表现的性质是________ ,反应中生成标准状况下4.48LB气体,转移的电子数为________ (用NA表示)。

回答下列问题:
(1)若B是一种无色气体单质。
①反应Ⅰ是在加热条件下进行,则A的化学式为
②反应Ⅰ是在常温条件下进行,则A的化学式为
(2)若B是一种黄绿色气体,则在加热的条件下反应Ⅰ的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】有X、Y、Z三种短周期元素,已知X原子的L层电子比M层电子多2个;Y3+的电子层结构与Ne的相同;Z与X处于同一周期,且其气态单质呈黄绿色。试回答:
(1)写出X元素的名称:___________ 。
(2)写出Y元素在元素周期表中的位置:___________ 。
(3)与Z同主族的元素中,氢化物的稳定性最强的是___________ (填氢化物的化学式)。
(4)Z元素所在主族的元素形成的含氧酸酸性最强的酸是(写化学式)___________ 。
(5)写出Y单质与氢氧化钠溶液反应的化学方程式:___________ 。
(6)在标准状况下,2.24 L单质Z与足量氢氧化钙完全反应时,转移电子___________ mol。
(1)写出X元素的名称:
(2)写出Y元素在元素周期表中的位置:
(3)与Z同主族的元素中,氢化物的稳定性最强的是
(4)Z元素所在主族的元素形成的含氧酸酸性最强的酸是(写化学式)
(5)写出Y单质与氢氧化钠溶液反应的化学方程式:
(6)在标准状况下,2.24 L单质Z与足量氢氧化钙完全反应时,转移电子
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】回答下列问题:
(1)亚氯酸钠是(NaClO2)一种高效氧化剂、漂白剂。在NaOH溶液中ClO2与H2O2反应可以得到亚氯酸钠。
①ClO2中氯元素的化合价是___ ;在制备亚氯酸钠的反应中ClO2作____ (填“氧化剂”或“还原剂”);若反应中生成1molNaClO2,转移电子的物质的量为___ 。
②该反应的化学方程式为___ 。
(2)用电化学气敏传感器测定汽车尾气中CO含量,原理如图,根据燃料电池的原理,推测B电极是该电池的___ (填“正极”或“负极”),A电极上的电极反应式为___ 。
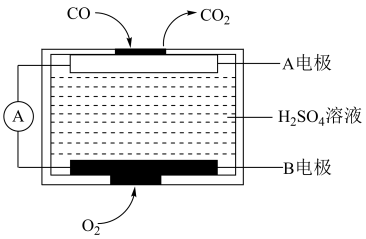
(3)已知H+(aq)+OH-(ag)=H2O(1) ΔH=-57.3kJ/mol。回答有关中和反应的问题。
①用0.1molBa(OH)2配成稀溶液与足量稀硝酸反应,能放出____ kJ热量。
②如图装置中仪器A的名称____ ,碎泡沫塑料的作用是____ 。

若通过实验测定中和热的ΔH,其结果常常大于-57.3kJ/mol,其原因可能是____ (填序号)
a.实验装置保温、隔热效果差
b.在量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有稀硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(1)亚氯酸钠是(NaClO2)一种高效氧化剂、漂白剂。在NaOH溶液中ClO2与H2O2反应可以得到亚氯酸钠。
①ClO2中氯元素的化合价是
②该反应的化学方程式为
(2)用电化学气敏传感器测定汽车尾气中CO含量,原理如图,根据燃料电池的原理,推测B电极是该电池的

(3)已知H+(aq)+OH-(ag)=H2O(1) ΔH=-57.3kJ/mol。回答有关中和反应的问题。
①用0.1molBa(OH)2配成稀溶液与足量稀硝酸反应,能放出
②如图装置中仪器A的名称

若通过实验测定中和热的ΔH,其结果常常大于-57.3kJ/mol,其原因可能是
a.实验装置保温、隔热效果差
b.在量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有稀硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
您最近一年使用:0次





