常温下,下列溶液酸性最强的是
| A.c(H+)=1×10-5mol/L | B.pH=3的溶液 |
| C.c(OH-)=1×10-5mol/L | D.0.1mol/L 的盐酸 |
更新时间:2019/07/01 15:46:33
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】常温下,有下列四种溶液:
下列说法正确的是( )
| ① | ② | ③ | ④ |
| 0.1 mol·L-1NaOH溶液 | pH=11 NaOH溶液 | 0.1mol·L-1CH3COOH溶液 | pH=3 CH3COOH溶液 |
| A.由水电离出的c(H+):①>③ |
| B.③稀释到原来的100倍后,pH与④相同 |
| C.②与④混合,若溶液显酸性,则所得溶液中离子浓度可能为c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
| D.①与③混合,若溶液pH=7,则V(NaOH)>V(CH3COOH) |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】25℃时,有浓度均为 的4种溶液:
的4种溶液:
①盐酸 ②HF溶液 ③NaOH溶液 ④氨水
已知:25℃时,电离平衡常数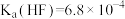 ,
,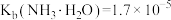
下列说法不正确的是
 的4种溶液:
的4种溶液:①盐酸 ②HF溶液 ③NaOH溶液 ④氨水
已知:25℃时,电离平衡常数
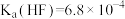 ,
,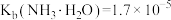
下列说法不正确的是
| A.溶液pH:③>④>②>① |
B.水电离出的 浓度:①=③<②<④ 浓度:①=③<②<④ |
C.②和④等体积混合后的溶液中: |
D. ①和 ①和 ③混合后溶液 ③混合后溶液 (溶液体积变化忽略不计),则 (溶液体积变化忽略不计),则 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】常温下将pH均为3,体积均为V0的HA和HB溶液,分别加水稀释至体积V,溶液pH随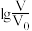 的变化如图所示。
的变化如图所示。

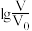 的变化如图所示。
的变化如图所示。
| A.稀释相同倍数时:c(A-)>c(B-) | B.水的电离程度:b=c<a |
| C.溶液中离子的总物质的量:b>a>c | D.溶液中离子的总浓度:a>b>c |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列溶液一定呈中性的是
A. 的溶液 的溶液 | B.溶液中 |
| C.使石蕊溶液呈紫色的溶液 | D.酸与碱恰好完全反应生成正盐的溶液 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,相同物质的量浓度的NaCN和NaClO相比,NaCN溶液的pH较大,则常温同体积同物质的量浓度的HCN和HClO溶液,下列有关说法不正确的是
| A.pH:HClO<HCN |
| B.电离程度:HCN<HClO |
| C.酸根离子浓度:c(CN-)<c(ClO-) |
| D.与相同条件的NaOH溶液恰好完全反应时,消耗NaOH的物质的量:HClO>HCN |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】某学习小组研究某酸性工业废水样品,以下实验操作或分析结论中,正确的是
| A.用玻璃棒蘸取废水样品,沾在用蒸馏水润湿的pH试纸上测定其pH |
| B.将无色酚酞试液滴入废水样品中以验证其酸性 |
C.该工业废水中 c c c |
D.测得废水样品的 ,说明该废水样品中 c ,说明该废水样品中 c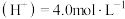 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.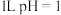 的 的 溶液中,所含的 溶液中,所含的 离子总数为 离子总数为 |
B.一定条件下,在某一恒容密闭容器中, 和 和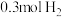 充分反应后,生成的 充分反应后,生成的 分子总数为 分子总数为 |
C. 溶液中,所含的阳离子总数大于 溶液中,所含的阳离子总数大于 |
D. 溶液中,所含的 溶液中,所含的 分子总数为 分子总数为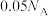 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】缓冲溶液可以抗御少量酸碱对溶液pH的影响。人体血液里最主要的缓冲体系是碳酸氢盐缓冲体系(H2CO3/HCO3-),维持血液的pH保持稳定。已知在人体正常体温时,反应H2CO3 HCO3-+H+的Ka=10-6.1,正常人的血液中c(HCO3-):c(H2CO3)≈20:1,lg2=0.3。则下列判断正确的是
HCO3-+H+的Ka=10-6.1,正常人的血液中c(HCO3-):c(H2CO3)≈20:1,lg2=0.3。则下列判断正确的是
 HCO3-+H+的Ka=10-6.1,正常人的血液中c(HCO3-):c(H2CO3)≈20:1,lg2=0.3。则下列判断正确的是
HCO3-+H+的Ka=10-6.1,正常人的血液中c(HCO3-):c(H2CO3)≈20:1,lg2=0.3。则下列判断正确的是| A.正常人血液内Kw=10-14 |
| B.由题给数据可算得正常人血液的pH约为7.4 |
| C.正常人血液中存在:c(HCO3-)+c(OH-)+2c(CO32-)=c(H+)+c(H2CO3) |
| D.当过量的碱进入血液中时,只有发生HCO3-+OH-=CO32-+H2O的反应 |
您最近半年使用:0次

 的电离方程式是:
的电离方程式是: ,
, ,
, 逆向移动,
逆向移动, 减小
减小 溶液温度升高20℃,溶液pH增大
溶液温度升高20℃,溶液pH增大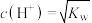 的溶液一定呈中性
的溶液一定呈中性

