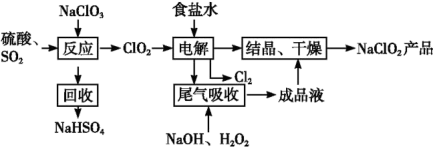
高铁酸钾(K2FeO4)是一种可溶于水,具有极强氧化性的高效多功能水处理剂,也可作高容量电池材料。回答下列问题:
(1)高铁酸钾中铁元素的化合价为___________ 。
(2)工业上通常先用干法制备高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,析出高铁酸钾。干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2==2Na2FeO4+2Na2O+2Na2SO4+O2↑。该反应中还原剂为_______________ 。低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾,其原因是_________________ 。
(3)常温下,高铁酸钾能氧化浓盐酸生成氯气,该反应离子方程式为___ 。
(4)比亚迪双模电动汽车使用高铁电池供电,其电池反应为3Zn+2K2FeO4+8H2O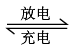 3Zn(OH)2+2Fe(OH)3+4KOH。放电时,负极反应式为
3Zn(OH)2+2Fe(OH)3+4KOH。放电时,负极反应式为_______________________________________ ,正极附近溶液的pH变__________ (填“大”或“小”)。
(5)工业上可用K2FeO4溶液氧化废水中的还原性污染物M,为研究反应效果,设计如下所示的对比实验探究温度、浓度、pH对降解速率和反应效果的影响,实验测得M的浓度与时间关系如图所示。
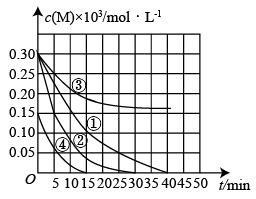
实验①中前25 min内M的反应速率为_____________________ ;其他条件相同时,实验①、②说明温度越高,M的反应速率越_________ (填“大”或“小”);其他条件相同时,实验①、③说明pH越大,M的反应速率越_________ (填“大”或“小”)。
(1)高铁酸钾中铁元素的化合价为
(2)工业上通常先用干法制备高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,析出高铁酸钾。干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2==2Na2FeO4+2Na2O+2Na2SO4+O2↑。该反应中还原剂为
(3)常温下,高铁酸钾能氧化浓盐酸生成氯气,该反应离子方程式为
(4)比亚迪双模电动汽车使用高铁电池供电,其电池反应为3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH。放电时,负极反应式为
3Zn(OH)2+2Fe(OH)3+4KOH。放电时,负极反应式为(5)工业上可用K2FeO4溶液氧化废水中的还原性污染物M,为研究反应效果,设计如下所示的对比实验探究温度、浓度、pH对降解速率和反应效果的影响,实验测得M的浓度与时间关系如图所示。

实验编号 | 温度(℃) | pH |
① | 25 | 1 |
② | 45 | 1 |
③ | 25 | 7 |
④ | 25 | 1 |
更新时间:2019-09-07 20:53:06
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】次磷酸(H3PO2)是一种精细磷化工产品,具有较强的还原性。回答下列问题:
(1)H3PO2是一元中强酸,写出其电离方程式____________________ 。
(2)H3PO2和NaH2PO2均可将溶液中的Ag+还原为Ag,从而可用于化学镀银。
①H3PO2中,P元素的化合价为_____________ 。
②NaH2PO2为________ (填 “正盐”或“酸式盐”),其溶液显______ (填“弱酸性”、 “中性”或“弱碱性”)。
③利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产 物为_____ (填化学式)。
(1)H3PO2是一元中强酸,写出其电离方程式
(2)H3PO2和NaH2PO2均可将溶液中的Ag+还原为Ag,从而可用于化学镀银。
①H3PO2中,P元素的化合价为
②NaH2PO2为
③利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产 物为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】二氧化碳的捕集和利用是我国能源领域实现碳达峰、碳中和目标的一个重要研究方向。
(1)某校科研人员利用NaOH溶液实现“碳捕获”的技术的装置如图:
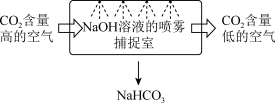
①在整个“捕捉”过程中,将NaOH溶液喷成雾状是为了___________ ,发生的离子方程式为___________ ;
②若将NaHCO3溶液进行处理,从而实现NaOH溶液的循环利用,可采取的措施为___________ 。
③下列溶液中,同样能用于“捕捉”二氧化碳的是___________ (填序号)。
A.KNO3溶液 B.CaCl2溶液 C.CuSO4溶液 D.Na2CO3溶液
(2)科学家提出用FeO作催化剂,利用太阳能热化学循环分解CO2制取C。用FeO作催化剂,通过两步反应分解CO2制取C。已知第二步反应为: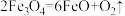 ,则第一步反应的化学方程式为
,则第一步反应的化学方程式为___________ 。
(3)《JournalofEnergyChemistry》杂志报道我国科学家设计的CO2熔盐捕获与转化电解装置如图所示。以下说法正确的是___________ (填序号)。

A.电解总反应为CO2 C+O2
C+O2
B.①②中捕获CO2时碳元素化合价发生了变化
C.转移1mol电子理论上可捕获CO25.6L
(4)科研人员发现CO2捕获和转化还可以通过如下途径实现,其原理如图所示。
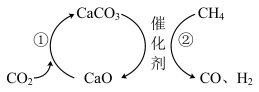
请写出过程②的化学方程式___________ 。
(1)某校科研人员利用NaOH溶液实现“碳捕获”的技术的装置如图:

①在整个“捕捉”过程中,将NaOH溶液喷成雾状是为了
②若将NaHCO3溶液进行处理,从而实现NaOH溶液的循环利用,可采取的措施为
③下列溶液中,同样能用于“捕捉”二氧化碳的是
A.KNO3溶液 B.CaCl2溶液 C.CuSO4溶液 D.Na2CO3溶液
(2)科学家提出用FeO作催化剂,利用太阳能热化学循环分解CO2制取C。用FeO作催化剂,通过两步反应分解CO2制取C。已知第二步反应为:
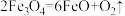 ,则第一步反应的化学方程式为
,则第一步反应的化学方程式为(3)《JournalofEnergyChemistry》杂志报道我国科学家设计的CO2熔盐捕获与转化电解装置如图所示。以下说法正确的是

A.电解总反应为CO2
 C+O2
C+O2B.①②中捕获CO2时碳元素化合价发生了变化
C.转移1mol电子理论上可捕获CO25.6L
(4)科研人员发现CO2捕获和转化还可以通过如下途径实现,其原理如图所示。

请写出过程②的化学方程式
您最近一年使用:0次
【推荐1】饮用水中的NO,对人类健康会产生危害,为了降低饮用水中NO 的浓度,可以在碱性条件下用铝粉将NO,还原为N2,其化学方程式为:Al+NaNO3+NaOH=NaAlO2+N2+H2O。
的浓度,可以在碱性条件下用铝粉将NO,还原为N2,其化学方程式为:Al+NaNO3+NaOH=NaAlO2+N2+H2O。
(1)请配平该反应_____________
(2)上述反应中,____________ 元素的化合价升高,则该元素的原子________ (填“得到”或“失去”)电子。
(3)用“单线桥法”表示反应中电子转移的方向和数目________ 。
 的浓度,可以在碱性条件下用铝粉将NO,还原为N2,其化学方程式为:Al+NaNO3+NaOH=NaAlO2+N2+H2O。
的浓度,可以在碱性条件下用铝粉将NO,还原为N2,其化学方程式为:Al+NaNO3+NaOH=NaAlO2+N2+H2O。(1)请配平该反应
(2)上述反应中,
(3)用“单线桥法”表示反应中电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】毫无疑问,从元素化合价 和物质类别 这两个角度学习、研究物质的性质,是一种行之有效的、科学的探究方法。图示是氯元素相关二维部分信息图,请完成下列问题:

(1)根据图中信息,写出+5 价和 +7 价氯的氧化物 的化学式:_______ ;_______ 。
(2)写出氯酸与氢氧化钾反应的化学方程式:_______ 。
(3)根据价态理论,HCl既具有氧化性,又具有还原性。
①请任意写出一个体现HCl氧化性的离子方程式:_______ 。
②浓盐酸在加热条件下可与NaClO发生反应制备Cl2,写出该反应的化学方程式:_______ 。
(4)Cl2既具有氧化性,又具有还原性。
①请结合图中的信息说明原因:_______ 。
②某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合溶液,经测定ClO-、ClO 的个数比为1:3,则氯气与氢氧化钠反应时,被还原的氯原子和被氧化的氯原子的个数比为:
的个数比为1:3,则氯气与氢氧化钠反应时,被还原的氯原子和被氧化的氯原子的个数比为:_______ 。

(1)根据图中信息,写出
(2)写出氯酸与氢氧化钾反应的化学方程式:
(3)根据价态理论,HCl既具有氧化性,又具有还原性。
①请任意写出一个体现HCl氧化性的离子方程式:
②浓盐酸在加热条件下可与NaClO发生反应制备Cl2,写出该反应的化学方程式:
(4)Cl2既具有氧化性,又具有还原性。
①请结合图中的信息说明原因:
②某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合溶液,经测定ClO-、ClO
 的个数比为1:3,则氯气与氢氧化钠反应时,被还原的氯原子和被氧化的氯原子的个数比为:
的个数比为1:3,则氯气与氢氧化钠反应时,被还原的氯原子和被氧化的氯原子的个数比为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】已知下列反应:
①SO2+H2O=H2SO3 ②C+H2O=H2+CO
③2A1+6H+=2A13++3H2↑ ④2Mg+CO2 2MgO+C
2MgO+C
⑤2Na2O2+2H2O=4NaOH+O2↑ ⑥Ca2C2+2H2O=Ca(OH)2+C2H2↑
(1)上述反应中不属于氧化还原反应的有___________ (填各反应的序号,下同);反应物中H2O被还原的是___________ :还原产物为单质的是___________ 。
(2)①②④反应中涉及的所有物质中属于电解质的有___________ (填物质化学式)。
(3)用单线桥表示反应④中电子转移的方向和数目___________ 。
(4)反应⑤中每生成1个O2转移的电子数目为___________ 。
①SO2+H2O=H2SO3 ②C+H2O=H2+CO
③2A1+6H+=2A13++3H2↑ ④2Mg+CO2
 2MgO+C
2MgO+C⑤2Na2O2+2H2O=4NaOH+O2↑ ⑥Ca2C2+2H2O=Ca(OH)2+C2H2↑
(1)上述反应中不属于氧化还原反应的有
(2)①②④反应中涉及的所有物质中属于电解质的有
(3)用单线桥表示反应④中电子转移的方向和数目
(4)反应⑤中每生成1个O2转移的电子数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)铁丝和铜丝缠绕在一起放入浓硝酸中,一段时间后有气体冒出,此时负极反应的电极方程式为_______ 。
(2)如图所示,某种氢氧燃料电池工作时A极上发生的电极反应为: ,B极发生
,B极发生_______ (填“氧化”或“还原”)反应,电子从该极_______ (填“流入”或“流出”),电极反应式为_______ 。
_______ ,实验②与实验①相比产生的相同体积气体,所需时间不同的原因是_______ ,温度不同的原因是_______ 。
(1)铁丝和铜丝缠绕在一起放入浓硝酸中,一段时间后有气体冒出,此时负极反应的电极方程式为
(2)如图所示,某种氢氧燃料电池工作时A极上发生的电极反应为:
 ,B极发生
,B极发生
| 时间/min | 实验① | 实验② | ||
| 气体体积/mL | 溶液温度/℃ | 气体体积/mL | 溶液温度/℃ | |
| 0 | 0 | 22.0 | 0 | 22.0 |
| 8.5 | 30 | 24.8 | 50 | 23.8 |
| 10.5 | 30 | 26.0 | — | — |

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】I.完成下列问题
(1)对于Fe+2HCl=FeCl2+H2↑,改变下列条件对生成氢气的速率有何影响?(填“增大”“减小”或“不变”)
①增大铁的质量:___________ ;
②增加盐酸体积:___________ ;
③把铁片改成铁粉:___________ ;
④滴入几滴CuSO4溶液:___________ ;
⑤加入NaCl固体:___________ ;
⑥加入一定体积的Na2SO4溶液:___________ 。
(2)一定温度下,反应N2(g)+O2(g) 2NO(g)在密闭容器中进行,回答下列措施对化学反应速率的影响(填“增大”“减小”或“不变”)。
2NO(g)在密闭容器中进行,回答下列措施对化学反应速率的影响(填“增大”“减小”或“不变”)。
⑦缩小体积使压强增大:___________ ;
⑧恒容充入N2:___________ ;
⑨恒容充入He:___________ ;
⑩恒压充入He:___________ 。
II.某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。该小组设计了如下方案。
(3)已知反应后H2C2O4转化为CO2逸出,KMnO4溶液转化为MnSO4,每消耗1molH2C2O4转移___________ mol电子。为了观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为n(H2C2O4)∶n(KMnO4)≥___________ 。
(1)对于Fe+2HCl=FeCl2+H2↑,改变下列条件对生成氢气的速率有何影响?(填“增大”“减小”或“不变”)
①增大铁的质量:
②增加盐酸体积:
③把铁片改成铁粉:
④滴入几滴CuSO4溶液:
⑤加入NaCl固体:
⑥加入一定体积的Na2SO4溶液:
(2)一定温度下,反应N2(g)+O2(g)
 2NO(g)在密闭容器中进行,回答下列措施对化学反应速率的影响(填“增大”“减小”或“不变”)。
2NO(g)在密闭容器中进行,回答下列措施对化学反应速率的影响(填“增大”“减小”或“不变”)。⑦缩小体积使压强增大:
⑧恒容充入N2:
⑨恒容充入He:
⑩恒压充入He:
II.某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。该小组设计了如下方案。
| 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
| 浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL | ||
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】把在空气中久置的镁条7.2 g投入盛有500 mL 0.5 mol·L-1硫酸溶液的烧杯中,镁条与硫酸反应产生氢气的速率与反应时间如图所示,回答下列问题:

(1)曲线由0→a段不产生氢气的原因________ ,有关的离子方程式为______________ ;
(2)曲线由b→c段,产生氢气的速率逐渐增大的主要原因________________ ;
(3)曲线由c以后,产生氢气的速率逐渐下降的主要原因________________ 。
(4)在b到c这段时间内,收集到氢气V L(标准状况),则这段时间内用硫酸表示的平均速率为________ mol/(L·s)(假设反应前后溶液体积不变)。
(5)对于足量镁条和100 mL 2 mol/L硫酸生成氢气的反应,下列措施能减缓反应速率,但又不影响生成氢气的总量的是________ 。
①加NaOH固体;②加BaCl2溶液;③加KNO3溶液;④加H2O;⑤加CH3COONa固体;⑥加小苏打溶液;⑦加少量CuSO4溶液;⑧加Na2SO4溶液;⑨将2 mol/L硫酸换成160 mL 2.5 mol/L的盐酸;⑩将镁条换成镁粉。

(1)曲线由0→a段不产生氢气的原因
(2)曲线由b→c段,产生氢气的速率逐渐增大的主要原因
(3)曲线由c以后,产生氢气的速率逐渐下降的主要原因
(4)在b到c这段时间内,收集到氢气V L(标准状况),则这段时间内用硫酸表示的平均速率为
(5)对于足量镁条和100 mL 2 mol/L硫酸生成氢气的反应,下列措施能减缓反应速率,但又不影响生成氢气的总量的是
①加NaOH固体;②加BaCl2溶液;③加KNO3溶液;④加H2O;⑤加CH3COONa固体;⑥加小苏打溶液;⑦加少量CuSO4溶液;⑧加Na2SO4溶液;⑨将2 mol/L硫酸换成160 mL 2.5 mol/L的盐酸;⑩将镁条换成镁粉。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】控制适合的条件,将反应2Fe3++2I-  2Fe2++I2设计成如图所示的原电池。回答下列问题:
2Fe2++I2设计成如图所示的原电池。回答下列问题:
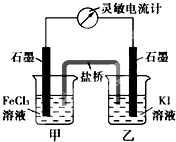
(1)反应开始时,乙中石墨电极上发生________ 反应(填“氧化”或“还原”),盐桥中的阴离子移向________ (填“甲”或“乙”)烧杯。
(2)反应开始时,甲中石墨电极上的电极反应式为________ 。
(3)反应达到化学平衡状态时,电流计指针________ 偏转。(填“是”或“否”)。
(4)反应达到平衡状态后,在甲中溶入FeCl2固体,乙中石墨电极为________ 极。
 2Fe2++I2设计成如图所示的原电池。回答下列问题:
2Fe2++I2设计成如图所示的原电池。回答下列问题:
(1)反应开始时,乙中石墨电极上发生
(2)反应开始时,甲中石墨电极上的电极反应式为
(3)反应达到化学平衡状态时,电流计指针
(4)反应达到平衡状态后,在甲中溶入FeCl2固体,乙中石墨电极为
您最近一年使用:0次
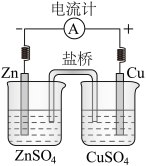
【推荐2】有关电化学示意图如下。回答下列问题:
(1)图中正极的电极反应是______ ;当Zn片的质量减少0.65g时,外电路中有_____ mol电子通过。
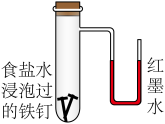
(2)预测图中U形管的实验现象是______ ;结合化学用语解释产生现象的原因____ 。
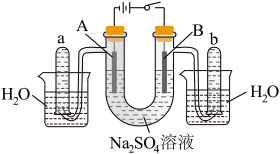
(3)用石墨电极电解滴加紫色石蕊溶液的稀Na2SO4溶液,通电后A、B两极均有无色气体生成,装置如图所示:
①NaOH在______ 极生成(填“A”或“B”)。
②B极发生反应的类型为______ 反应(填“氧化”或“还原”)。
(1)图中正极的电极反应是

(2)预测图中U形管的实验现象是

(3)用石墨电极电解滴加紫色石蕊溶液的稀Na2SO4溶液,通电后A、B两极均有无色气体生成,装置如图所示:

①NaOH在
②B极发生反应的类型为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下图为相互串联的三个装置,试回答:

(1)写出甲池负极的电极反应式:___________ 。
(2)若利用乙池在铁片上镀银,则B电极反应式是___________ 。
(3)若利用乙池进行粗铜的电解精炼,则___________ 极(填“A”或“B”)是粗铜。
(4)向丙池溶液中滴加几滴酚酞试液,___________ 电极(填“石墨”或“Fe”)周围先出现红色;若甲池消耗3.2g CH3OH气体,则丙池中阳极上产生气体的体积(标准状态)为___________ 。

(1)写出甲池负极的电极反应式:
(2)若利用乙池在铁片上镀银,则B电极反应式是
(3)若利用乙池进行粗铜的电解精炼,则
(4)向丙池溶液中滴加几滴酚酞试液,
您最近一年使用:0次