A、B、C、D四种短周期元素,它们的核电荷数依次增大;A元素原子核外只有一个电子;C元素的焰色反应呈黄色;B元素原子L层电子数是K层电子数的3倍;D原子核中的质子数比C多6个。
回答:
⑴.A是____ ,B是_____ 。
⑵.C元素最高价氧化物对应水化物的化学式为________ 。
⑶C和D形成的化合物的化学键类型为______ 。(填“离子键”或“共价键”)
⑷.D元素在周期表中的位置是第____ 周期第_____ 族。
回答:
⑴.A是
⑵.C元素最高价氧化物对应水化物的化学式为
⑶C和D形成的化合物的化学键类型为
⑷.D元素在周期表中的位置是第
11-12高二上·广西南宁·阶段练习 查看更多[1]
(已下线)2011-2012学年广西武鸣高中高二上学期段考化学(文)试卷
更新时间:2011-12-12 19:16:23
|
相似题推荐
【推荐1】R、W、X、Y、Z是原子序数依次增大的前四周期元素,其中R与W位于同一周期,且R元素的第一电离能大于氧,W的单质在暗处与 能剧烈化合,常温下X的单质为淡黄色固体,含Y元素的物质灼烧时焰色为紫色,基态Z原子有5个未成对电子。请回答下列问题:
能剧烈化合,常温下X的单质为淡黄色固体,含Y元素的物质灼烧时焰色为紫色,基态Z原子有5个未成对电子。请回答下列问题:
(1)基态Z原子的价层电子排布式为__________ ,该元素位于元素周期表中的__________ 区。
(2)基态R原子中有__________ 个未成对电子,其中能量最高的电子所在原子轨道的电子云轮廓图为__________ 形。
(3)R、W、X三种元素中第一电离能由大到小的顺序为____ (用元素符号表示),原因是________ 。
(4)R、W、X、Y、Z中非金属元素形成的最简单气态氢化物的稳定性由强到弱的顺序是__________ (填化学式)。
(5)X、Y两种元素组成的化合物 的电子式为
的电子式为__________ ,其中含有的化学键类型为__________ 。
 能剧烈化合,常温下X的单质为淡黄色固体,含Y元素的物质灼烧时焰色为紫色,基态Z原子有5个未成对电子。请回答下列问题:
能剧烈化合,常温下X的单质为淡黄色固体,含Y元素的物质灼烧时焰色为紫色,基态Z原子有5个未成对电子。请回答下列问题:(1)基态Z原子的价层电子排布式为
(2)基态R原子中有
(3)R、W、X三种元素中第一电离能由大到小的顺序为
(4)R、W、X、Y、Z中非金属元素形成的最简单气态氢化物的稳定性由强到弱的顺序是
(5)X、Y两种元素组成的化合物
 的电子式为
的电子式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】元素周期表是打开物质世界奥秘之门的一把金钥匙 ,1869 年门捷列夫发现了元素周期律并发表了元素周期表,下表是元素周期表的一部分。
(1)上述元素中化学性质最稳定的是_______ (填元素符号,下同 ),最轻的金属_______ 是制造电池的理想物质。
(2)h元素的原子结构示意图为_____ ,写出 h 单质的一种用途______ 。
(3) c、d、As 三种元素的最简单氢化物的稳定性为_____ ; c 、d、f、i 的简单离子半径由大到小顺序是____ 。
(4)e与j 组成的化合物是自然界中常见的矿石一萤石的主要成分,用电子式表示该物质______ 。
(5)元素f与g的最高价氧化物对应的水化物反应的化学方程式是_______ 。
(6)由d、f、i三种元素组成的化合物M的水溶液是一种生活中常见的消毒剂。As可与M的碱性溶液反应,当消耗lmol还原剂时,消耗2.5mol氧化剂,转移5mol电子。则该反应的离子方程式为______ 。
a | |||||||||||||||||
b | c | d | e | ||||||||||||||
f | g | h | i | ||||||||||||||
j | As |
(2)h元素的原子结构示意图为
(3) c、d、As 三种元素的最简单氢化物的稳定性为
(4)e与j 组成的化合物是自然界中常见的矿石一萤石的主要成分,用电子式表示该物质
(5)元素f与g的最高价氧化物对应的水化物反应的化学方程式是
(6)由d、f、i三种元素组成的化合物M的水溶液是一种生活中常见的消毒剂。As可与M的碱性溶液反应,当消耗lmol还原剂时,消耗2.5mol氧化剂,转移5mol电子。则该反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】Q、R、X、Y、Z五种元素的原子序数依次递增。已知:①Z的原子序数为29,其余的均为短周期主族元素;②Y原子价电子(外围电子)排布msnmpn ③R原子核外L层电子数为奇数;④Q、X原子p轨道的电子数分别为2和4。
请回答下列问题:
(1)基态原子Z的电子排布式是_______ 。
(2)在[Z(NH3)4]2+离子中, NH3提供_______ 。
(3)QX2的电子式_______ ,一种由X和R组成的化合物与QX2互为等电子体,其化学式为_______ 。
(4)比较X的氢化物与同主族相邻元素所形成的氢化物稳定性_______ ,(填化学式),并说明理由_______ 。
请回答下列问题:
(1)基态原子Z的电子排布式是
(2)在[Z(NH3)4]2+离子中, NH3提供
(3)QX2的电子式
(4)比较X的氢化物与同主族相邻元素所形成的氢化物稳定性
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D为原子序数依次增大的四种短周期元素,其性质或结构信息如下表:
试回答以下问题
(1)B在周期表中的位置是_____ 。B的氢化物与E的氢化物比较,沸点较高的是___ (填化学式),在水中溶解度较大的是_____ (填化学式)
(2)写出D3B与甲反应所得溶液呈_______ (填“酸性”、“碱性”或“中性”),原因是(用化学方程式表示)_________ 。
(3)写出丙的电子式为______ 。说明丙的水溶液在放置过程中其酸性会增强的原因(用离子方程式表示)___________ 。
(4)由A、B、C、D四种元素中的三种元素组成的一种盐丁,其外观与氯化钠相似,丁的水溶液呈碱性。可用来鉴别丁和氯化钠的试剂有_____ 。
A.氢碘酸和淀粉的混合液 B.AgNO3溶液
C.甲基橙试剂 D.稀硫酸
(5)将光亮的铜丝插入丁溶液中,没有现象发生,如用盐酸酸化,反应迅速发生,铜丝缓慢溶解生成深绿色溶液,写出该反应的离子方程式_____________ 。
| 元素 | A | B | C | D | |
| 性质或结构信息 | 室温下单质呈气态。原子最外层电子数与D相同 | D3B中阳离子与阴离子的电子层结构相同 | A和C可形成两种常见的化合物甲和乙,乙具有弱酸性 | 单质质软,银白色固体。导电性强.在空气中燃烧生成淡黄色固体 | E是一种气态氧化物丙,丙相对于空气的密度为3.0,溶解于水可得只含单一溶质的弱酸性溶液,该溶液在光照条件下放置酸性会增强 |
(1)B在周期表中的位置是
(2)写出D3B与甲反应所得溶液呈
(3)写出丙的电子式为
(4)由A、B、C、D四种元素中的三种元素组成的一种盐丁,其外观与氯化钠相似,丁的水溶液呈碱性。可用来鉴别丁和氯化钠的试剂有
A.氢碘酸和淀粉的混合液 B.AgNO3溶液
C.甲基橙试剂 D.稀硫酸
(5)将光亮的铜丝插入丁溶液中,没有现象发生,如用盐酸酸化,反应迅速发生,铜丝缓慢溶解生成深绿色溶液,写出该反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】有关元素X、Y、D、E的信息如下:
用化学用语 回答下列问题:
(1)D在元素周期表中的位置为____ 。
(2)X、Y、D形成的简单离子的半径由大到小为_____ 。
(3)X的一种氢化物可用于实验室制取X的单质,其反应的化学方程式为_________ ,D的单质溶于强碱的离子方程式为________ 。
(4)E元素与Y元素可形成EY2和EY3两种化合物,下列说法正确的是(填序号)_____ 。
①保存EY2溶液时,需向溶液加入少量E单质
②EY2、EY3均能通过化合反应生成
③向煮沸的NaOH溶液中滴加几滴饱和EY3溶液,可以制得胶体
| 元素 | 有关信息 |
| X | 地壳中含量最高的元素 |
| Y | 第三周期中原子半径最小的元素 |
| D | 最高价氧化物既能溶于强酸又能溶于强碱 |
| E | 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
(1)D在元素周期表中的位置为
(2)X、Y、D形成的简单离子的半径由大到小为
(3)X的一种氢化物可用于实验室制取X的单质,其反应的化学方程式为
(4)E元素与Y元素可形成EY2和EY3两种化合物,下列说法正确的是(填序号)
①保存EY2溶液时,需向溶液加入少量E单质
②EY2、EY3均能通过化合反应生成
③向煮沸的NaOH溶液中滴加几滴饱和EY3溶液,可以制得胶体
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】主族元素A、B、C、D的原子序数都小于18,A与D同主族,B与C在同一周期,A、D原子的价电子数都是1,C原子最外层电子数比B原子少2个,且最外层电子数是次外层电子数的2倍。A、B的单质在常温下均为气体,它们在高温下以体积比2∶1完全反应,生成物在常温下为液体。此液体与D单质能剧烈反应生成A的单质。所得溶液滴入酚酞显红色,同时溶液中含有与氖原子的电子层结构相同的阳离子。试回答下列问题:
(1)写出元素符号:B___________ ,D___________ 。
(2)写出元素原子的价电子排布:A___________ ,C___________ 。
(3)B与C在高温下完全反应后的生成物的化学式为___________ ,它是由___________ (填“极性”或“非极性”)键形成的___________ 分子,分子的空间构型呈___________ 。
(4)A与B的单质以体积比2∶1形成的化合物的中心原子的杂化方式为___________ ,分子的空间构型呈___________ 。
(1)写出元素符号:B
(2)写出元素原子的价电子排布:A
(3)B与C在高温下完全反应后的生成物的化学式为
(4)A与B的单质以体积比2∶1形成的化合物的中心原子的杂化方式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】短周期主族元素W、X、Y、Z、M、N、Q原子序数依次增大,元素W的一种核素的中子数为0,X的原子最外层电子数是次外层的2倍,X与M同主族,Z与N同主族,Z2-电子层结构与氖原子相同。
(1)M在元素周期表中的位置是______ 。
(2)化合物p由W、X、Y、N四种元素组成。已知向p溶液中加入FeCl3溶液,溶液变血红色;向p溶液中加入NaOH溶液并加热,可放出使湿润的红色石蕊试纸变蓝的气体。p的化学式为______ 。
(3)由X、Y、Z三种元素可组成摩尔质量为84 g·mol-1的物质q,且q分子中三种元素的原子个数之比为1:1:1。已知q分子中各原子均达到8电子稳定结构,且分子中不含双键,但含极性键和非极性键,q分子的结构式为______ 。
(4)(XY)2的性质与单质Q2相似,(XY)2与NaOH溶液常温下反应的离子方程式为______ 。
(5)常温下,1 mol Z3能与Y的最简单氢化物反应,生成一种常见的含氧酸盐和1 mol Z2,该反应的化学方程式为______ 。
(6)Z元素与除M外的其余五种元素间两两形成的化合物都不止一种,写出符合下列条件的化合物分子式_____
①Z与其它原子的个数比为2:1;
②分子中电子总数为奇数
(7)用如图的装置,既可设计比较X、M、N非金属性强弱的实验,也可设计比较N、Q非金属性强弱的实验。若用强酸制弱酸的原理比较X、M、N非金属性强弱,则A装置中发生反应的化学方程式是_______ ;若用氧化还原反应原理比较N、Q非金属性强弱,则B装置中发生反应的离子方程式是________ (此空供选用的实验试剂有:KMnO4固体、MnO2固体、稀盐酸、浓盐酸、Na2S溶液、Na2SO3溶液、NaOH溶液)。
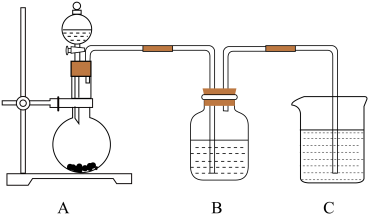
(1)M在元素周期表中的位置是
(2)化合物p由W、X、Y、N四种元素组成。已知向p溶液中加入FeCl3溶液,溶液变血红色;向p溶液中加入NaOH溶液并加热,可放出使湿润的红色石蕊试纸变蓝的气体。p的化学式为
(3)由X、Y、Z三种元素可组成摩尔质量为84 g·mol-1的物质q,且q分子中三种元素的原子个数之比为1:1:1。已知q分子中各原子均达到8电子稳定结构,且分子中不含双键,但含极性键和非极性键,q分子的结构式为
(4)(XY)2的性质与单质Q2相似,(XY)2与NaOH溶液常温下反应的离子方程式为
(5)常温下,1 mol Z3能与Y的最简单氢化物反应,生成一种常见的含氧酸盐和1 mol Z2,该反应的化学方程式为
(6)Z元素与除M外的其余五种元素间两两形成的化合物都不止一种,写出符合下列条件的化合物分子式
①Z与其它原子的个数比为2:1;
②分子中电子总数为奇数
(7)用如图的装置,既可设计比较X、M、N非金属性强弱的实验,也可设计比较N、Q非金属性强弱的实验。若用强酸制弱酸的原理比较X、M、N非金属性强弱,则A装置中发生反应的化学方程式是

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】B、C、D、E、F是原子序数依次增大的短周期主族元素,B是短周期中金属性最强的元素,C是同周期中离子半径最小的元素,D元素的最高价氧化物对应水化物与B元素的最高价氧化物对应水化物反应的产物M是制备木材防火剂的原料,E的最外层电子数与内层电子数之比为3﹕5。请回答:
(1)D的原子结构示意图为___________________ 。
(2)写出工业制F单质的化学方程式:___________________ 。
(3)用电子式表示元素B与元素F形成的化合物:___________________ 。
(4)B单质与氧气反应的产物与C的单质同时放入水中,产生两种无色气体,有关的化学方程式为____________________ 、___________________ 。
(5)写出M与盐酸反应的离子方程式:___________________ 。
(6)工业上将干燥的F单质通入熔融的E单质中可制得化合物E2F2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为___________________ 。
(1)D的原子结构示意图为
(2)写出工业制F单质的化学方程式:
(3)用电子式表示元素B与元素F形成的化合物:
(4)B单质与氧气反应的产物与C的单质同时放入水中,产生两种无色气体,有关的化学方程式为
(5)写出M与盐酸反应的离子方程式:
(6)工业上将干燥的F单质通入熔融的E单质中可制得化合物E2F2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】四种短周期主族元素X、Y、Z、R的原子序数与原子半径关系如图1所示,且原子序数均不超过10.由这四种元素组成一种电解质溶剂的分子结构如图2所示。
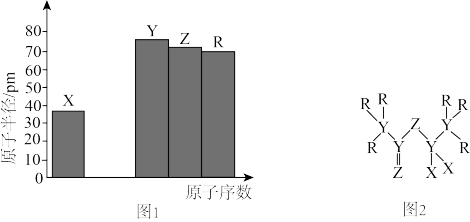
请回答下列问题:
(1)基态Y原子核外电子最高能级的电子云轮廓图为___________ 。
(2)X、Y、Z能组成多种二元或三元化合物。写出一种符合下列条件的结构简式:
①所有原子共直线的烃类且相对分子质量最小:___________ 。
②既能与溴反应,又能与 溶液反应的烃的衍生物:
溶液反应的烃的衍生物:___________ 。
③σ键、π键数目之比等于 的四原子分子:
的四原子分子:___________ 。
④碳原子有3种杂化类型且相对分子质量最小的链状烃:___________ 。
(3)Y和Z组成的简单阴离子空间构型是___________ 。
(4)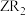 分子的VSEPR模型为
分子的VSEPR模型为___________ 。
(5)R与碱金属元素组成的化合物熔点与碱金属原子序数的关系如图3所示。
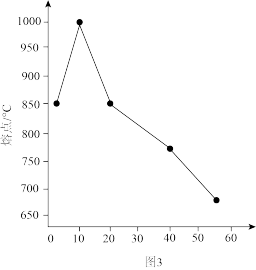
氟化钠、氟化钾、氟化铷、氟化铯的熔点依次降低,其主要原因是___________ 。在上述碱金属元素的氟化物中,离子键百分数最大的是___________ (填名称)。

请回答下列问题:
(1)基态Y原子核外电子最高能级的电子云轮廓图为
(2)X、Y、Z能组成多种二元或三元化合物。写出一种符合下列条件的结构简式:
①所有原子共直线的烃类且相对分子质量最小:
②既能与溴反应,又能与
 溶液反应的烃的衍生物:
溶液反应的烃的衍生物:③σ键、π键数目之比等于
 的四原子分子:
的四原子分子:④碳原子有3种杂化类型且相对分子质量最小的链状烃:
(3)Y和Z组成的简单阴离子空间构型是
(4)
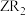 分子的VSEPR模型为
分子的VSEPR模型为(5)R与碱金属元素组成的化合物熔点与碱金属原子序数的关系如图3所示。

氟化钠、氟化钾、氟化铷、氟化铯的熔点依次降低,其主要原因是
您最近一年使用:0次



