用高效的二氧化氯(ClO2)替代液氯进行消毒,可避免产生对人体健康有害的有机氯代物。
(1)工业上,ClO2常用NaClO3和Na2SO3溶液混合并加硫酸酸化后反应制得,则化学反应方程式为___ ,在该反应中NaClO3和Na2SO3的物质的量之比为________ 。
(2)有效氯含量是含氯消毒剂的一个重要指标,有效氯含量的定义:从HI中氧化出相同量的I2所需Cl2的质量与指定含氯消毒剂的质量之比,常用百分数表示。则ClO2的有效氯含量是________ 。
(3)化学小组的同学欲对用ClO2消毒过的自来水进行氯元素含量的测定(假定ClO2全部转化为Cl-),他们进行了如下实验:向30.00 mL水样中加几滴K2CrO4溶液作指示剂,用0.001 mol·L-1AgNO3溶液滴定,当有砖红色Ag2CrO4沉淀出现时,达滴定终点,此时用去AgNO3溶液12.12 mL。
①水样中Cl-的物质的量浓度是________ 。
②已知Ksp(AgCl)=1.780×10-10,Ksp(Ag2CrO4)=2.00×10-12。如在滴定终点时,测得溶液中CrO42-的浓度是5.000×10-3mol·L-1。试计算此时溶液中Cl-的浓度是________ 。
(1)工业上,ClO2常用NaClO3和Na2SO3溶液混合并加硫酸酸化后反应制得,则化学反应方程式为
(2)有效氯含量是含氯消毒剂的一个重要指标,有效氯含量的定义:从HI中氧化出相同量的I2所需Cl2的质量与指定含氯消毒剂的质量之比,常用百分数表示。则ClO2的有效氯含量是
(3)化学小组的同学欲对用ClO2消毒过的自来水进行氯元素含量的测定(假定ClO2全部转化为Cl-),他们进行了如下实验:向30.00 mL水样中加几滴K2CrO4溶液作指示剂,用0.001 mol·L-1AgNO3溶液滴定,当有砖红色Ag2CrO4沉淀出现时,达滴定终点,此时用去AgNO3溶液12.12 mL。
①水样中Cl-的物质的量浓度是
②已知Ksp(AgCl)=1.780×10-10,Ksp(Ag2CrO4)=2.00×10-12。如在滴定终点时,测得溶液中CrO42-的浓度是5.000×10-3mol·L-1。试计算此时溶液中Cl-的浓度是
更新时间:2019-09-24 07:49:22
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】铬渣(主要含Cr2O3 ,还有Fe2O3、Al2O3、SiO2 等杂质)是铬电镀过程中产生的含铬污泥,实现其综合利用可减少铬产生的环境污染。铬渣的综合利用工艺流程如下:
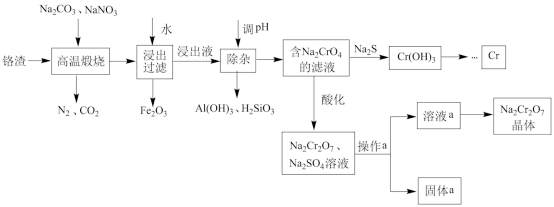
试回答下列问题:
(1)高温煅烧时,Cr2O3参与反应的化学方程式为__________ 。
(2)“浸出液”调pH时加入的试剂最好为________ ,除杂时生成Al(OH)3的离子方程式为________ 。
(3)加入Na2S时,硫元素全部以S2O32-形式存在,写出该反应的离子方程式: ._______
(4)根据图1溶解度信息可知,操作a包含蒸发结晶和______ 。固体a化学式为________
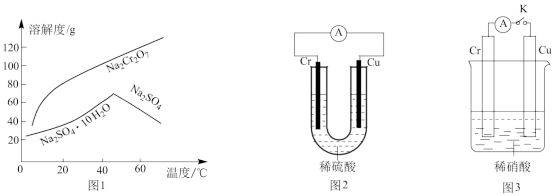
(5)设计如图装置探究铬的性质,观察到图2装置中铜电极上产生大量的无色气泡,根据上述现象试推测金属铬的化学性质:________ 。在图3装置中当开关K断开时,铬电极无现象,K闭合时,铬电极上产生大量无色气体,然后气体变为红棕色,根据上述现象试推测金属铬的化学性质:__________ 。
(6)工业上处理酸性Cr2O72-废水多采用铁氧磁体法,该法是向废水中加入FeSO4.7H2O将Cr2O72-还原成Cr3+ ,调节pH,使Fe、Cr转化成相当于FeⅠⅠ[FexⅡCr(2-x)Ⅲ]O4(铁氧磁体,罗马数字表示元素价态)的沉淀。每处理1 mol Cr2O72- ,需加入a molFeSO4·7H2O,下列结论正确的是________ . (填字母)。
A x=0.5,a=6 B x=0.5,a= 10 C x=1.5,a=6 D x=1.5,a=10

试回答下列问题:
(1)高温煅烧时,Cr2O3参与反应的化学方程式为
(2)“浸出液”调pH时加入的试剂最好为
(3)加入Na2S时,硫元素全部以S2O32-形式存在,写出该反应的离子方程式: .
(4)根据图1溶解度信息可知,操作a包含蒸发结晶和

(5)设计如图装置探究铬的性质,观察到图2装置中铜电极上产生大量的无色气泡,根据上述现象试推测金属铬的化学性质:
(6)工业上处理酸性Cr2O72-废水多采用铁氧磁体法,该法是向废水中加入FeSO4.7H2O将Cr2O72-还原成Cr3+ ,调节pH,使Fe、Cr转化成相当于FeⅠⅠ[FexⅡCr(2-x)Ⅲ]O4(铁氧磁体,罗马数字表示元素价态)的沉淀。每处理1 mol Cr2O72- ,需加入a molFeSO4·7H2O,下列结论正确的是
A x=0.5,a=6 B x=0.5,a= 10 C x=1.5,a=6 D x=1.5,a=10
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】某炼锌的有机物钴渣逐级分离与富集钴的工艺流程如图:
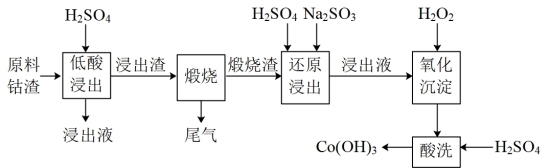
已知:
①原料钴渣的主要成分:钴的有机盐[(C3H6NS2)2Co]、ZnSO4•6H2O和Fe4(OH)2(SO4)5。
②“煅烧渣”中钴元素的主要成分:CoO、Co3O4和CoSO4。
③部分阳离子以氢氧化物形式沉淀时溶液的pH如表:
回答下列问题:
(1)Fe4(OH)2(SO4)5中铁元素的化合价为____ 。
(2)低酸浸出液中,主要的金属阳离子为____ 。
(3)“煅烧”的主要目的是____ 。
(4)“还原浸出”时,钴元素发生还原反应的离子方程式为_____ 。
(5)已知电位差△E>0时,“氧化沉淀”反应可以发生,△E越大,反应越容易进行。△E=E(H2O2/H2O)-E[(Co(Ⅲ)/Co(Ⅱ)]、E(H2O2/H2O)、E[(Co(Ⅲ)/Co(Ⅱ)]与pH的关系如图。“氧化沉淀”时,向还原浸出液添加试剂的正确操作为____ (选填序号),理由是_____ 。
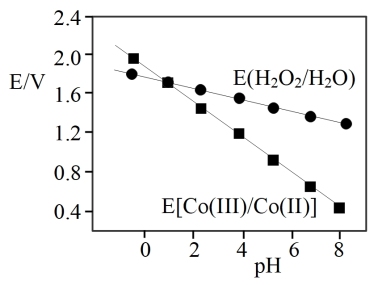
a.直接加入H2O2
b.先加入NaOH溶液,调节pH,再加入H2O2
c.先加入H2SO4溶液,调节pH,再加入H2O2
(6)“酸洗”可除去钴渣中少量Fe(OH)3、Zn(OH)2等杂质,应控制溶液的pH范围为____ 。

已知:
①原料钴渣的主要成分:钴的有机盐[(C3H6NS2)2Co]、ZnSO4•6H2O和Fe4(OH)2(SO4)5。
②“煅烧渣”中钴元素的主要成分:CoO、Co3O4和CoSO4。
③部分阳离子以氢氧化物形式沉淀时溶液的pH如表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Co(OH)3 | Zn(OH)2 |
| 开始沉淀 | 2.2 | 7.4 | 5.9 | -1.1 | 6.2 |
| 完全沉淀 | 3.2 | 8.9 | 9.2 | 1.1 | 8.0 |
(1)Fe4(OH)2(SO4)5中铁元素的化合价为
(2)低酸浸出液中,主要的金属阳离子为
(3)“煅烧”的主要目的是
(4)“还原浸出”时,钴元素发生还原反应的离子方程式为
(5)已知电位差△E>0时,“氧化沉淀”反应可以发生,△E越大,反应越容易进行。△E=E(H2O2/H2O)-E[(Co(Ⅲ)/Co(Ⅱ)]、E(H2O2/H2O)、E[(Co(Ⅲ)/Co(Ⅱ)]与pH的关系如图。“氧化沉淀”时,向还原浸出液添加试剂的正确操作为

a.直接加入H2O2
b.先加入NaOH溶液,调节pH,再加入H2O2
c.先加入H2SO4溶液,调节pH,再加入H2O2
(6)“酸洗”可除去钴渣中少量Fe(OH)3、Zn(OH)2等杂质,应控制溶液的pH范围为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】碘是人体必需的微量元素,在医药和工业中都有广泛用途,因此从含碘废液中回收碘充分利用二次资源是非常重要的。实验室从含碘废液(除H2O外,含有CCl4、I2、I-)中回收碘,其实验过程如图1:(已知氧化性Cl2> IO3-)
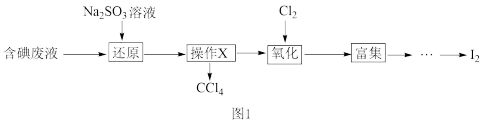
(1)向含碘废液中加入稍过量的Na2SO3溶液,反应的离子方程式为_________ ,该操作将I2还原为I-的目的是_________________________________________ 。
(2)操作X的名称为______________________________________ 。
(3)氧化时,在三颈烧瓶中将含I-的水溶液用盐酸调至pH约为2,通入Cl2,在40℃左右反应(实验装置如图2所示)。下列有关说法正确的是_____ (填字母)。

a.在实验中要缓慢通入氯气。提高氯气的利用率,防止产生污染
b.控制在较低温度下进行的主要原因是增大氯气的溶解度
c.通入过量的氯气可提高碘的产量
d.为有效防止碘的挥发水应从b口通入
e.锥形瓶中应盛放NaOH溶液
(4)二氧化氯(C1O2,黄绿色易溶于水的气体)是高效、低毒的消毒剂和水处理剂。现用C1O2氧化酸性含I-废液回收碘。
①写出C1O2氧化I-的离子方程式____________________________________ 。
②若处理含I-相同量的废液回收碘、所需Cl2的物质的量是C1O2的______________ 倍。
(5)已知:5SO32-+2IO3-+2H+ I2+5SO42-+H2O。某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO3-中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO3-的实验方案:(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)
I2+5SO42-+H2O。某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO3-中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO3-的实验方案:(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)
①取适量含碘废水用CCl4多次萃取、分液,直到水层检验不出碘单质存在;
②_______________________ ;
③另从水层取少量溶液,加入2-3滴淀粉溶液,滴加________________ (填试剂和现象)。说明废水中含有IO3-,否则说明废水中不含IO3-。

(1)向含碘废液中加入稍过量的Na2SO3溶液,反应的离子方程式为
(2)操作X的名称为
(3)氧化时,在三颈烧瓶中将含I-的水溶液用盐酸调至pH约为2,通入Cl2,在40℃左右反应(实验装置如图2所示)。下列有关说法正确的是

a.在实验中要缓慢通入氯气。提高氯气的利用率,防止产生污染
b.控制在较低温度下进行的主要原因是增大氯气的溶解度
c.通入过量的氯气可提高碘的产量
d.为有效防止碘的挥发水应从b口通入
e.锥形瓶中应盛放NaOH溶液
(4)二氧化氯(C1O2,黄绿色易溶于水的气体)是高效、低毒的消毒剂和水处理剂。现用C1O2氧化酸性含I-废液回收碘。
①写出C1O2氧化I-的离子方程式
②若处理含I-相同量的废液回收碘、所需Cl2的物质的量是C1O2的
(5)已知:5SO32-+2IO3-+2H+
 I2+5SO42-+H2O。某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO3-中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO3-的实验方案:(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)
I2+5SO42-+H2O。某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO3-中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO3-的实验方案:(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)①取适量含碘废水用CCl4多次萃取、分液,直到水层检验不出碘单质存在;
②
③另从水层取少量溶液,加入2-3滴淀粉溶液,滴加
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】工业上以软锰矿(主要成分为MnO2,另含有少量FeCO3、Al2O3、SiO2)为原料制取金属锰的工艺流程如下:

(1)“粉磨”的目的是_______ 。
(2)写出“滤渣1”的一种用途_______ 。
(3)“滤渣2”的主要成分是_______ (填化学式),“沉锰”过程_______ (填“能”或“不能”)用Na2CO3代替NH4HCO3。
(4)经检测,“浸取液”中无Fe2+,“浸取”时MnO2发生反应的离子方程式为_______ 。
(5)在“沉锰”操作中发生反应的离子方程式为_______ 。

(6)为测定“滤渣2”中铝元素的含量,设计以下方案:
①将m g滤渣2处理成a mL溶液;
②取少量①中溶液用EDTA滴定测得溶液中Fe3+、Al3+的浓度之和为b mmol/L;
③另取少量①中溶液,用盐酸羟胺将Fe3+还原为Fe2+;
④将③所得溶液利用吸光度法测得其吸光度为0.400(吸光度与Fe2+的浓度关系如下图所示)。该样品中Al元素的质量分数为_______ (用含字母的表达式表示,不必化简)。

(1)“粉磨”的目的是
(2)写出“滤渣1”的一种用途
(3)“滤渣2”的主要成分是
(4)经检测,“浸取液”中无Fe2+,“浸取”时MnO2发生反应的离子方程式为
(5)在“沉锰”操作中发生反应的离子方程式为

(6)为测定“滤渣2”中铝元素的含量,设计以下方案:
①将m g滤渣2处理成a mL溶液;
②取少量①中溶液用EDTA滴定测得溶液中Fe3+、Al3+的浓度之和为b mmol/L;
③另取少量①中溶液,用盐酸羟胺将Fe3+还原为Fe2+;
④将③所得溶液利用吸光度法测得其吸光度为0.400(吸光度与Fe2+的浓度关系如下图所示)。该样品中Al元素的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】过氧化钙遇水具有放氧的特性,且本身无毒,不污染环境,是一种用途广泛的优良供氧剂,在工农业生产中有广泛的用途。
I.过氧化钙的制备:将 溶于水中,在搅拌下加入
溶于水中,在搅拌下加入 ,再通入氨气进行反应可制备
,再通入氨气进行反应可制备 ,在碱性环境下制取
,在碱性环境下制取 的装置如下:
的装置如下:

(1)写制备 的化学方程式
的化学方程式___________ ;
(2)X仪器的名称为___________ ;
(3)乙中沉淀反应时常用冰水浴控制温度在0℃左右,其可能的原因分析:其一,该反应是放热反应,温度低有利于提高 的产率;其二:
的产率;其二:___________ ;
(4)反应结束后,经过滤、洗涤、低温烘干可获得 。检验
。检验 是否洗涤干净的操作为
是否洗涤干净的操作为___________ 。
II.水产运输中常向水中加一定量 增加溶氧量(DO),水中溶氧量(DO)是用每升水中溶解氧气的质量来表示,其测定步骤及原理如下:
增加溶氧量(DO),水中溶氧量(DO)是用每升水中溶解氧气的质量来表示,其测定步骤及原理如下:
a.固氧:碱性下, 将
将 氧化为
氧化为 :
: ;
;
b.氧化:酸性下, 将
将 氧化为
氧化为 ;
;
c.滴定:用 标准溶液滴定生成的
标准溶液滴定生成的 :
: 。某同学向100.00mL水中加一定量
。某同学向100.00mL水中加一定量 ,取此水样50.00mL,按上述方法测定水中溶氧量(DO),消耗
,取此水样50.00mL,按上述方法测定水中溶氧量(DO),消耗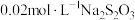 标准溶液15.00mL。
标准溶液15.00mL。
(5)滴定过程中使用的指示剂是___________ ;
(6)请写出步骤b中的离子方程式___________ ;
(7)该水样中的溶氧量(DO)为___________  (忽略体积变化)。
(忽略体积变化)。
I.过氧化钙的制备:将
 溶于水中,在搅拌下加入
溶于水中,在搅拌下加入 ,再通入氨气进行反应可制备
,再通入氨气进行反应可制备 ,在碱性环境下制取
,在碱性环境下制取 的装置如下:
的装置如下:
(1)写制备
 的化学方程式
的化学方程式(2)X仪器的名称为
(3)乙中沉淀反应时常用冰水浴控制温度在0℃左右,其可能的原因分析:其一,该反应是放热反应,温度低有利于提高
 的产率;其二:
的产率;其二:(4)反应结束后,经过滤、洗涤、低温烘干可获得
 。检验
。检验 是否洗涤干净的操作为
是否洗涤干净的操作为II.水产运输中常向水中加一定量
 增加溶氧量(DO),水中溶氧量(DO)是用每升水中溶解氧气的质量来表示,其测定步骤及原理如下:
增加溶氧量(DO),水中溶氧量(DO)是用每升水中溶解氧气的质量来表示,其测定步骤及原理如下:a.固氧:碱性下,
 将
将 氧化为
氧化为 :
: ;
;b.氧化:酸性下,
 将
将 氧化为
氧化为 ;
;c.滴定:用
 标准溶液滴定生成的
标准溶液滴定生成的 :
: 。某同学向100.00mL水中加一定量
。某同学向100.00mL水中加一定量 ,取此水样50.00mL,按上述方法测定水中溶氧量(DO),消耗
,取此水样50.00mL,按上述方法测定水中溶氧量(DO),消耗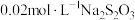 标准溶液15.00mL。
标准溶液15.00mL。(5)滴定过程中使用的指示剂是
(6)请写出步骤b中的离子方程式
(7)该水样中的溶氧量(DO)为
 (忽略体积变化)。
(忽略体积变化)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】NaBiO3可作为测定锰的氧化剂,Bi2O3在电子行业有着广泛应用,可利用浮选过的辉铋矿(主要成分是Bi2S3,还含少量SiO2等杂质)来制备,工艺流程如下:

已知:NaBiO3难溶于水。
回答下列问题
(1)溶液Ⅰ中主要成分为BiCl3、FeCl2,则滤渣Ⅰ的主要成分是________ (写化学式)。
(2)海绵铋与盐酸、H2O2反应的化学方程式是__________
(3)向溶液Ⅲ中加入NaOH和NaClO发生反应的离于方程式是______ ,从反应后的混合体系中获得纯净NaBiO3,操作Ⅱ包括_________ 。
(4)一定温度下,向氨水中通入CO2,得到 (NH4)2CO3、NH4HCO3等物质,溶液中各种微粒的物质的量分数与pH的关系如图所示。随着CO2的通入,溶液中c(OH-)/c(NH3·H2O)将______ (填“增大”“减小”或“不变”)。pH=9时,溶液中c(NH4+)+c(H+)=______ (用离子浓度表示)。

(5)取所得NaBiO3样品2.0g,加入稀硫酸和MnSO4溶液使其完全溶解,然后用新配制的0.5mol/LFeSO4溶液滴定生成的MnO4-,滴定完成后消耗22.00mLFeSO4溶液。则该样晶中NaBiO3纯度为_________ 。

已知:NaBiO3难溶于水。
回答下列问题
(1)溶液Ⅰ中主要成分为BiCl3、FeCl2,则滤渣Ⅰ的主要成分是
(2)海绵铋与盐酸、H2O2反应的化学方程式是
(3)向溶液Ⅲ中加入NaOH和NaClO发生反应的离于方程式是
(4)一定温度下,向氨水中通入CO2,得到 (NH4)2CO3、NH4HCO3等物质,溶液中各种微粒的物质的量分数与pH的关系如图所示。随着CO2的通入,溶液中c(OH-)/c(NH3·H2O)将

(5)取所得NaBiO3样品2.0g,加入稀硫酸和MnSO4溶液使其完全溶解,然后用新配制的0.5mol/LFeSO4溶液滴定生成的MnO4-,滴定完成后消耗22.00mLFeSO4溶液。则该样晶中NaBiO3纯度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】铅及其化合物用途广泛,请回答下列相关问题:
(1)铅元素(82Pb)位于周期表中第_______ 周期,基态价电子排布式为_______ 。相同温度下,同浓度的Na2PbO3溶液碱性比Na2CO3溶液碱性_______ (填“强”或“弱”)。
(2)工业上利用铅浮渣(主要成分是PbO2、Pb,含有少量Ag、CaO和其他不溶于硝酸的杂质)生产硫酸铅和硫化铅纳米粒子,流程如图所示:
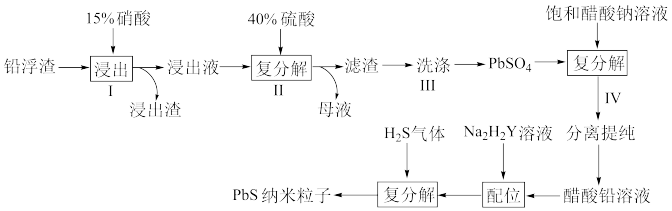
已知:25℃时,Ksp(CaSO4)=4.9×10−5,Ksp(PbSO4)=1.6×10−8,Ksp(PbS)=1.0×10−28。
①已知步骤Ⅰ有NO产生,Pb被稀硝酸氧化成Pb2+。写出Pb参加反应的离子方程式:_______ 。
②步骤Ⅰ需控制硝酸的用量并使Pb稍有剩余,浸出渣的成分除了不溶于硝酸的杂质和铅外,还主要有_______ 。
③步骤Ⅲ需用Pb(NO3)2溶液多次洗涤硫酸铅的原因是_______ 。
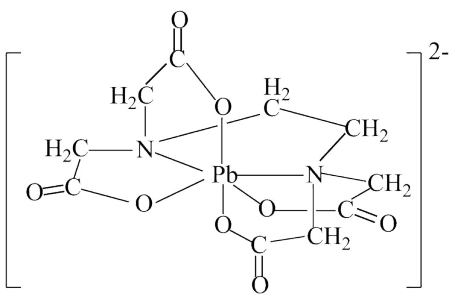
④EDTA二钠简写成Na2H2Y,可以与Pb2+形成稳定的配离子,其结构如图,此配离子内所含作用力除σ键外,还有_______ 。
⑤PbS晶胞与NaCl晶胞相同,则S2−的配位数是_______ 。
(1)铅元素(82Pb)位于周期表中第
(2)工业上利用铅浮渣(主要成分是PbO2、Pb,含有少量Ag、CaO和其他不溶于硝酸的杂质)生产硫酸铅和硫化铅纳米粒子,流程如图所示:

已知:25℃时,Ksp(CaSO4)=4.9×10−5,Ksp(PbSO4)=1.6×10−8,Ksp(PbS)=1.0×10−28。
①已知步骤Ⅰ有NO产生,Pb被稀硝酸氧化成Pb2+。写出Pb参加反应的离子方程式:
②步骤Ⅰ需控制硝酸的用量并使Pb稍有剩余,浸出渣的成分除了不溶于硝酸的杂质和铅外,还主要有
③步骤Ⅲ需用Pb(NO3)2溶液多次洗涤硫酸铅的原因是
④EDTA二钠简写成Na2H2Y,可以与Pb2+形成稳定的配离子,其结构如图,此配离子内所含作用力除σ键外,还有

⑤PbS晶胞与NaCl晶胞相同,则S2−的配位数是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】硫酸锌是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应用。工业上利用菱锌矿(主要成分为ZnCO3,还含有少量SiO2及Ca、Mg、Fe、Cu、Pb等元素的化合物)制备硫酸锌晶体,工艺流程如图。
回答下列问题。
(1)“焙烧”时ZnCO3发生主要反应的化学方程式为___________ 。
(2)试剂“X”最适宜为___________ (填标号)。
A.ZnO B.NH3 C.Ca(OH)2
(3)“氧化”时保持溶液80℃~90℃,需分步加入KMnO4,充分反应,过滤;“滤渣3”中有MnO2,该步反应的离子方程式为___________ 。
(4)Pb元素在___________ 操作单元中除去。
(5)加入锌的目的是___________ 。
(6)“除钙镁”当镁离子恰好完全沉淀时,c(Ca2+)=___________ (保留两位有效数字)。[当 时认为完全沉淀]
时认为完全沉淀]
(7)“滤渣5”经浓硫酸处理可生成HF循环利用,反应的化学方程式为___________ (写一个即可)。

| 物质 | Fe(OH)3 | Zn(OH)2 | Cu(OH)2 | Fe(OH)2 | Mg(OH)2 | MgF2 | CaF2 |
| Ksp |  | 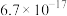 | 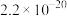 |  | 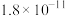 |  | 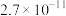 |
(1)“焙烧”时ZnCO3发生主要反应的化学方程式为
(2)试剂“X”最适宜为
A.ZnO B.NH3 C.Ca(OH)2
(3)“氧化”时保持溶液80℃~90℃,需分步加入KMnO4,充分反应,过滤;“滤渣3”中有MnO2,该步反应的离子方程式为
(4)Pb元素在
(5)加入锌的目的是
(6)“除钙镁”当镁离子恰好完全沉淀时,c(Ca2+)=
 时认为完全沉淀]
时认为完全沉淀](7)“滤渣5”经浓硫酸处理可生成HF循环利用,反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】工业上,从精制黑钨矿(FeWO4、MnWO4)中提取金属钨的一种流程如下图所示,该流程同时获取副产物Fe2O3和MnCl2。

已知:I.过程①~④中,钨的化合价均不变;
Ⅱ.常温下钨酸难溶于水;
Ⅲ.25℃时,Ksp[Fe(OH)3]=1.0×10-38,Ksp [Mn(OH)2]=4.0×10-14
回答下列问题:
(1)上述流程中的“滤渣1”除MnO2外还有_____ 、“气体”除水蒸气、HCl外还有____ (均填化学式);
(2)过程①中MnWO4参与反应的化学方程式为______ ;FeWO4参与的反应中氧化剂与还原剂的物质的量之比为___________ ;
(3)已知WO3(s)+3H2(g)=W(s)+3H2O(g) ΔH=a kJ·mol-1
WO3(s)=WO3(g) ΔH=b kJ·mol-1
写出WO3(g)与H2(g)反应生成W(s)的热化学方程式:_______ ;
(4)过程⑦在25℃时调pH,至少应调至_______ (当离子浓度等于1.0×10-5mol·L-1时,可认为其已沉淀完全);
(5)过程⑧要获得MnCl2固体,在加热时必须同时采取的一项措施是__________ ;
(6)钠钨青铜是一类特殊的非化学计量比化合物,其通式为NaxWO3,其中0<x<1,这类化合物具有特殊的物理化学性质,是一种低温超导体。应用惰性电极电解熔融的Na2WO4和WO2混合物可以制备钠钨青铜,写出WO42-在阴极上放电的电极反应式:___________ 。

已知:I.过程①~④中,钨的化合价均不变;
Ⅱ.常温下钨酸难溶于水;
Ⅲ.25℃时,Ksp[Fe(OH)3]=1.0×10-38,Ksp [Mn(OH)2]=4.0×10-14
回答下列问题:
(1)上述流程中的“滤渣1”除MnO2外还有
(2)过程①中MnWO4参与反应的化学方程式为
(3)已知WO3(s)+3H2(g)=W(s)+3H2O(g) ΔH=a kJ·mol-1
WO3(s)=WO3(g) ΔH=b kJ·mol-1
写出WO3(g)与H2(g)反应生成W(s)的热化学方程式:
(4)过程⑦在25℃时调pH,至少应调至
(5)过程⑧要获得MnCl2固体,在加热时必须同时采取的一项措施是
(6)钠钨青铜是一类特殊的非化学计量比化合物,其通式为NaxWO3,其中0<x<1,这类化合物具有特殊的物理化学性质,是一种低温超导体。应用惰性电极电解熔融的Na2WO4和WO2混合物可以制备钠钨青铜,写出WO42-在阴极上放电的电极反应式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】金属钼在工业和国防建设中有重要的作用。钼(Mo)的常见化合价为+6、+5、+4.由钼精矿(主要成分是MoS2)可制备单质钼和钼酸钠晶体(Na2MoO4•2H2O),部分流程如图所示:
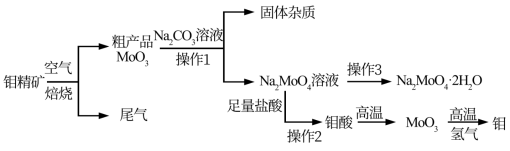
已知:钼酸微溶于水,可溶于液碱和氨水。请回答下列问题:
(1)焙烧钼精矿时发生的化学方程式为_______ 。
(2)钼精矿焙烧时排放的尾气中的SO2可以用纯碱溶液回收,请写出用足量的纯碱溶液吸收SO2的化学方程式_______ 。(已知: ;
; ;
; ;
;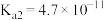 )
)
(3)操作3的结晶方式是_______ 。写出操作1的滤液中加入足量盐酸反应的离子方程式_______ 。实验室中由钼酸得到MoO3所用到的硅酸盐材质仪器的名称是_______ 。(至少2种)
(4)焙烧钼精矿所用的装置是多层焙烧炉,图为各炉层固体物料的物质的量的百分数( )。
)。
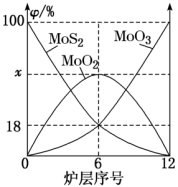
①x=_______ 。
②焙烧炉中也会发生MoS2与MoO3反应生成MoO2和SO2的反应,则该反应中氧化剂与还原剂的物质的量之比为_______ 。
(5)操作1中,加入碳酸钠溶液充分反应后,碱浸液中 ,
, ,在结晶前需加入Ba(OH)2固体以除去溶液中的
,在结晶前需加入Ba(OH)2固体以除去溶液中的 。当BaMoO4开始沉淀时,
。当BaMoO4开始沉淀时, 的去除率是
的去除率是_______ 。[ 、
、 ,溶液体积变化可忽略不计,结果保留两位有效数字]
,溶液体积变化可忽略不计,结果保留两位有效数字]

已知:钼酸微溶于水,可溶于液碱和氨水。请回答下列问题:
(1)焙烧钼精矿时发生的化学方程式为
(2)钼精矿焙烧时排放的尾气中的SO2可以用纯碱溶液回收,请写出用足量的纯碱溶液吸收SO2的化学方程式
 ;
; ;
; ;
;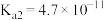 )
)(3)操作3的结晶方式是
(4)焙烧钼精矿所用的装置是多层焙烧炉,图为各炉层固体物料的物质的量的百分数(
 )。
)。
①x=
②焙烧炉中也会发生MoS2与MoO3反应生成MoO2和SO2的反应,则该反应中氧化剂与还原剂的物质的量之比为
(5)操作1中,加入碳酸钠溶液充分反应后,碱浸液中
 ,
, ,在结晶前需加入Ba(OH)2固体以除去溶液中的
,在结晶前需加入Ba(OH)2固体以除去溶液中的 。当BaMoO4开始沉淀时,
。当BaMoO4开始沉淀时, 的去除率是
的去除率是 、
、 ,溶液体积变化可忽略不计,结果保留两位有效数字]
,溶液体积变化可忽略不计,结果保留两位有效数字]
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】LiPF6是锂离子电池中广泛应用的电解质。某工厂用LiF、PCl5为原料,低温反应制备LiPF6,其流程如下:
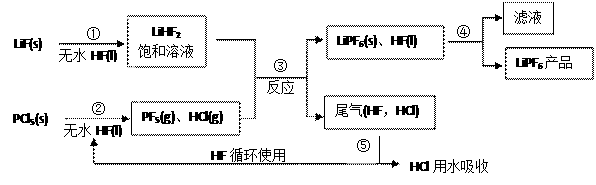
已知:HCl的沸点是—85.0℃,HF的沸点是19.5℃。
(1)第①步反应中无水HF的作用是____________ 、_____________ 。无水HF有腐蚀性和毒性,工厂安全手册提示:如果不小心将HF沾到皮肤上,可立即用2%的_______ 溶液冲洗。
(2)该流程需在无水条件下进行,第③步反应中PF5极易与水反应,其产物为两种酸,写出PF5与水反应的化学方程式:________________________________________ 。
(3)第④步分离采用的方法是_______ ;第⑤步分离尾气中HF、HCl采用的方法是_____________

已知:HCl的沸点是—85.0℃,HF的沸点是19.5℃。
(1)第①步反应中无水HF的作用是
(2)该流程需在无水条件下进行,第③步反应中PF5极易与水反应,其产物为两种酸,写出PF5与水反应的化学方程式:
(3)第④步分离采用的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】磺酰氯(SO2Cl2)是一种有机氯化剂,也是锂电池正极活性物质。已知磺酰氯是一种无色液体,熔点-54.1℃,沸点69.1℃,遇水发生剧烈水解,且产生白雾。
(1)SO2Cl2水解的方程式为_______________________________________________
(2)某学习小组的同学依据反应:SO2(g)+ Cl2(g) SO2Cl2(g);△H <0,设计制备磺酰氯装置如图:
SO2Cl2(g);△H <0,设计制备磺酰氯装置如图:

①E中所用的试剂为________________
②实验室用Na2SO3和硫酸制备SO2,可选用的气体发生装置是____ (选填编号);检查该装置气密性的操作是:关闭止水夹,再___________________________________
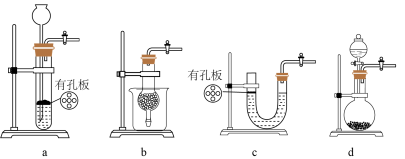
③B处反应管内五球中玻璃棉上的活性炭的作用为:_______________________ D处U形管中盛放的试剂为_________________ ,作用 :________________________
(3)已知:以下三个反应的反应热,a、b、c均为正值
①SO2(g)+Cl2(g)+SCl2(g) 2SOCl2(g) △H=-akJ·mol-1
2SOCl2(g) △H=-akJ·mol-1
②SO2Cl2(g)+SCl2(g) 2SOCl2(g) △H=-bkJ·mol-1
2SOCl2(g) △H=-bkJ·mol-1
③SO2Cl2(l) SO2Cl2(g) △H= + ckJ·mol-1
SO2Cl2(g) △H= + ckJ·mol-1
则反应:SO2(g)+Cl2(g) SO2Cl2(l) △H=
SO2Cl2(l) △H=______________ kJ·mol-1(用含a、b、c的代数式表示);该反应平衡常数表达式为K=___________ 。从化学平衡移动角度分析,反应管通水冷却的目的为____
(1)SO2Cl2水解的方程式为
(2)某学习小组的同学依据反应:SO2(g)+ Cl2(g)
 SO2Cl2(g);△H <0,设计制备磺酰氯装置如图:
SO2Cl2(g);△H <0,设计制备磺酰氯装置如图:
①E中所用的试剂为
②实验室用Na2SO3和硫酸制备SO2,可选用的气体发生装置是

③B处反应管内五球中玻璃棉上的活性炭的作用为:
(3)已知:以下三个反应的反应热,a、b、c均为正值
①SO2(g)+Cl2(g)+SCl2(g)
 2SOCl2(g) △H=-akJ·mol-1
2SOCl2(g) △H=-akJ·mol-1②SO2Cl2(g)+SCl2(g)
 2SOCl2(g) △H=-bkJ·mol-1
2SOCl2(g) △H=-bkJ·mol-1③SO2Cl2(l)
 SO2Cl2(g) △H= + ckJ·mol-1
SO2Cl2(g) △H= + ckJ·mol-1则反应:SO2(g)+Cl2(g)
 SO2Cl2(l) △H=
SO2Cl2(l) △H=
您最近一年使用:0次



