在0.l mol·L-1的CH3COOH溶液中存在电离平衡:CH3COOH CH3COO-+H+对于该平衡,下列叙述正确的是
CH3COO-+H+对于该平衡,下列叙述正确的是
 CH3COO-+H+对于该平衡,下列叙述正确的是
CH3COO-+H+对于该平衡,下列叙述正确的是| A.加入少量CH3COONa固体,平衡不移动,c(H+)不变 |
| B.加入少量NaOH固体,平衡向正向移动,溶液中c(H+)减小 |
C.加水,平衡向正向移动, 增大 增大 |
| D.通入少量HCl气体,平衡逆向移动,溶液中c(H+)减少 |
2019高二上·全国·专题练习 查看更多[1]
(已下线)2019年10月3日《每日一题》选修4—— 影响电离平衡的因素
更新时间:2019-10-09 20:41:36
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】25℃时,用HCl气体调节0.1mol•L-1氨水的pH,系统中微粒浓度的对数值(lgc)与pH的关系如图1所示,反应物的物质的量之比[x= ]与pH的关系如图2所示。若忽略通过气体后溶液体积的变化,下列有关说法正确的是
]与pH的关系如图2所示。若忽略通过气体后溶液体积的变化,下列有关说法正确的是
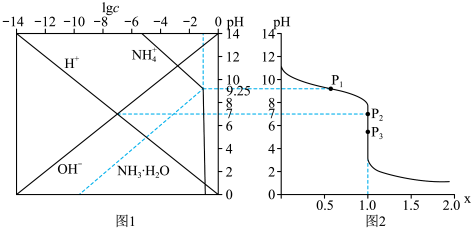
 ]与pH的关系如图2所示。若忽略通过气体后溶液体积的变化,下列有关说法正确的是
]与pH的关系如图2所示。若忽略通过气体后溶液体积的变化,下列有关说法正确的是
| A.P1所示溶液:c(Cl-)=0.05mol•L-1 |
| B.P2所示溶液:c(NH3•H2O)>c(OH-)+c(Cl-) |
C.P3所示溶液:c( )+c(NH3•H2O)=c(Cl-)+c(H+) )+c(NH3•H2O)=c(Cl-)+c(H+) |
| D.25℃时,NH3•H2O的电离平衡常数为10-4.75 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】液氨与纯水类似,也存在微弱的电离: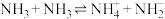 ,T℃时,液氨的离子积常数
,T℃时,液氨的离子积常数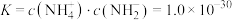 ,若用定义pH的方式来规定
,若用定义pH的方式来规定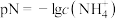 ,则下列叙述正确的是
,则下列叙述正确的是
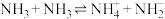 ,T℃时,液氨的离子积常数
,T℃时,液氨的离子积常数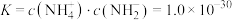 ,若用定义pH的方式来规定
,若用定义pH的方式来规定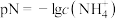 ,则下列叙述正确的是
,则下列叙述正确的是| A.其他条件不变,增加液氨的量,电离平衡正向移动 |
B.液氨达到电离平衡时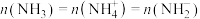 |
| C.T℃时的液氨中,pN=15 |
| D.一定温度下,向液氨中加入氯化铵固体,电离平衡逆向移动,K值减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】一定温度下,在冰醋酸中加水稀释时,溶液的导电能力的变化趋势如图所示,下列有关说法中错误的是
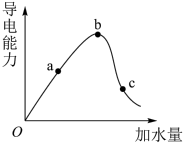
| A.稀释过程中,b点时的电离程度最大 |
| B.加水前,CH3COOH主要以分子形式存在 |
| C.a、b、c三点的pH大小关系:c>a>b |
| D.a、c点的溶液中分别加入足量的锌粉,产生H2的质量相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某浓度的醋酸溶液中存在下列平衡:CH3COOH H++CH3COO-,如想增大CH3COO-的浓度,而不增大H+的浓度,应采取的措施是
H++CH3COO-,如想增大CH3COO-的浓度,而不增大H+的浓度,应采取的措施是
①加入CH3COONa固体 ②适当升高温度 ③加冰醋酸 ④加入少量NaOH固体
 H++CH3COO-,如想增大CH3COO-的浓度,而不增大H+的浓度,应采取的措施是
H++CH3COO-,如想增大CH3COO-的浓度,而不增大H+的浓度,应采取的措施是①加入CH3COONa固体 ②适当升高温度 ③加冰醋酸 ④加入少量NaOH固体
| A.①② | B.②③ | C.②④ | D.①④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】对室温下pH相同、体积相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是
| A.加适量的醋酸钠晶体后,两者的pH均增大 | B.温度都升高后,两者pH均增大 |
| C.用湿润的pH试纸测定出的pH值醋酸更大 | D.与足量锌反应两者产生的氢气一样多 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在恒温条件下,欲使CH3COONa的稀溶液中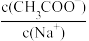 比值增大,可在溶液中加入少量下列物质中的
比值增大,可在溶液中加入少量下列物质中的
①固体NaOH ②固体KOH ③固体NaHS ④固体CH3COONa ⑤冰醋酸
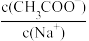 比值增大,可在溶液中加入少量下列物质中的
比值增大,可在溶液中加入少量下列物质中的①固体NaOH ②固体KOH ③固体NaHS ④固体CH3COONa ⑤冰醋酸
| A.只有①② | B.只有②⑤ | C.只有②④⑤ | D.只有①⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】向0.1mol·L-1稀盐酸中分别加入下列固体物质,溶液中c(H+)可能不变的是
| A.CH3COONa | B.AgNO3 | C.KOH | D.Zn |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,在pH=5的CH3COOH溶液中存在如下电离平衡:CH3COOH CH3COO-+H+,对于该平衡,下列叙述正确的是
CH3COO-+H+,对于该平衡,下列叙述正确的是
 CH3COO-+H+,对于该平衡,下列叙述正确的是
CH3COO-+H+,对于该平衡,下列叙述正确的是| A.加入水时,平衡向右移动,CH3COOH电离常数增大 |
| B.加入少量CH3COONa固体,平衡向右移动 |
| C.加入少量NaOH固体,平衡向右移动,c(H+)减少 |
| D.稍微升高溶液温度,溶液中的c(OH-)增大 |
您最近一年使用:0次

 的数目增多
的数目增多 的电离常数不变
的电离常数不变

 OH-+
OH-+

