大气中CO2含量的增加会加剧温室效应,为减少其排放,需将工业生产中产生的CO2分离出来进行储存和利用。
(1)CO2与NH3反应可合成化肥尿素[化学式为CO(NH2)2],反应2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(g)在合成塔中进行。如图1中Ⅰ、Ⅱ、Ⅲ三条曲线为合成塔中按不同氨碳比[
CO(NH2)2(l)+H2O(g)在合成塔中进行。如图1中Ⅰ、Ⅱ、Ⅲ三条曲线为合成塔中按不同氨碳比[ ]和水碳比[
]和水碳比[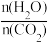 ]投料时二氧化碳转化率的情况。
]投料时二氧化碳转化率的情况。
①曲线Ⅰ、Ⅱ、Ⅲ水碳比的数值范围分别为0.6~0.7、1~1.1和1.5~1.61,则生产中应选用水碳比的数值范围为____ 。
②请推测生产中氨碳比控制在4.0左右还是控制在4.5左右比较适宜,并简述你的理由_____ 。
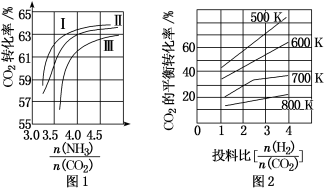
(2)CO2与H2也可用于合成甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。在体积可变的恒压密闭容器中,该反应在不同温度、不同投料比时,CO2的平衡转化率如图2所示。
CH3OH(g)+H2O(g)。在体积可变的恒压密闭容器中,该反应在不同温度、不同投料比时,CO2的平衡转化率如图2所示。
①该反应的化学平衡常数的表达式为_____ 。
②该反应的ΔS___ 0,ΔH___ 0(填“>”或“<”)。
③700K投料比[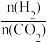 ]=2时,H2的平衡转化率为
]=2时,H2的平衡转化率为_____ 。
(1)CO2与NH3反应可合成化肥尿素[化学式为CO(NH2)2],反应2NH3(g)+CO2(g)
 CO(NH2)2(l)+H2O(g)在合成塔中进行。如图1中Ⅰ、Ⅱ、Ⅲ三条曲线为合成塔中按不同氨碳比[
CO(NH2)2(l)+H2O(g)在合成塔中进行。如图1中Ⅰ、Ⅱ、Ⅲ三条曲线为合成塔中按不同氨碳比[ ]和水碳比[
]和水碳比[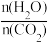 ]投料时二氧化碳转化率的情况。
]投料时二氧化碳转化率的情况。①曲线Ⅰ、Ⅱ、Ⅲ水碳比的数值范围分别为0.6~0.7、1~1.1和1.5~1.61,则生产中应选用水碳比的数值范围为
②请推测生产中氨碳比控制在4.0左右还是控制在4.5左右比较适宜,并简述你的理由

(2)CO2与H2也可用于合成甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。在体积可变的恒压密闭容器中,该反应在不同温度、不同投料比时,CO2的平衡转化率如图2所示。
CH3OH(g)+H2O(g)。在体积可变的恒压密闭容器中,该反应在不同温度、不同投料比时,CO2的平衡转化率如图2所示。①该反应的化学平衡常数的表达式为
②该反应的ΔS
③700K投料比[
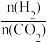 ]=2时,H2的平衡转化率为
]=2时,H2的平衡转化率为
更新时间:2019-10-15 14:40:16
|
相似题推荐
【推荐1】1100℃时,体积为2L的恒容容器中发生反应: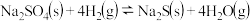
(1)下列能判断反应达到平衡状态的是______ 。
A.容器中压强不变
B.混合气体密度不变
C.1mol 键断裂同时形成2mol
键断裂同时形成2mol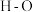
D. 的体积分数不变
的体积分数不变
(2)若2 min时反应达平衡,此时气体质量增加8g,则用 表示该反应的反应速率为
表示该反应的反应速率为_______ 。
(3)某温度下该反应达平衡状态,测得混合气体的平均相对分子质量为14,则该温度下的平衡常数K为________ 。
(4)若反应达平衡后,加入少量的 ,再次平衡后,
,再次平衡后, 的体积分数
的体积分数______  填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变” 。
。
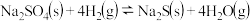
(1)下列能判断反应达到平衡状态的是
A.容器中压强不变
B.混合气体密度不变
C.1mol
 键断裂同时形成2mol
键断裂同时形成2mol
D.
 的体积分数不变
的体积分数不变(2)若2 min时反应达平衡,此时气体质量增加8g,则用
 表示该反应的反应速率为
表示该反应的反应速率为(3)某温度下该反应达平衡状态,测得混合气体的平均相对分子质量为14,则该温度下的平衡常数K为
(4)若反应达平衡后,加入少量的
 ,再次平衡后,
,再次平衡后, 的体积分数
的体积分数 填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变” 。
。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】在2 L密闭容器内,800 ℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
(1)写出该反应的平衡常数表达式:K=____________ 。
(2)如图中表示NO2的变化的曲线是__________ 。用O2表示从0~2s内该反应的平均速率v=_________ 。
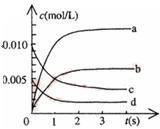
(3)能说明该反应已达到平衡状态的是_________________ 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)某同学查阅资料得知,该反应K300℃>K350℃;25 ℃时,生成1 mol NO2,热量变化为56.4 kJ。但是该同学由于疏忽,忘记注明“+”、“-”。根据题目信息,该反应的热化学方程式为_______________________ 。
(5)为使该反应的反应速率增大,且平衡向正反应方向移动的是_________ 。
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K=
(2)如图中表示NO2的变化的曲线是

(3)能说明该反应已达到平衡状态的是
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)某同学查阅资料得知,该反应K300℃>K350℃;25 ℃时,生成1 mol NO2,热量变化为56.4 kJ。但是该同学由于疏忽,忘记注明“+”、“-”。根据题目信息,该反应的热化学方程式为
(5)为使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
您最近一年使用:0次
【推荐3】一定温度下,向 恒容容器中充入
恒容容器中充入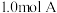 和
和 ,发生反应
,发生反应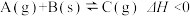 ,经过一段时间后达到平衡。反应过程中测定的部分数据如表,回答下列问题:
,经过一段时间后达到平衡。反应过程中测定的部分数据如表,回答下列问题:
(1)前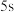 的平均反应速率
的平均反应速率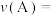
_______ ,达平衡时 的平衡体积分数为
的平衡体积分数为_______ 。
(2)由表中数据计算该温度下该反应的平衡常数为_______ ,随着反应温度升高,该反应的平衡常数_______ (选填“增大”、“减小”或“不变”)。
(3)保持温度不变,起始时向容器中充入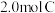 ,达平衡时,
,达平衡时, 的转化率为
的转化率为_______ 。
 恒容容器中充入
恒容容器中充入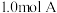 和
和 ,发生反应
,发生反应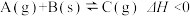 ,经过一段时间后达到平衡。反应过程中测定的部分数据如表,回答下列问题:
,经过一段时间后达到平衡。反应过程中测定的部分数据如表,回答下列问题:
|
|
|
|
|
|
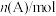 |
|
|
|
|
|
(1)前
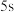 的平均反应速率
的平均反应速率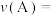
 的平衡体积分数为
的平衡体积分数为(2)由表中数据计算该温度下该反应的平衡常数为
(3)保持温度不变,起始时向容器中充入
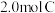 ,达平衡时,
,达平衡时, 的转化率为
的转化率为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】425℃时,向某V L的密闭容器中充入2molH2(g)和2mol I2(g)发生反应: H2(g)+I2(g) 2HI(g)
2HI(g) =-26.5kJ/mol,测得各物质的物质的量浓度与时间变化的关系如图所示。
=-26.5kJ/mol,测得各物质的物质的量浓度与时间变化的关系如图所示。
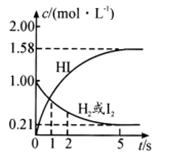
请回答下列问题:
(1)V=__________ .
(2)该反应达到最大限度了的时间是____________ ,该时间内平均反应速率v(HI)=________________ 。
(3)该反应达到平衡状态时,__________ (填“吸收”或“放出”)的热量为__________ 。
 2HI(g)
2HI(g) =-26.5kJ/mol,测得各物质的物质的量浓度与时间变化的关系如图所示。
=-26.5kJ/mol,测得各物质的物质的量浓度与时间变化的关系如图所示。
请回答下列问题:
(1)V=
(2)该反应达到最大限度了的时间是
(3)该反应达到平衡状态时,
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】I将等物质的量的A、B混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g)  xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
(1)反应开始前容器中的A、B的物质的量:n(A)=n(B)=__________ mol;
(2)前5 min内用B表示的平均反应速率v(B)=_____________ ;
(3)化学反应方程式中x的值为________ 。
II 一定条件下,反应室(容积恒定为2 L)中有反应:A(g)+2B(g) C(g)。
C(g)。
(4)能说明上述反应达到平衡状态的是__________ (填字母,下同)。
A 反应中A与B的物质的量浓度之比为1∶2
B 混合气体总物质的量不再变化
C 混合气体的密度不随时间的变化而变化
D 2v正(A)=v逆(B)
(5)1 mol A(g)与2 mol B(g)在催化剂作用下在反应室反应生成C(g),A的平衡转化率与温度、压强的关系如图所示:
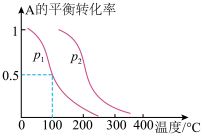
①p1__________ (填“<”、“>”或“=”,下同)p2,正反应的ΔH__________ 0。
②下列措施中一定能使c(C)/c(A)增大的是__________ 。
A 升高温度 B 恒温恒容再充入A
C 恒温恒容再充入B D 恒温恒容再充入1 mol C
(6)100 ℃时将1 mol A和2 mol B通入反应室,保持温度不变,10 min末C(g)的浓度为0.05 mol·L-1,则10 min末B的转化率为__________ ,此时v正__________ (填“<”、“>”或“=”)v逆。
 xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:(1)反应开始前容器中的A、B的物质的量:n(A)=n(B)=
(2)前5 min内用B表示的平均反应速率v(B)=
(3)化学反应方程式中x的值为
II 一定条件下,反应室(容积恒定为2 L)中有反应:A(g)+2B(g)
 C(g)。
C(g)。(4)能说明上述反应达到平衡状态的是
A 反应中A与B的物质的量浓度之比为1∶2
B 混合气体总物质的量不再变化
C 混合气体的密度不随时间的变化而变化
D 2v正(A)=v逆(B)
(5)1 mol A(g)与2 mol B(g)在催化剂作用下在反应室反应生成C(g),A的平衡转化率与温度、压强的关系如图所示:

①p1
②下列措施中一定能使c(C)/c(A)增大的是
A 升高温度 B 恒温恒容再充入A
C 恒温恒容再充入B D 恒温恒容再充入1 mol C
(6)100 ℃时将1 mol A和2 mol B通入反应室,保持温度不变,10 min末C(g)的浓度为0.05 mol·L-1,则10 min末B的转化率为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】已知甲烷隔绝空气在不同温度下有可能发生如下两个反应:①CH4(g)=C(s)+2H2(g),②2CH4(g)=C2H2(g)+3H2(g)。某同学为了得到用天然气制取炭黑的允许温度范围和最佳温度,在图书馆查到了如下热力学数据:
①的ΔH(298 K)=74.848 kJ·mol-1,ΔS(298 K)=80.674 J·mol-1·K-1
②的ΔH(298 K)=376.426 kJ·mol-1,ΔS(298 K)=220.211 J·mol-1·K-1
已知焓变和熵变随温度变化很小。请帮助这位同学考虑如下问题:
(1)判断②反应是高温自发还是低温自发:___________ (填“高温”或“低温”)。
(2)通过计算判断①反应在常温下能否自发进行:___________ 。
(3)求算制取炭黑的允许温度范围:___________ 。
(4)为了提高甲烷的碳化程度,你认为下面四个温度中最合适的是___________(填字母)。
①的ΔH(298 K)=74.848 kJ·mol-1,ΔS(298 K)=80.674 J·mol-1·K-1
②的ΔH(298 K)=376.426 kJ·mol-1,ΔS(298 K)=220.211 J·mol-1·K-1
已知焓变和熵变随温度变化很小。请帮助这位同学考虑如下问题:
(1)判断②反应是高温自发还是低温自发:
(2)通过计算判断①反应在常温下能否自发进行:
(3)求算制取炭黑的允许温度范围:
(4)为了提高甲烷的碳化程度,你认为下面四个温度中最合适的是___________(填字母)。
| A.905.2 K | B.927 K |
| C.1 273 K | D.2 000 K |
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】(1)已知在 、
、 时,反应
时,反应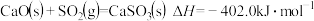 ,
,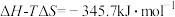 ,若该反应的
,若该反应的 和
和 不随温度变化而变化,则保持该反应能自发进行的温度应低于
不随温度变化而变化,则保持该反应能自发进行的温度应低于_______ (结果保留整数)。
(2)已知: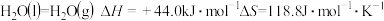 ,则水的沸点是
,则水的沸点是_______ (结果保留1位小数)。
(3)已知在 时,由石墨转化为金刚石的反应的
时,由石墨转化为金刚石的反应的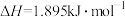 ,
,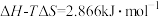 ,石墨的熵S石
,石墨的熵S石 ,则金刚石的熵S金=
,则金刚石的熵S金=________ ,这两种碳的同素异形体中更有序的是________ 。
 、
、 时,反应
时,反应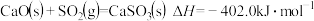 ,
,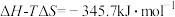 ,若该反应的
,若该反应的 和
和 不随温度变化而变化,则保持该反应能自发进行的温度应低于
不随温度变化而变化,则保持该反应能自发进行的温度应低于(2)已知:
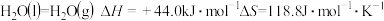 ,则水的沸点是
,则水的沸点是(3)已知在
 时,由石墨转化为金刚石的反应的
时,由石墨转化为金刚石的反应的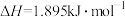 ,
,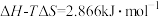 ,石墨的熵S石
,石墨的熵S石 ,则金刚石的熵S金=
,则金刚石的熵S金=
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】反应A(g) 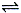 B(g) +C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:
B(g) +C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:
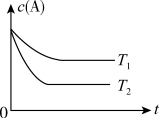
(1)上述反应的温度T1____ T2,平衡常数K(T1)____ K(T2)。(填“大于”、“小于”或“等于”)
(2)若温度T2时,5min后反应达到平衡,A的转化率为70%,则:
①平衡时体系总的物质的量为________ 。
②反应的平衡常数K=_______ 。
③反应在0~5min区间的平均反应速率v(A)=________ 。
(3)已知1g FeS2完全燃烧放出7.1kJ热量,FeS2燃烧反应的热化学方程式为______ 。
(4)物质(t-BuNO)2在正庚烷溶剂中发生如下反应:(t-BuNO)2 2(t-BuNO) ΔH = 50.5 kJ·mol-1。该反应的ΔS
2(t-BuNO) ΔH = 50.5 kJ·mol-1。该反应的ΔS_____ 0(填“>”、“<”或“=”)。在______ 填“较高”或“较低”)温度下有利于该反应自发进行。
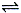 B(g) +C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:
B(g) +C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:
(1)上述反应的温度T1
(2)若温度T2时,5min后反应达到平衡,A的转化率为70%,则:
①平衡时体系总的物质的量为
②反应的平衡常数K=
③反应在0~5min区间的平均反应速率v(A)=
(3)已知1g FeS2完全燃烧放出7.1kJ热量,FeS2燃烧反应的热化学方程式为
(4)物质(t-BuNO)2在正庚烷溶剂中发生如下反应:(t-BuNO)2
 2(t-BuNO) ΔH = 50.5 kJ·mol-1。该反应的ΔS
2(t-BuNO) ΔH = 50.5 kJ·mol-1。该反应的ΔS
您最近一年使用:0次

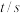



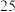
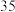

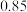
 xC(g)+2D(g)。经5min后达到平衡,平衡时测得D的浓度为0.5mol/L,c(A):c(B)=3:5,v(C)=0.1mol/(L·min)。则:
xC(g)+2D(g)。经5min后达到平衡,平衡时测得D的浓度为0.5mol/L,c(A):c(B)=3:5,v(C)=0.1mol/(L·min)。则:

