Ⅰ. 由中科院等离子体物理研究所自主研制的全超导托卡马克实验装置(俗称“人造太阳”)正在接受技术升级。人造太阳是利用氘、氚核聚变反应释放巨大能量原理而实现的。下列说法正确的是________ 。
A.氕、氘、氚三种元素在周期表中的位置不同
B.20 g D2O含有的中子数为6.02×1024个
C.在隔绝空气和高温下LiCl与金属钠反应可获得金属锂
Ⅱ. 部分元素在周期表中的位置如下:
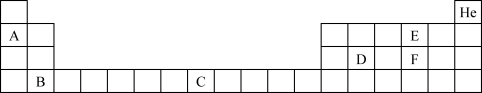
请回答下列问题:
(1)元素C在周期表中的位置为________ 。
(2)判断E和F对应的简单氢化物沸点高低,并解释原因____________ 。
(3)用电子式表示F的氢化物的形成过程:___________ 。
Ⅲ.溴及其化合物广泛用于医药、塑料阻燃剂等,苦卤提溴的工业流程如下:
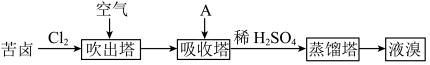
(1)结合元素周期律解释Cl的非金属性强于Br的原因:_______________ 。
(2)吸收塔中,A吸收了Br2后的溶液中含有Br−和BrO3−,则A是________ (填序号)。
A.NaCl溶液 B.Na2CO3溶液 C.SO2气体
(3)从吸收塔出来的溶液中加入稀H2SO4得到Br2的离子方程式是______ 。
A.氕、氘、氚三种元素在周期表中的位置不同
B.20 g D2O含有的中子数为6.02×1024个
C.在隔绝空气和高温下LiCl与金属钠反应可获得金属锂
Ⅱ. 部分元素在周期表中的位置如下:

请回答下列问题:
(1)元素C在周期表中的位置为
(2)判断E和F对应的简单氢化物沸点高低,并解释原因
(3)用电子式表示F的氢化物的形成过程:
Ⅲ.溴及其化合物广泛用于医药、塑料阻燃剂等,苦卤提溴的工业流程如下:

(1)结合元素周期律解释Cl的非金属性强于Br的原因:
(2)吸收塔中,A吸收了Br2后的溶液中含有Br−和BrO3−,则A是
A.NaCl溶液 B.Na2CO3溶液 C.SO2气体
(3)从吸收塔出来的溶液中加入稀H2SO4得到Br2的离子方程式是
更新时间:2019-10-22 08:39:24
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.物质分类的思想、反应类别的分类在化学学习中有非常重要的作用,根据题目要求回答下列有关问题:
(1)①石墨 ②液氯 ③浓盐酸 ④ 溶液 ⑤漂白粉 ⑥熔融的
溶液 ⑤漂白粉 ⑥熔融的 ⑦
⑦ ⑧氯化钠晶体 ⑨乙醇,其中属于电解质的是
⑧氯化钠晶体 ⑨乙醇,其中属于电解质的是_______ ,属于非电解质的是_______ ,能导电的是_______ 。(填序号)
Ⅱ.已知:①
②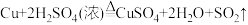
③
(2)当反应①转移 电子时,消耗
电子时,消耗 的质量是
的质量是_______ g,产生氢气的体积 (标准状况)_______ L。
(3)当反应②中生成 气体(标准状况下)时,被还原的
气体(标准状况下)时,被还原的 的物质的量
的物质的量_______ 。
(4)用单线桥法表示反应②电子转移的方向和数目(在化学方程式上标出)_______ 。
(1)①石墨 ②液氯 ③浓盐酸 ④
 溶液 ⑤漂白粉 ⑥熔融的
溶液 ⑤漂白粉 ⑥熔融的 ⑦
⑦ ⑧氯化钠晶体 ⑨乙醇,其中属于电解质的是
⑧氯化钠晶体 ⑨乙醇,其中属于电解质的是Ⅱ.已知:①

②
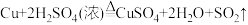
③

(2)当反应①转移
 电子时,消耗
电子时,消耗 的质量是
的质量是(3)当反应②中生成
 气体(标准状况下)时,被还原的
气体(标准状况下)时,被还原的 的物质的量
的物质的量(4)用单线桥法表示反应②电子转移的方向和数目(在化学方程式上标出)
您最近一年使用:0次
【推荐2】从化合价的角度认识氯的化合物。
(1)二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备ClO2的反应原理如下:2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①该反应中,氧化剂是___ ,氧化产物是___ ,氧化剂和还原剂的物质的量之比为__ ,依据氧化还原反应规律判断,氧化性强弱为NaClO3___ Cl2(填>、<或=)。
②ClO2在杀菌消毒过程中会产生副产物亚氯酸盐(ClO ),需将其转化为Cl-除去,下列试剂中,可将ClO
),需将其转化为Cl-除去,下列试剂中,可将ClO 转化为Cl-的是
转化为Cl-的是___ (填字母序号)。
a.FeSO4 b.O3 c.KMnO4 d.SO2
(2)亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。Mathieson方法制备亚氯酸钠的流程如图:

请将流程中发生的两个反应的离子方程式补充完整:
反应①: ClO
ClO +
+ SO2=
SO2= SO
SO +
+
___
反应②: ClO2+
ClO2+ H2O2+
H2O2+ =
= ClO
ClO +
+ O2↑+
O2↑+ H2O
H2O___
(1)二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备ClO2的反应原理如下:2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①该反应中,氧化剂是
②ClO2在杀菌消毒过程中会产生副产物亚氯酸盐(ClO
 ),需将其转化为Cl-除去,下列试剂中,可将ClO
),需将其转化为Cl-除去,下列试剂中,可将ClO 转化为Cl-的是
转化为Cl-的是a.FeSO4 b.O3 c.KMnO4 d.SO2
(2)亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。Mathieson方法制备亚氯酸钠的流程如图:

请将流程中发生的两个反应的离子方程式补充完整:
反应①:
 ClO
ClO +
+ SO2=
SO2= SO
SO +
+
反应②:
 ClO2+
ClO2+ H2O2+
H2O2+ =
= ClO
ClO +
+ O2↑+
O2↑+ H2O
H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】利用氯元素的价类二维图,可以更方便的研究含氯物质的性质及其转化关系,回答下列问题:__________ ,属于________ (“酸性”或“碱性”)氧化物;用电子式表示乙的形成过程________________________ 。
(2)图中甲、乙、丙、戊中,属于电解质的是__________________ (填电子式);根据氯元素的化合价判断乙物质具有__________________ 性;庚是漂白粉的有效成分,写出用乙制取庚的化学方程式:___________________________________________________________ ;
(3)电解甲溶液制备己的化学反应为: (未配平),则配平后参与反应的甲与
(未配平),则配平后参与反应的甲与 的物质的量之比是
的物质的量之比是________ ;己为酸性最强的无机酸,其电离方程式_____________________ 。
(4)辛的焰色实验中,透过蓝色钴玻璃,观察到紫色,写出辛的化学式为__________ ,该物质中含有的化学键为___________ 。

(2)图中甲、乙、丙、戊中,属于电解质的是
(3)电解甲溶液制备己的化学反应为:
 (未配平),则配平后参与反应的甲与
(未配平),则配平后参与反应的甲与 的物质的量之比是
的物质的量之比是(4)辛的焰色实验中,透过蓝色钴玻璃,观察到紫色,写出辛的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
(1)据汞的原子结构示意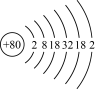 ,汞在第
,汞在第_____ 周期。
(2)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断不正确的是______ 。
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO2)具有还原性
c.硒的氧化物对应的水化物属于强酸
(3)氮是自然界各种生物体生命活动不可缺少的重要元素,磷(P)、砷(As)也是氮族元素。
①砷有多种同位素原子,其中稳定的核素是73As,它的中子数为______ 。
②已知NH4Cl与PH4I的性质相似,则对PH4I性质的推测不正确的是_____ (填序号)。
a.含有离子键和共价键
b.能与NaOH溶液反应
c.与NH4Cl加热充分分解产物的种类完全一样
③下列关于第VA族元素及其化合物的说法不正确的是_____ (填字母)。
a.热稳定性:NH3>PH3 b.酸性:HNO3>H3AsO4
c.As的氧化物的水化物是弱碱 d.形成的简单离子半径随着原子序数递增而增大
(1)据汞的原子结构示意
 ,汞在第
,汞在第(2)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断不正确的是
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO2)具有还原性
c.硒的氧化物对应的水化物属于强酸
(3)氮是自然界各种生物体生命活动不可缺少的重要元素,磷(P)、砷(As)也是氮族元素。
①砷有多种同位素原子,其中稳定的核素是73As,它的中子数为
②已知NH4Cl与PH4I的性质相似,则对PH4I性质的推测不正确的是
a.含有离子键和共价键
b.能与NaOH溶液反应
c.与NH4Cl加热充分分解产物的种类完全一样
③下列关于第VA族元素及其化合物的说法不正确的是
a.热稳定性:NH3>PH3 b.酸性:HNO3>H3AsO4
c.As的氧化物的水化物是弱碱 d.形成的简单离子半径随着原子序数递增而增大
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】可通过周期表预测元素的性质(由递变规律推测)。试回答下列问题。
(1)比较不同周期、不同主族元素的性质,如金属性Mg>Al、Ca>Mg,则碱性Mg(OH)2_______ Al(OH)3、Ca(OH)2_______ Mg(OH)2,则Ca(OH)2_______ Al(OH)3(填“>”“<”或“=”)。
(2)推测未知元素的某些性质,如:已知Ca(OH)2微溶,Mg(OH)2难溶,可推知Be(OH)2_______ 溶;再如:已知卤族元素的性质递变规律,可推知元素砹(At)应为有色固体,与氢_______ 化合,HAt_______ 稳定,水溶液呈_______ 性,AgAt_______ 溶于水等。
(1)比较不同周期、不同主族元素的性质,如金属性Mg>Al、Ca>Mg,则碱性Mg(OH)2
(2)推测未知元素的某些性质,如:已知Ca(OH)2微溶,Mg(OH)2难溶,可推知Be(OH)2
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)已知固态NH3、H2O、HF中的氢键的键能和结构示意图如表所示:

H2O、HF、NH3沸点依次降低的原因是____ 。
(2)已知:常温时H2A的Ka1=5×10-5,Ka2=3×10-9,请判断NaHA溶液的酸碱性并说明原因:____ 。
(1)已知固态NH3、H2O、HF中的氢键的键能和结构示意图如表所示:
| 物质及其氢键 | HF(s):F—H…F | H2O(s):O—H…O | NH3(s):N—H…N |
| 键能/(kJ·mol-1) | 28.1 | 18.8 | 5.4 |

H2O、HF、NH3沸点依次降低的原因是
(2)已知:常温时H2A的Ka1=5×10-5,Ka2=3×10-9,请判断NaHA溶液的酸碱性并说明原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】丙酸钠(CH3CH2COONa)和氨基乙酸钠均能水解,水解产物有丙酸(CH3CH2COOH)和氨基乙酸(H2NCH2COOH),常温下丙酸为液体,而氨基乙酸为固体,主要原因是_______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1) 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为_______ (填化学式,下同),还原性由强到弱的顺序为_______ ,键角由大到小的顺序为_______ 。
(2)常温下,在水中的溶解度乙醇大于氯乙烷,原因是_______ 。
(3)在常压下,甲醇的沸点(65℃)比甲醛的沸点(-19℃)高。主要原因是_______ 。
(4)苯胺(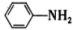 )与甲苯(
)与甲苯( )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是_______ 。
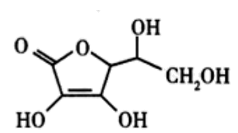
(5)抗坏血酸的分子结构如图所示,推测抗坏血酸在水中的溶解性:_______ (填“难溶于水”或“易溶于水”)。
 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为(2)常温下,在水中的溶解度乙醇大于氯乙烷,原因是
(3)在常压下,甲醇的沸点(65℃)比甲醛的沸点(-19℃)高。主要原因是
(4)苯胺(
 )与甲苯(
)与甲苯( )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是(5)抗坏血酸的分子结构如图所示,推测抗坏血酸在水中的溶解性:

您最近一年使用:0次
【推荐1】对于数以千万计的化学物质和十分丰富的化学变化,分类法的作用几乎是无可替代的。某化学兴趣小组对下列三组物质进行研究:
A组:CaO、 、
、 、CuO
、CuO
B组: 、
、 、
、 、Cu
、Cu
C组: 、HCl、
、HCl、 、
、
完成下表,并根据所给物质填空。
(1)上表中应该分别填入:①_______ ,②_______ ,③_______ 。
(2)写出实验室制备 的化学反应方程式
的化学反应方程式_______ 。
(3)工业上用 与石灰乳制取漂白粉,漂白粉的有效成分的化学式是
与石灰乳制取漂白粉,漂白粉的有效成分的化学式是_______ 。84消毒液与氯气相比具有贮运方便等优点,工业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产100kg该溶液需消耗氯气的质量为_______ kg(保留整数)。
(4)采用“空气吹出法”可从浓海水吹出 ,并用纯碱吸收。纯碱吸收溴的主要反应是:
,并用纯碱吸收。纯碱吸收溴的主要反应是: (未配平)。该反应的氧化产物是
(未配平)。该反应的氧化产物是_______ ,吸收 时,转移的电子数为
时,转移的电子数为_______ mol。
A组:CaO、
 、
、 、CuO
、CuOB组:
 、
、 、
、 、Cu
、CuC组:
 、HCl、
、HCl、 、
、
完成下表,并根据所给物质填空。
| 组别 | A组 | B组 | C组 |
| 分类标准 | 碱性氧化物 | ② | ③ |
| 不属于该类别的物质 | ① | Cu |  |
(1)上表中应该分别填入:①
(2)写出实验室制备
 的化学反应方程式
的化学反应方程式(3)工业上用
 与石灰乳制取漂白粉,漂白粉的有效成分的化学式是
与石灰乳制取漂白粉,漂白粉的有效成分的化学式是(4)采用“空气吹出法”可从浓海水吹出
 ,并用纯碱吸收。纯碱吸收溴的主要反应是:
,并用纯碱吸收。纯碱吸收溴的主要反应是: (未配平)。该反应的氧化产物是
(未配平)。该反应的氧化产物是 时,转移的电子数为
时,转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】海水中含有大量的卤族元素,具有十分巨大的开发利用潜力。
I.氯气是非常重要的化工产品
(1)用浓盐酸和二氧化锰制氯气是实验室常用的方法,写出该反应的化学方程式:_____ 。
(2)也可用浓盐酸和高锰酸钾制氯气,反应方程式如下:2KMnO4+16HCl(浓)=KCl+2MnCl2+5Cl2↑+8H2O,实验室用该方法制氯气时,可选用的发生装置是___________ (写编号)。
(3)为证明氯气与水反应产物具有漂白性,将Cl2缓缓通过下列装置:
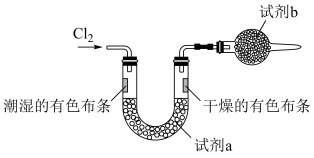
试剂a应选择___________ ;试剂b的作用是___________ ;___________ 。
(4)通常使用84消毒液时需要把消毒对象在其中浸泡一段时间,以提高消毒效果。请结合反应方程式分析原因___________
II.地球上99%的溴元素以Br-形式存在于海水中。海水中Br-含量约为65mg/L,而苦卤(海水晒盐后得到的母液)中Br-含量高很多,苦卤常作海水提溴的主要原料。目前最成熟的“空气吹出法”海水提溴工艺流程如图(已知:溴的沸点为59℃):
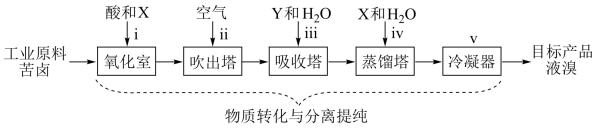
(5)为实现Br-转化为Br2的目的,所加试剂X应必有的化学性质是___________ 。
(6)利用“空气吹出法”将“氧化室”产生的低浓度Br2分离出来的方法利用了溴的___________ 这一物理性质。
(7)将低浓度Br2富集为高浓度Br2历经步骤iii反应的离子方程式为:___________ 。
I.氯气是非常重要的化工产品
(1)用浓盐酸和二氧化锰制氯气是实验室常用的方法,写出该反应的化学方程式:
(2)也可用浓盐酸和高锰酸钾制氯气,反应方程式如下:2KMnO4+16HCl(浓)=KCl+2MnCl2+5Cl2↑+8H2O,实验室用该方法制氯气时,可选用的发生装置是
| 编号 | A | B | C |
| 发生装置 | 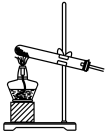 |  | 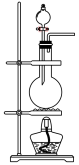 |

试剂a应选择
(4)通常使用84消毒液时需要把消毒对象在其中浸泡一段时间,以提高消毒效果。请结合反应方程式分析原因
II.地球上99%的溴元素以Br-形式存在于海水中。海水中Br-含量约为65mg/L,而苦卤(海水晒盐后得到的母液)中Br-含量高很多,苦卤常作海水提溴的主要原料。目前最成熟的“空气吹出法”海水提溴工艺流程如图(已知:溴的沸点为59℃):

(5)为实现Br-转化为Br2的目的,所加试剂X应必有的化学性质是
(6)利用“空气吹出法”将“氧化室”产生的低浓度Br2分离出来的方法利用了溴的
(7)将低浓度Br2富集为高浓度Br2历经步骤iii反应的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.金属元素的原子结构决定了金属元素的性质、在自然界中的存在形式及冶炼方法。
(1)金属在自然界中大多以化合物的形式存在,在这些金属化合物中,金属元素都显___________ (填“正”或“负”)化合价。
(2)金属的冶炼方法可以分为:A.焦炭法;B.热分解法;C.活泼金属置换法;D.电解法。
请从上述四种方法中选择相应的序号填入表中空格:
(3)写出Al与Cr2O3反应的化学方程式:___________ 。
Ⅱ.以下为工业从海水中提取液溴的流程图:
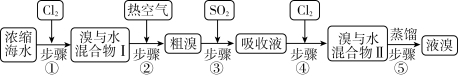
已知:溴的沸点为59℃,微溶于水,有毒性。请回答:
(4)用热空气能将溴单质吹出的原因是___________ 。
(5)从“溴与水混合物Ⅰ”到“溴与水混合物Ⅱ”的目的是___________ 。
(1)金属在自然界中大多以化合物的形式存在,在这些金属化合物中,金属元素都显
(2)金属的冶炼方法可以分为:A.焦炭法;B.热分解法;C.活泼金属置换法;D.电解法。
请从上述四种方法中选择相应的序号填入表中空格:
| 高炉炼铁 | 湿法炼铜 | 铝热法炼铬 | 工业上冶炼钾 |
| ① | ② | ③ | ④ |
Ⅱ.以下为工业从海水中提取液溴的流程图:

已知:溴的沸点为59℃,微溶于水,有毒性。请回答:
(4)用热空气能将溴单质吹出的原因是
(5)从“溴与水混合物Ⅰ”到“溴与水混合物Ⅱ”的目的是
您最近一年使用:0次



