某温度下,向c(H+)=1×10-6 mol·L-1的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液中c(H+)=1×10-3mol·L-1。下列对该溶液的叙述不正确的是( )
| A.该温度高于25℃ |
B. 的电离方程式为NaHSO4=Na++H++SO42- 的电离方程式为NaHSO4=Na++H++SO42- |
| C.加入NaHSO4晶体抑制了水的电离 |
| D.由水电离出来的H+的浓度为1×10-12mol·L-1 |
更新时间:2019-10-29 13:56:30
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】常温下,用0.1mol/L的HCl溶液滴定amLNaOH稀溶液,反应恰好完全时,消耗HCl溶液bmL,此时溶液中氢氧根离子的浓度c(OH-)是
| A.1×10-7mol/L | B.1×107mol/L | C.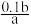 mol/L mol/L | D. mol/L mol/L |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列说法中正确的是
A.100℃时Kw为 ,则100℃下 ,则100℃下 的 的 溶液pH为13 溶液pH为13 |
B.常温下,将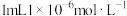 的稀盐酸稀释至1000mL,所得溶液的pH为9 的稀盐酸稀释至1000mL,所得溶液的pH为9 |
C.常温下当水电离的 为 为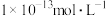 时,此溶液的pH可能为1或13 时,此溶液的pH可能为1或13 |
D.将 的盐酸与 的盐酸与 的醋酸各1mL分别稀释至100mL,稀释后醋酸溶液的pH更大 的醋酸各1mL分别稀释至100mL,稀释后醋酸溶液的pH更大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】向纯水中加入少量的KHSO4固体(温度不变),则溶液的
| A.pH值减小 |
| B.c(H+)和c(OH-)的乘积增大 |
| C.酸性减弱 |
| D.OH-离子浓度增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】25℃时,水的电离达到平衡:H2O H++OH- △H>0,下列叙述正确的是
H++OH- △H>0,下列叙述正确的是
 H++OH- △H>0,下列叙述正确的是
H++OH- △H>0,下列叙述正确的是| A.向水中加入少量固体硫酸氢钠,c (H+)增大,Kw不变 |
| B.向水中加入氨水,平衡逆向移动,c (OH-)降低 |
| C.向水中加入金属钠,平衡逆向移动,c (H+)减小 |
| D.将水加热,Kw增大,pH不变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】水的电离平衡曲线如下图所示,已知 ,下列说法正确的是
,下列说法正确的是
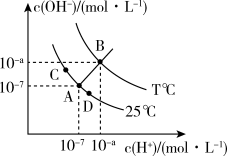
 ,下列说法正确的是
,下列说法正确的是 
A.保持温度不变,向A点溶液中通入适量 ,可获得D点溶液 ,可获得D点溶液 |
| B.B点溶液呈酸性 |
| C.C点溶液和D点溶液混合,所得溶液呈中性 |
D. |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】25℃时,下列溶液中水的电离程度最小的是
| A.pH=11 的氨水 | B.0.01 mol/L的 Na2CO3溶液 |
| C.pH=2的NaHSO4溶液 | D.0.1 mol/L的盐酸 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下图为常温下向10mL0.1 mol·L-1 NH3·H2O中加入等浓度的盐酸时,NH3·H2O的物质的量随V(盐酸)的变化曲线。(电离度为已电离的NH3•H2O占初始时NH3•H2O的百分比),下列说法正确的是( )
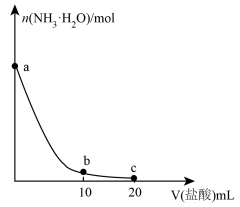

| A.测得a点时溶液的pH=11,则NH3·H2O的电离度为1% |
| B.b点时溶液的pH=7 |
| C.水的电离程度:b<c |
| D.c点时溶液中存在关系式:2c(Cl-)=c(NH4+) +c(NH3•H2O) |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】25℃时,pH=2的NH4Cl溶液中,由水电离出的H+浓度是
| A.1×10-2mol·L-1 | B.1×10-7mol·L-1 |
| C.1×10-12mol·L-1 | D.1×10-14mol·L-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】能影响水的电离平衡,并使溶液中的 c(H+)<c(OH-)的操作是
| A.向水中加入硫酸钾晶体 |
| B.将水加热煮沸 |
| C.向水中通入二氧化硫气体 |
| D.向水中加入小苏打晶体 |
您最近一年使用:0次

 、Cl-
、Cl- 、Br-、Cl-
、Br-、Cl-
 、Cl-、SO
、Cl-、SO

