铅蓄电池是化学电源,其电极材料分别是Pb和PbO2,电解液为稀硫酸。工作时该电池总反应式为:Pb(s)+PbO2(s)+2H2SO4(aq)  2PbSO4(s)+2H2O(l)。根据上述情况判断:
2PbSO4(s)+2H2O(l)。根据上述情况判断:
(1)放电时,电解质溶液的pH________ (填“增大”“减小”或“不变”)。
(2)放电时,电解质溶液中阴离子移向_____ 极,电子从_____ 极流向____ 极。
(3)写出负极的电极方程式:_____________________________________ 。
 2PbSO4(s)+2H2O(l)。根据上述情况判断:
2PbSO4(s)+2H2O(l)。根据上述情况判断:(1)放电时,电解质溶液的pH
(2)放电时,电解质溶液中阴离子移向
(3)写出负极的电极方程式:
更新时间:2019-11-03 17:23:38
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】为了探究原电池和电解池的工作原理,某研究性学习小组分别用如图甲、乙所示的装置进行实验,回答下列问题。
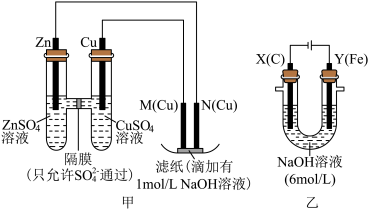
Ⅰ.用甲装置进行第一组实验:
(1)甲中电子的流向正确的是_____ (填序号)。
A.由Cu流向M,M流向N,N流向Zn
B.由Cu沿导线流向M,由N沿导线流向Zn
C.由Zn沿导线流向N,由M沿导线流向Cu
(2)在保证电极反应不变的情况下,下列材料能代替硫酸铜溶液中Cu电极的是_____(填序号)。
(3)实验过程中,甲池左侧的 浓度
浓度_____ (填“增大”或“减小”),滤纸上能观察到的现象是_____ 。
Ⅱ.该小组同学用乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子( )在溶液中呈紫红色。请根据实验现象及资料信息,填写下列空白:
)在溶液中呈紫红色。请根据实验现象及资料信息,填写下列空白:
(4)可用碱性甲烷燃料电池作为乙池的外加电源,写出该燃料电池负极的电极反应式_____ 。
(5)电解过程中,X极附近溶液的碱性_____ (填“增强”“减弱”或“不变”)。
(6)电解过程中,Y极发生的电极反应为 和
和_____ 。

Ⅰ.用甲装置进行第一组实验:
(1)甲中电子的流向正确的是
A.由Cu流向M,M流向N,N流向Zn
B.由Cu沿导线流向M,由N沿导线流向Zn
C.由Zn沿导线流向N,由M沿导线流向Cu
(2)在保证电极反应不变的情况下,下列材料能代替硫酸铜溶液中Cu电极的是_____(填序号)。
| A.石墨 | B.铂 | C.铝 | D.镁 |
 浓度
浓度Ⅱ.该小组同学用乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子(
 )在溶液中呈紫红色。请根据实验现象及资料信息,填写下列空白:
)在溶液中呈紫红色。请根据实验现象及资料信息,填写下列空白:(4)可用碱性甲烷燃料电池作为乙池的外加电源,写出该燃料电池负极的电极反应式
(5)电解过程中,X极附近溶液的碱性
(6)电解过程中,Y极发生的电极反应为
 和
和
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池,测得原电池的电流(I)随时间(t)的变化如图乙所示,反应过程中有红棕色气体产生。
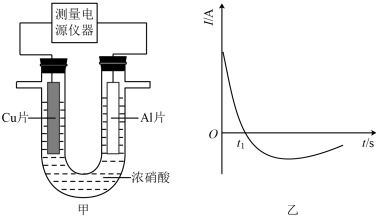
(1)①0~t1时,原电池的负极是____ 片,发生氧化反应后其氧化产物的化学式是____ ,正极的电极反应式是____ ,溶液中的H+向____ (填“Al”或“Cu”)移动。
②t1时原电池中电子流动方向发生改变,其原因是____ 。
(2)有关的电池装置如图:
①上述四种电池中,属于二次电池的是____ (填序号,下同),其负极的电极反应式为____ 。
②a装置中,外电路中电子的流向是____ (填“从Zn流向Cu”或“从Cu流向Zn”)。
③c装置中,若电解质改为碱性介质,则负极的电极反应式为____ 。

(1)①0~t1时,原电池的负极是
②t1时原电池中电子流动方向发生改变,其原因是
(2)有关的电池装置如图:
| 电池装置 | 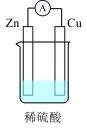 | 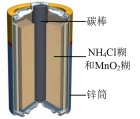 |  | 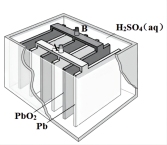 |
| 编号 | a | b | c | d |
②a装置中,外电路中电子的流向是
③c装置中,若电解质改为碱性介质,则负极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】合理开发利用能源具有重要意义。回答下列问题:
(1)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质。
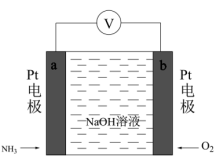
①电极b的名称是___________ ,电子的流动方向为___________ 。
②a极的电极反应式为___________ 。
③电池工作时,理论上反应消耗NH3与O2的物质的量之比为___________ 。
(2)通过如下流程可实现SO2和NO综合处理并获得保险粉( )和硝铵。
)和硝铵。

①装置Ⅲ中生成 与
与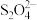 的物质的量之比为
的物质的量之比为___________ 。
②装置Ⅳ中溶液含有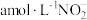 和
和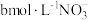 ,欲将cL该溶液完全转化为硝铵,需要通入
,欲将cL该溶液完全转化为硝铵,需要通入 与
与 的体积比为
的体积比为___________ (同温同压下)。
(1)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质。

①电极b的名称是
②a极的电极反应式为
③电池工作时,理论上反应消耗NH3与O2的物质的量之比为
(2)通过如下流程可实现SO2和NO综合处理并获得保险粉(
 )和硝铵。
)和硝铵。
①装置Ⅲ中生成
 与
与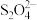 的物质的量之比为
的物质的量之比为②装置Ⅳ中溶液含有
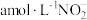 和
和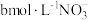 ,欲将cL该溶液完全转化为硝铵,需要通入
,欲将cL该溶液完全转化为硝铵,需要通入 与
与 的体积比为
的体积比为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】Ⅰ.一定温度下在某定容容器中发生反应:2A(g)+3B(g)=2C(g),开始时,A的浓度为2mol·L-1,B的浓度为4mol·L-1,2min后,A的浓度减少0.8mol·L-1,则:
(1)v(B)=_______ ,v(C)=_______ 。
(2)在2min末,C的浓度是_______ ,B的浓度是_______ 。
Ⅱ.如图所示的原电池装置中:

(1)_______ (填“铜”或“锌”)作负极。
(2)正极的电极反应式为_______ 。
(3)电子的流向_______ 。
(4)若铜电极上产生了标准状况下11.2L气体,则Zn电极会减轻_______ g。
(1)v(B)=
(2)在2min末,C的浓度是
Ⅱ.如图所示的原电池装置中:

(1)
(2)正极的电极反应式为
(3)电子的流向
(4)若铜电极上产生了标准状况下11.2L气体,则Zn电极会减轻
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】原电池是将化学能转化为电能的装置,某兴趣小组利用数据采集器和传感器等仪器对原电池进行实验探究。
I.能量变化探究
将上表的现象和结论补充完整
(1)_____________
(2)__________ 、__________
II.原电池电压影响因素的测定
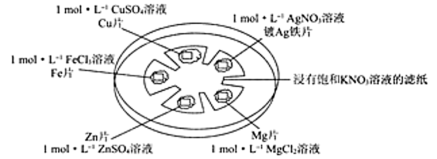
如图所示,在培养皿中进行微型实验,用浸有饱和KNO3溶液的滤纸充当盐桥,在滤纸间隔位置放置金属片,并滴三滴相应溶液,用电压传感器的两个探头分别与不同的金属表面接触形成闭合回路,测定电压。
(3)准确配制一定物质的量浓度的溶液时,操作X应在__________ (填字母)之间。
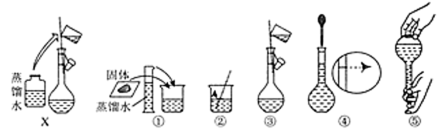
A.②③ B.③④ C.④⑤
(4)以上五种金属的活动性由活泼到不活泼的顺序为_________________ 。
(5)实验条件下,连接不同金属片时所得数据见下表,表中Y极代表__________ (填“正”或“负”)极,预测表中Ag和Zn相连接时,测得电压的数值a可能的范围为____________ ;Fe和Mg相连接时,Z极的电极反应式为__________ ,Y极的电极反应式为____________ 。
I.能量变化探究
| 实验操作 | 数据及图象 | 现象与结论 |
| 将60mL1mol/LCuSO4溶液置于100mL烧杯中,向其中加入1g镁粉 | 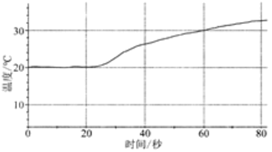 | (1)反应过程中,化学能直接转化为 能; |
| 将60mL1mol/LCuSO4溶液置于100mL烧杯中,平行插入铜片和镁片,与电流传感器形成闭合回路 | 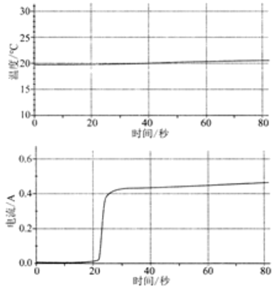 | (2)体系温度变化很小,原因是 ;反应过程中,镁片和铜片的质量变化分别为: ; |
(1)
(2)
II.原电池电压影响因素的测定
如图所示,在培养皿中进行微型实验,用浸有饱和KNO3溶液的滤纸充当盐桥,在滤纸间隔位置放置金属片,并滴三滴相应溶液,用电压传感器的两个探头分别与不同的金属表面接触形成闭合回路,测定电压。

(3)准确配制一定物质的量浓度的溶液时,操作X应在

A.②③ B.③④ C.④⑤
(4)以上五种金属的活动性由活泼到不活泼的顺序为
(5)实验条件下,连接不同金属片时所得数据见下表,表中Y极代表
| Y极 | Z极 | 测得电压/V |
| Ag | Fe | 1.009 |
| Ag | Zn | a |
| Ag | Mg | 2.114 |
| Fe | Zn | 0.473 |
| Fe | Mg | 1.111 |
| Zn | Mg | 0.636 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】氮及其化合物与人们的生产、生活密切相关。回答下列问题:
(1)氮与氧能形成多种氧化物,消除氮氧化物有多种方法,NH3催化、还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示。
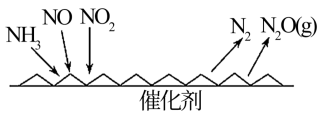
①由图可知,SCR技术中的还原剂为_______ (填化学式)。
②设参加反应的NO和NO2的物质的量相等,写出图中发生反应的化学方程式:_______ 。
(2)25℃时,水能吸收部分NO、NO2的混合气体得到HNO2溶液,向20mL 0.1mol·L-1 HNO2溶液中逐滴加入0.1mo·L-1的NaOH溶液所得pH变化曲线如图所示;已知:10-2.1=0.008
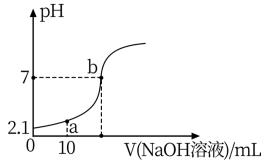
① =
=_______ (保留2位有效数字,下同)。
②a点溶液中各离子浓度由大到小的顺序为_______ 。
③b点对应的溶液中 =
=_______ 。
(3)利用如图所示装置,可将汽车尾气中的NO、NO2[设n(NO)= n(NO2)]转化为化工原料HNO3,同时可获得电能。
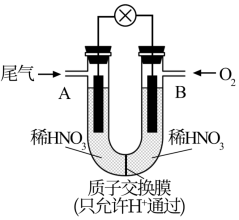
①该装置的正极是_______ (填“A”或“B”)极。
②A电极的电极反应式为_______ 。
(1)氮与氧能形成多种氧化物,消除氮氧化物有多种方法,NH3催化、还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示。

①由图可知,SCR技术中的还原剂为
②设参加反应的NO和NO2的物质的量相等,写出图中发生反应的化学方程式:
(2)25℃时,水能吸收部分NO、NO2的混合气体得到HNO2溶液,向20mL 0.1mol·L-1 HNO2溶液中逐滴加入0.1mo·L-1的NaOH溶液所得pH变化曲线如图所示;已知:10-2.1=0.008

①
 =
=②a点溶液中各离子浓度由大到小的顺序为
③b点对应的溶液中
 =
=(3)利用如图所示装置,可将汽车尾气中的NO、NO2[设n(NO)= n(NO2)]转化为化工原料HNO3,同时可获得电能。

①该装置的正极是
②A电极的电极反应式为
您最近一年使用:0次
【推荐1】三氧化二镍(Ni2O3)是重要的电子元件和蓄电池材料,工业上利用含镍废料(主要含金属Ni、A1、Fe及其氧化物、SiO2、C等)回收其中的镍并制备Ni2O3的工艺流程如下所示:

已知:①在该实验条件下NaClO3、Fe3+不能氧化Ni2+。
②溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
③反萃取的反应原理为NiR2+2H+ Ni2++2HR
Ni2++2HR
(1)“预处理”的操作可以选择用_______ (填标号)来除去镍废料表面的矿物油污。
A.纯碱溶液浸泡 B.NaOH溶液浸泡 C.酒精清洗
(2)“氧化”时主要反应的离子方程式是_______ ,实际生产中为了减少杂质离子的引入,可以用来替代NaClO3的试剂是_______ (填化学式)。
(3)利用上述表格数据,计算Al(OH)3的Ksp=_______ (列出计算式),若“氧化”后的溶液中Ni2+浓度为0.1mol·L-1,则“调pH”应控制的pH范围是_______ 。
(4)向有机相中加入H2SO4溶液能进行反萃取的原因为_______ (结合平衡移动原理解释)。
(5)资料显示,硫酸镍结晶水合物的形态与温度有如下关系:
从NiSO4溶液获得稳定的NiSO4·6H2O晶体的操作依次是_______ 。
(6)有机相提取的Ni2+再生时可用于制备镍氢电池,该电池充电时的总反应为Ni(OH)2+M=NiOOH+MH,则放电时负极的电极反应式为_______ 。

已知:①在该实验条件下NaClO3、Fe3+不能氧化Ni2+。
②溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Ni2+ | A13+ | Fe3+ | Fe2+ |
| 开始沉淀时(c=0.010 mol·L-1)的pH | 7.2 | 3.7 | 2.2 | 7.5 |
| 完全沉淀时(c=1.0×10-5 mol·L-1)的pH | 8.7 | 4.7 | 3.2 | 9.0 |
 Ni2++2HR
Ni2++2HR(1)“预处理”的操作可以选择用
A.纯碱溶液浸泡 B.NaOH溶液浸泡 C.酒精清洗
(2)“氧化”时主要反应的离子方程式是
(3)利用上述表格数据,计算Al(OH)3的Ksp=
(4)向有机相中加入H2SO4溶液能进行反萃取的原因为
(5)资料显示,硫酸镍结晶水合物的形态与温度有如下关系:
| 温度 | 低于30.8℃ | 30.8℃~53.8℃ | 53.8℃~280℃ | 高于280℃ |
| 晶体形态 | NiSO4·7H2O | NiSO4·6H2O | 多种结晶水合物 | NiSO4 |
(6)有机相提取的Ni2+再生时可用于制备镍氢电池,该电池充电时的总反应为Ni(OH)2+M=NiOOH+MH,则放电时负极的电极反应式为
您最近一年使用:0次
【推荐2】I.含氮化合物在工农业生产中都有重要应用。
(1)已知:
 ,化学平衡常数为K1;
,化学平衡常数为K1;
 ,化学平衡常数为K2。则用NH3和O2制取N2H4的热化学方程式为
,化学平衡常数为K2。则用NH3和O2制取N2H4的热化学方程式为_______ 。该反应的化学平衡常数K=_______ (用K1、K2表示)。
(2)对于 在一定温度下,在1 L的恒容密闭容器中充入0.1 mol NO和0.3 mol CO,反应开始进行。下图为容器内的压强(P)与起始压强(P0)的比值(
在一定温度下,在1 L的恒容密闭容器中充入0.1 mol NO和0.3 mol CO,反应开始进行。下图为容器内的压强(P)与起始压强(P0)的比值(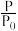 )随时间(t)的变化曲线,0~5 min内,该反应的平均反应速率v(N2)=
)随时间(t)的变化曲线,0~5 min内,该反应的平均反应速率v(N2)=_______ ,平衡时NO的转化率为_______ 。

II.2NH3(g)+CO2(g) NH2COONH4(s)
NH2COONH4(s)
(3)恒温恒容下通入2 mol NH3和1 mol CO2进行上述反应,下列事实能证明反应已达平衡的是_______。
(4)[用零价铁(Fe)去除水体中的硝酸盐(NO )已成为环境修复研究的热点之一、Fe还原水体中NO
)已成为环境修复研究的热点之一、Fe还原水体中NO 的反应原理如图所示。
的反应原理如图所示。

①作负极的物质是_______ 。
②正极的电极反应式是_______ 。
(1)已知:

 ,化学平衡常数为K1;
,化学平衡常数为K1;
 ,化学平衡常数为K2。则用NH3和O2制取N2H4的热化学方程式为
,化学平衡常数为K2。则用NH3和O2制取N2H4的热化学方程式为(2)对于
 在一定温度下,在1 L的恒容密闭容器中充入0.1 mol NO和0.3 mol CO,反应开始进行。下图为容器内的压强(P)与起始压强(P0)的比值(
在一定温度下,在1 L的恒容密闭容器中充入0.1 mol NO和0.3 mol CO,反应开始进行。下图为容器内的压强(P)与起始压强(P0)的比值(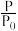 )随时间(t)的变化曲线,0~5 min内,该反应的平均反应速率v(N2)=
)随时间(t)的变化曲线,0~5 min内,该反应的平均反应速率v(N2)=
II.2NH3(g)+CO2(g)
 NH2COONH4(s)
NH2COONH4(s)(3)恒温恒容下通入2 mol NH3和1 mol CO2进行上述反应,下列事实能证明反应已达平衡的是_______。
| A.体系压强保持不变 | B.气体平均密度保持不变 |
| C.气体的平均摩尔质量保持不变 | D.氨气的体积分数不变 |
(4)[用零价铁(Fe)去除水体中的硝酸盐(NO
 )已成为环境修复研究的热点之一、Fe还原水体中NO
)已成为环境修复研究的热点之一、Fe还原水体中NO 的反应原理如图所示。
的反应原理如图所示。
①作负极的物质是
②正极的电极反应式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】分析如图所示装置,完成下列各题。
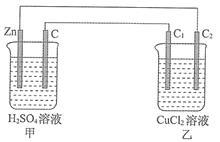
(1)一段时间后,可能发现的现象是:甲池,Zn棒逐渐溶解,石墨棒上有____________ 产生。与Zn棒相连的石墨棒质量____________ (填“增大”“减小”或“不变”)。
(2)甲池Zn极为____________ 极,电极反应式:____________________________________ 。
乙池中C1为____________ 极,电极反应式:____________________________________ 。乙池总反应式:____________________________________ 。

(1)一段时间后,可能发现的现象是:甲池,Zn棒逐渐溶解,石墨棒上有
(2)甲池Zn极为
乙池中C1为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
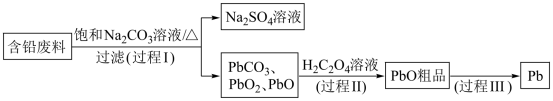
【推荐1】从含铅废料(PbSO4、PbO2、PbO等)中回收铅,实现铅的再生意义重大。一种回收铅的工作流程如下:
(1)铅和碳元素同主族,比碳多4个电子层,则铅元素的原子序数为______ ;铅蓄电池放电对,PbO2作______ 极。
(2)过程Ⅰ,已知:PbSO4、PbCO3的溶解度(20℃)见图1;相关物质溶解度见图2。

①根据图1写出过程Ⅰ的离子方程式:__________________ 。
②生产过程中的温度应保持在40℃,若温度降低,PbSO4的转化速率下降。根据图2,解释原因:
i.温度降低,反应速率降低;
ii.___________________ (请你提出一种合理解释)
(3)过程Ⅱ:发生反应2PbO2+H2C2O4=2PbO+H2O2+2CO2↑
请写出草酸的电子式________ 。PbO与Al2O3性质相似,PbO与氢氧化钠溶液反应的离子方程式是______________________ 。
(4)过程Ⅲ:将PbO粗品溶解在H2SO4和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液生成Pb,如图。

①阴极的电极反应式是_____________________ 。
②电解一段时间后,Na2PbCl4浓度极大下降,为了能使电解过程持续进行,阴极区采取的方法是____________ 。

(1)铅和碳元素同主族,比碳多4个电子层,则铅元素的原子序数为
(2)过程Ⅰ,已知:PbSO4、PbCO3的溶解度(20℃)见图1;相关物质溶解度见图2。

①根据图1写出过程Ⅰ的离子方程式:
②生产过程中的温度应保持在40℃,若温度降低,PbSO4的转化速率下降。根据图2,解释原因:
i.温度降低,反应速率降低;
ii.
(3)过程Ⅱ:发生反应2PbO2+H2C2O4=2PbO+H2O2+2CO2↑
请写出草酸的电子式
(4)过程Ⅲ:将PbO粗品溶解在H2SO4和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液生成Pb,如图。

①阴极的电极反应式是
②电解一段时间后,Na2PbCl4浓度极大下降,为了能使电解过程持续进行,阴极区采取的方法是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】目前工业上有一种方法是用CO2生产燃料甲醇(CH3OH)。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),图1表示该反应过程中能量(单位为kJ·mol—1)的变化。
CH3OH(g)+H2O(g),图1表示该反应过程中能量(单位为kJ·mol—1)的变化。
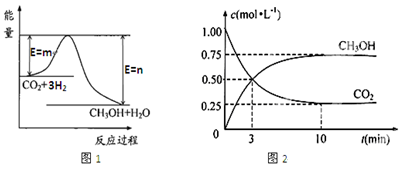
(1)该反应为_________ 热反应,原因是_____________________ 。
(2)下列能说明该反应已经达到平衡状态的是_________ (填序号)
A.v (H2)=3v(CO2) B.容器内气体压强保持不变
C.v逆(CO2)=v正(CH3OH) D.容器内气体密度保持不变
E.CH3OH 中1 mol H—O键断裂的同时2 mol C=O键断裂
F. 混合气体的平均摩尔质量不变
(3)在体积为1 L的密闭容器中,充入1 molCO2和3 molH2,测得CO2和CH3OH(g)的浓度随时间变化如图2所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v (H2)=________ 。 达平衡时容器内平衡时与起始时的压强比____________ 。
(4)甲醇、氧气在酸性条件下可构成燃料电池,其负极的电极反应为________________ ,
与铅蓄电池相比,当消耗相同质量的负极物质时,甲醇燃料电池的理论放电量是铅蓄电池的___________ 倍(保留小数点后1位)。
 CH3OH(g)+H2O(g),图1表示该反应过程中能量(单位为kJ·mol—1)的变化。
CH3OH(g)+H2O(g),图1表示该反应过程中能量(单位为kJ·mol—1)的变化。
(1)该反应为
(2)下列能说明该反应已经达到平衡状态的是
A.v (H2)=3v(CO2) B.容器内气体压强保持不变
C.v逆(CO2)=v正(CH3OH) D.容器内气体密度保持不变
E.CH3OH 中1 mol H—O键断裂的同时2 mol C=O键断裂
F. 混合气体的平均摩尔质量不变
(3)在体积为1 L的密闭容器中,充入1 molCO2和3 molH2,测得CO2和CH3OH(g)的浓度随时间变化如图2所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v (H2)=
(4)甲醇、氧气在酸性条件下可构成燃料电池,其负极的电极反应为
与铅蓄电池相比,当消耗相同质量的负极物质时,甲醇燃料电池的理论放电量是铅蓄电池的
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】铅及其化合物有着优异的性能和广泛的应用。工业上利用铅浮渣(主要成分是PbO、Pb,还含有少量的Ag、CaO)制备硫酸铅。制备流程图如下
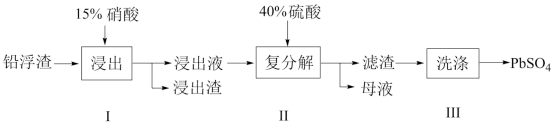
已知:Ksp(PbSO4)=1.6×10-8 Ksp(CaSO4)=4.9×10-5
(1)步骤I有NO产生浸出液中含量最多的金属阳离子为Pb2+,写出Pb参加反应的化学方程式___________________________ ,为防止Ag被溶解进入溶液,步骤I操作时应注意_______________________ 。
(2)粗PbSO4产品含有的杂质是____________ ;要得到纯净的PbSO4,需要用试剂进行多次洗涤,再用蒸馏水洗涤。最好选用的试剂是_________________ 。
A.稀硫酸 B.稀盐酸 C.硝酸铅溶液 D.酒精
(3)母液可循环利用的物质是HNO3,若母液中残留的 过多,循环利用时可能出现的问题是
过多,循环利用时可能出现的问题是______________________________ 。
(4)若将步骤Ⅱ中的Pb2+完全沉淀,则溶液中的c( )至少为
)至少为___________ mol/L。
(5)(CH3COO)2Pb是皮毛行业可溶于水的染色助剂,可用PbSO4与CH3COONH4反应制备,写出该反应的离子方程式_______________________ 。
(6)铅蓄电池是电压稳定、使用方便的二次电池。PbSO4在其中扮演了重要角色,写出铅蓄电池充电时阳极的电极反应_______________________ 。

已知:Ksp(PbSO4)=1.6×10-8 Ksp(CaSO4)=4.9×10-5
(1)步骤I有NO产生浸出液中含量最多的金属阳离子为Pb2+,写出Pb参加反应的化学方程式
(2)粗PbSO4产品含有的杂质是
A.稀硫酸 B.稀盐酸 C.硝酸铅溶液 D.酒精
(3)母液可循环利用的物质是HNO3,若母液中残留的
 过多,循环利用时可能出现的问题是
过多,循环利用时可能出现的问题是(4)若将步骤Ⅱ中的Pb2+完全沉淀,则溶液中的c(
 )至少为
)至少为(5)(CH3COO)2Pb是皮毛行业可溶于水的染色助剂,可用PbSO4与CH3COONH4反应制备,写出该反应的离子方程式
(6)铅蓄电池是电压稳定、使用方便的二次电池。PbSO4在其中扮演了重要角色,写出铅蓄电池充电时阳极的电极反应
您最近一年使用:0次



