(1)配平该反应化学方程式且回答下列问题:__ KMnO4+__ HCl=__ MnCl2+___ KCl+__ Cl2↑+__ H2O
(2)氧化剂是__ ,氧化产物是____ (填化学式)。
(3)若生成71gCl2,被氧化的HCl是__ mol。
(2)氧化剂是
(3)若生成71gCl2,被氧化的HCl是
更新时间:2019-11-04 19:05:08
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。
(1)在该反应中,还原剂是___ (填化学式)。KNO3发生了___ 反应(填“氧化”或“还原”)。
(2)烟花爆竹的成分中含有黑火药,点燃后,瞬间产生大量气体,同时释放大量热,在有限的空间里,气体受热迅速膨胀引起爆炸。反应中每消耗0.1molS,释放的气体体积为___ L(换算成标准状况)。
(3)除了黑火药,烟花爆竹中常加入一些金属元素,燃烧时会产生五彩缤纷的火焰。如表为一些金属元素的焰色:
若燃放烟花的火焰呈现紫色,则烟花中可能含有元素____ (填元素符号),该元素在周期表中的位置为___ 。
(1)在该反应中,还原剂是
(2)烟花爆竹的成分中含有黑火药,点燃后,瞬间产生大量气体,同时释放大量热,在有限的空间里,气体受热迅速膨胀引起爆炸。反应中每消耗0.1molS,释放的气体体积为
(3)除了黑火药,烟花爆竹中常加入一些金属元素,燃烧时会产生五彩缤纷的火焰。如表为一些金属元素的焰色:
| 金属元素 | 钠 | 钾 | 钙 | 锶 | 钡 | 铜 |
| 火焰颜色 | 黄 | 紫 | 砖红 | 洋红 | 黄绿 | 绿 |
若燃放烟花的火焰呈现紫色,则烟花中可能含有元素
您最近一年使用:0次
【推荐2】回答下列问题:
(1)已知Cl2能将 氧化成Br2,现将少量Cl2通入FeBr2的溶液中,反应的离子方程式为
氧化成Br2,现将少量Cl2通入FeBr2的溶液中,反应的离子方程式为
 ,这个事实说明具有还原性的离子还原性强弱为
,这个事实说明具有还原性的离子还原性强弱为________ 。
(2)人体血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能。亚硝酸钠(NaNO2)可将人体血红蛋白中的Fe2+转化为Fe3+,生成高铁血红蛋白而丧失与氧气的结合能力。若误食亚硝酸钠中毒,可服维生素C缓解,说明维生素C具有________ 性。
(3)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、 、
、 、
、 、
、 、H2O
、H2O
①写出并配平湿法制高铁酸钾的离子反应方程式:________ 。
②每生成 转移
转移_______ mol电子,若反应过程中转移了0.3mol电子,则还原产物的物质的量为______ mol。
(1)已知Cl2能将
 氧化成Br2,现将少量Cl2通入FeBr2的溶液中,反应的离子方程式为
氧化成Br2,现将少量Cl2通入FeBr2的溶液中,反应的离子方程式为
 ,这个事实说明具有还原性的离子还原性强弱为
,这个事实说明具有还原性的离子还原性强弱为(2)人体血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能。亚硝酸钠(NaNO2)可将人体血红蛋白中的Fe2+转化为Fe3+,生成高铁血红蛋白而丧失与氧气的结合能力。若误食亚硝酸钠中毒,可服维生素C缓解,说明维生素C具有
(3)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、
 、
、 、
、 、
、 、H2O
、H2O①写出并配平湿法制高铁酸钾的离子反应方程式:
②每生成
 转移
转移
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】从价类二维的角度认识化学物质是一种高效的学习方法,铜元素的价类二维图如图,根据要求回答有关问题:
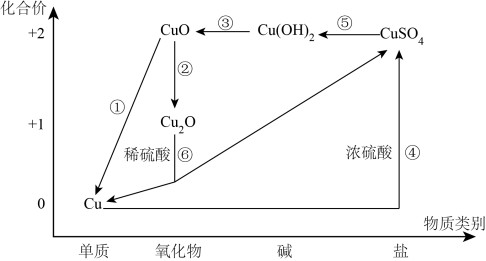
(1) 是铜绿的主要成分,其属于
是铜绿的主要成分,其属于 ______ (填序号)。
a.碱 b.正盐 c.碱式盐 d.酸式盐 e.碳酸盐
(2)转化②中铜元素的化合价_______ (填“升高”或“降低”)。
(3)转化④_____ (填“是”或“不是”)氧化还原反应。
(4)转化⑤的反应类型为_______ (填基本反应类型), 为
为 _______ (填“是”或“非”)电解质。
(5)已知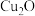 为砖红色不溶于水的固体,转化⑥可生成
为砖红色不溶于水的固体,转化⑥可生成 、
、 溶液和另一种物质,则转化⑥的方程式为
溶液和另一种物质,则转化⑥的方程式为 _______ 。
(6)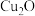 与稀
与稀 可以发生氧化还原反应,完成并配平下列方程式:
可以发生氧化还原反应,完成并配平下列方程式:_____
_______ 6
6 2
2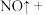 _______
_______

(1)
 是铜绿的主要成分,其属于
是铜绿的主要成分,其属于 a.碱 b.正盐 c.碱式盐 d.酸式盐 e.碳酸盐
(2)转化②中铜元素的化合价
(3)转化④
(4)转化⑤的反应类型为
 为
为 (5)已知
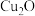 为砖红色不溶于水的固体,转化⑥可生成
为砖红色不溶于水的固体,转化⑥可生成 、
、 溶液和另一种物质,则转化⑥的方程式为
溶液和另一种物质,则转化⑥的方程式为 (6)
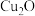 与稀
与稀 可以发生氧化还原反应,完成并配平下列方程式:
可以发生氧化还原反应,完成并配平下列方程式:_______
 6
6 2
2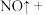 _______
_______
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
① (浓)
(浓)
②
③
④
⑤
⑥
⑦
⑧
(1)以上属于氧化还原反应反应的是___________ 。
(2)实验室制备氧气可以用加热高锰酸钾的方法实现,其发生的反应为 ,其中被氧化的元素是
,其中被氧化的元素是___________ (填元素符号),还原产物是___________ (填化学式,下同),氧化产物是___________ 。
(3)用双线桥表示反应中 中电子转移情况
中电子转移情况___________ 。
①
 (浓)
(浓)
②

③

④

⑤

⑥

⑦

⑧

(1)以上属于氧化还原反应反应的是
(2)实验室制备氧气可以用加热高锰酸钾的方法实现,其发生的反应为
 ,其中被氧化的元素是
,其中被氧化的元素是(3)用双线桥表示反应中
 中电子转移情况
中电子转移情况
您最近一年使用:0次
【推荐3】分析以下A~D四个涉及H2O2的反应(未配平),填空:
A.Na2O2+HCl→H2O2+NaCl
B.Ag2O+H2O→Ag+O2↑+H2O
C.H2O2→H2O+O2↑
D.H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
(1)H2O2仅体现氧化性的反应是__ ,H2O2仅体现还原性的反应是___ ,H2O2既体现氧化性,又体现还原性的反应是___ ,H2O2既不作氧化剂又不作还原剂的反应是___ (填序号)。
(2)用单线桥法表示D反应中电子转移的方向和数目:___ 。
3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
该反应中氧化剂是___ ,氧化产物是___ 。
(3)配平下列反应的化学方程式
①P+CuSO4+H2O=Cu+H3PO4+H2SO4:___ 。
②FeSO4+H2O+O2=Fe2(SO4)3+Fe(OH)3↓:___ 。
③C6H12O6+NaClO3+H2SO4=ClO2↑+CO2↑+H2O+Na2SO4:___ 。
A.Na2O2+HCl→H2O2+NaCl
B.Ag2O+H2O→Ag+O2↑+H2O
C.H2O2→H2O+O2↑
D.H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
(1)H2O2仅体现氧化性的反应是
(2)用单线桥法表示D反应中电子转移的方向和数目:
3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
该反应中氧化剂是
(3)配平下列反应的化学方程式
①P+CuSO4+H2O=Cu+H3PO4+H2SO4:
②FeSO4+H2O+O2=Fe2(SO4)3+Fe(OH)3↓:
③C6H12O6+NaClO3+H2SO4=ClO2↑+CO2↑+H2O+Na2SO4:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)化学与生活、生产息息相关。
① 可用于制备纯碱; ②
可用于制备纯碱; ② 可用于葡萄酒保存;
可用于葡萄酒保存;
③ 可用于制供氧剂; ④
可用于制供氧剂; ④ 可用于制耐火材料;
可用于制耐火材料;
⑤CO可用于冶炼金属; ⑥ 可用于制硫酸;
可用于制硫酸;
⑦ 可用于制硝酸
可用于制硝酸
上述物质中,属于酸性氧化物的是______________________ (填序号)。
(2)硝酸是用途广泛的重要化工原科。氨的催化氧化是工业合成硝酸的重要步骤,其中氧化剂与还原剂物质的量之比为___________ 。
(3)央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。明胶是水溶性蛋白质混合物,溶于水形成胶体。明胶的水溶液与NaCl溶液的共同点是___________ (填序号)。
A.都可以产生丁达尔效应 B.都属于混合物 C.都能透过滤纸
(4)氮、磷都是生命元素,它们的氢化物结构相似。 的沸点
的沸点___________  的沸点(填“>”或“<”)。
的沸点(填“>”或“<”)。
(5)经研究,发现可能存在第119号元素,有人称“类纺”,其位于元素周期表第八周期ⅠA族。有关“类钫”的预测正确的是 。
(6)实验室中 溶液久置后出现浑浊,请写出发生的化学反应方程式
溶液久置后出现浑浊,请写出发生的化学反应方程式_________________________ 。
(7)氰气[ ]称为拟卤素,与
]称为拟卤素,与 结构相似、性质相近。在
结构相似、性质相近。在 中元素
中元素___________ (写元素符号)显负价。
(1)化学与生活、生产息息相关。
①
 可用于制备纯碱; ②
可用于制备纯碱; ② 可用于葡萄酒保存;
可用于葡萄酒保存;③
 可用于制供氧剂; ④
可用于制供氧剂; ④ 可用于制耐火材料;
可用于制耐火材料;⑤CO可用于冶炼金属; ⑥
 可用于制硫酸;
可用于制硫酸;⑦
 可用于制硝酸
可用于制硝酸上述物质中,属于酸性氧化物的是
(2)硝酸是用途广泛的重要化工原科。氨的催化氧化是工业合成硝酸的重要步骤,其中氧化剂与还原剂物质的量之比为
(3)央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。明胶是水溶性蛋白质混合物,溶于水形成胶体。明胶的水溶液与NaCl溶液的共同点是
A.都可以产生丁达尔效应 B.都属于混合物 C.都能透过滤纸
(4)氮、磷都是生命元素,它们的氢化物结构相似。
 的沸点
的沸点 的沸点(填“>”或“<”)。
的沸点(填“>”或“<”)。(5)经研究,发现可能存在第119号元素,有人称“类纺”,其位于元素周期表第八周期ⅠA族。有关“类钫”的预测正确的是 。
| A.“类钫”单质具有强氧化性 | B.“类钫”单质能与冷水剧烈反应 |
| C.“类钫”最高价氧化物对应的水化物为弱碱 | D.“类钫”在化合物中显+1价 |
 溶液久置后出现浑浊,请写出发生的化学反应方程式
溶液久置后出现浑浊,请写出发生的化学反应方程式(7)氰气[
 ]称为拟卤素,与
]称为拟卤素,与 结构相似、性质相近。在
结构相似、性质相近。在 中元素
中元素
您最近一年使用:0次
【推荐2】我国法律规定,禁止酒后驾车。
(1)手持式酒精检测仪,检测呼出气体中乙醇浓度(BrAC)的主要原理为: 2K2Cr2O7+3C2H5OH+8H2SO4=2Cr2(SO4)3+2K2SO4+3___________+11H2O
①在横线上填相应的产物___________ 。
②判断司机酒驾所依据的现象是___________ 。
(2)BrAC一般作为酒驾检测的初筛手段,进一步是检测血液的乙醇浓度(BAC)。法律规定,20mg/10mL<BAC<80mg/100mL为酒后驾驶;BAC≥80mg/100mL为醉酒驾驶,BrAC与BAC的关系是:BAC(mg/L)=BrAC(mg/L)×2200,裁定醉酒驾驶BrAC的大小范围是___________ mg/L。
(3)近年又发展检测唾液中乙醇含量的方法,原理如下:
Ⅰ.将试纸浸入唾液10秒后取出,试纸中的乙醇在酶的作用下被空气氧化为CH3CHO和H2O2,写出化学方程式___________ 。
Ⅱ.H2O2与3,3′,5,5′—四甲基联苯胺(图1)反应反应一种有色化合物,颜色变化程度与乙醇含量成正比。

①被定义为“1”和“1”的碳原子是哪两个,在图1所示结构简式上将之涂黑。___________
②图2所示有机物的名称是___________ 。
(1)手持式酒精检测仪,检测呼出气体中乙醇浓度(BrAC)的主要原理为: 2K2Cr2O7+3C2H5OH+8H2SO4=2Cr2(SO4)3+2K2SO4+3___________+11H2O
①在横线上填相应的产物
②判断司机酒驾所依据的现象是
(2)BrAC一般作为酒驾检测的初筛手段,进一步是检测血液的乙醇浓度(BAC)。法律规定,20mg/10mL<BAC<80mg/100mL为酒后驾驶;BAC≥80mg/100mL为醉酒驾驶,BrAC与BAC的关系是:BAC(mg/L)=BrAC(mg/L)×2200,裁定醉酒驾驶BrAC的大小范围是
(3)近年又发展检测唾液中乙醇含量的方法,原理如下:
Ⅰ.将试纸浸入唾液10秒后取出,试纸中的乙醇在酶的作用下被空气氧化为CH3CHO和H2O2,写出化学方程式
Ⅱ.H2O2与3,3′,5,5′—四甲基联苯胺(图1)反应反应一种有色化合物,颜色变化程度与乙醇含量成正比。

①被定义为“1”和“1”的碳原子是哪两个,在图1所示结构简式上将之涂黑。
②图2所示有机物的名称是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】今有10种物质:①Al;②氢氧化钠溶液;③Na2FeO4;④NH3;⑤CO2;⑥Al2O3; ⑦石墨;⑧Cl2;⑨NaHCO3;⑩酒精,按要求完成下列填空。
(1)以上物质属于电解质_______ (填写相应的编号);
(2)写出②和⑨的溶液反应的离子方程式_______ ;
(3)⑤可以和Na2O2反应,写出该反应的化学方程式_______ 。
(4)⑧可以用于制备“战略金属”钛,有关反应如下,该反应中氧化剂是_______ (填化学式)。TiO2+2C+2Cl2 TiCl4+2CO;
TiCl4+2CO;
(5)③称为高铁酸钠,是水处理过程中的一种新型的绿色多功能净水剂。从物质分类的角度,高铁酸钠属于_______ (“酸”、“碱”、“盐”或“氧化物”),高铁酸钠净水过程中发生的化学反应主要是:Na2FeO4+_______H2O=_______Fe(OH)3(胶体)+_______O2↑+_______NaOH,请配平该化学方程式_______ 。
(6)0.5 mol Al2O3的质量为_______ ;3.4 g NH3所含分子数为_______ (用NA表示);
(1)以上物质属于电解质
(2)写出②和⑨的溶液反应的离子方程式
(3)⑤可以和Na2O2反应,写出该反应的化学方程式
(4)⑧可以用于制备“战略金属”钛,有关反应如下,该反应中氧化剂是
 TiCl4+2CO;
TiCl4+2CO;(5)③称为高铁酸钠,是水处理过程中的一种新型的绿色多功能净水剂。从物质分类的角度,高铁酸钠属于
(6)0.5 mol Al2O3的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】
(1)已知硫酸锰(MnSO4)和过硫酸钾(K2S2O8)两种盐溶液在银离子催化下可发生氧化还原反应,生成高锰酸钾、硫酸钾和硫酸。请写出并配平上述反应的化学方程式____________________ 。
(2)在热的稀硫酸溶液中溶解了11.4g FeSO4,当加入50mL 0.5 mol/L KNO3溶液后,使其中的Fe2+全部氧化成Fe3+,KNO3也反应完全,并有NxOy氮氧化物气体逸出。
x=______ ,y=_______ 。
(3) ___FeSO4+___KNO3+___H2SO4→___K2SO4+___Fe2(SO4)3+___NxOy+___H2O,配平上述化学方程式并用单线桥表明电子转移的方向和数目(将配平后的系数填在相应的空格中)__________________________________________ 。
(1)已知硫酸锰(MnSO4)和过硫酸钾(K2S2O8)两种盐溶液在银离子催化下可发生氧化还原反应,生成高锰酸钾、硫酸钾和硫酸。请写出并配平上述反应的化学方程式
(2)在热的稀硫酸溶液中溶解了11.4g FeSO4,当加入50mL 0.5 mol/L KNO3溶液后,使其中的Fe2+全部氧化成Fe3+,KNO3也反应完全,并有NxOy氮氧化物气体逸出。
x=
(3) ___FeSO4+___KNO3+___H2SO4→___K2SO4+___Fe2(SO4)3+___NxOy+___H2O,配平上述化学方程式并用单线桥表明电子转移的方向和数目(将配平后的系数填在相应的空格中)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在反应5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O中,氧化剂是__________ ,还原剂是__________ ;氧化剂具有__________ 性;被氧化和被还原的原子数之比是__________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知Ksp[Fe(OH)3]=2.6×10-39,回答下列问题:
(1) FeCl3溶液可用做净水剂,其净水原理为(用离子方程式表示):______________________ 。
(2)某酸性MgCl2 溶液中含有少量FeCl3,为得到纯净的MgCl2溶液,可加入___________ 调节溶液的pH=4,使溶液中的Fe3+变为Fe(OH)3 沉淀,此时溶液中的c(Fe3+)=_________________ 。
(3)由FeCl3·6H2O 晶体得到纯的无水FeCl3的合理方法是:______________________________ 。
(4)草酸亚铁是制备高纯度活性铁粉的原料,其样品纯度测定步骤如下:准确称取草酸亚铁(FeC2O4)样品wg ,将其研成粉末后溶于适量的稀硫酸中(假设杂质不反应)配成250omL溶液。准确量取20mL 该溶液于锥形瓶中,用c mol/L 的K2Cr2O7 酸性溶液(用稀硫酸酸化) 滴定至终点,消耗滴定液VmL(还原产物为Cr3+,氧化产物为Fe3+和CO2)。
①滴定时反应的离子方程式为____________________________________ 。
②该草酸亚铁样品的纯度为___________________________ 。
(1) FeCl3溶液可用做净水剂,其净水原理为(用离子方程式表示):
(2)某酸性MgCl2 溶液中含有少量FeCl3,为得到纯净的MgCl2溶液,可加入
(3)由FeCl3·6H2O 晶体得到纯的无水FeCl3的合理方法是:
(4)草酸亚铁是制备高纯度活性铁粉的原料,其样品纯度测定步骤如下:准确称取草酸亚铁(FeC2O4)样品wg ,将其研成粉末后溶于适量的稀硫酸中(假设杂质不反应)配成250omL溶液。准确量取20mL 该溶液于锥形瓶中,用c mol/L 的K2Cr2O7 酸性溶液(用稀硫酸酸化) 滴定至终点,消耗滴定液VmL(还原产物为Cr3+,氧化产物为Fe3+和CO2)。
①滴定时反应的离子方程式为
②该草酸亚铁样品的纯度为
您最近一年使用:0次



