下列有关离子反应的叙述不 正确的是( )
| A.溶液中有难溶于水的沉淀生成是离子反应的发生条件之一 |
| B.离子反应发生的方向总是向着溶液中离子浓度降低的方向进行 |
| C.离子反应生成的沉淀的溶解度为零 |
| D.生成沉淀的离子反应之所以能发生,在于生成物的溶解度小 |
更新时间:2019-11-05 08:19:41
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】室温下,将0.3molBaSO4加入5L1mol/LNa2CO3溶液中,不考虑体积变化,达到平衡时,c(SO )=0.02mol/L,下列说法错误的是
)=0.02mol/L,下列说法错误的是
 )=0.02mol/L,下列说法错误的是
)=0.02mol/L,下列说法错误的是| A.有BaCO3沉淀生成 |
| B.依据题干信息可推出:Ksp[BaSO4]<Ksp[BaCO3] |
| C.向溶液中继续加入少量Na2CO3固体,BaCO3沉淀增多 |
| D.向溶液中继续加入少量蒸馏水,BaCO3沉淀减少 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列陈述I与陈述II均正确, 且有因果关系的是
| 选项 | 陈述I | 陈述II |
| A | SO2具有氧化性 | 在葡萄酒酿制过程中添加适量SO2 |
| B | 人体需要补充铁单质 | 酱油中加入铁强化剂 |
| C | NaHCO3受热易分解生成CO2气体 | 用纯碱焙制糕点 |
| D | S2-能与Cu2+、Hg2+生成难溶的硫化物沉淀 | 用Na2S处理 含Cu2+、Hg2+的工业废水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】根据下列图示所得出的结论不正确的是


| A.由图甲可知,除去CuSO4溶液中的Fe3+可加入适量CuO调节pH至4左右 |
B.图乙是一定温度下三种碳酸盐的沉淀溶解平衡曲线,a点可表示MgCO3的不饱和溶液,且c(Mg2+)<c(CO ) ) |
C.图丙是室温下AgCl和AgI的饱和溶液中离子浓度的关系曲线,该温度下反应AgCl(s)+I-(aq) AgI(s)+Cl-(aq)的平衡常数K=2.5×106 AgI(s)+Cl-(aq)的平衡常数K=2.5×106 |
| D.图丁是室温下AgCl和Ag2CrO4的沉淀溶解平衡曲线,阴影区域中的点可以同时生成Ag2CrO4沉淀和AgCl沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】将等量的固体Mg(OH)2,置于等体积的下列液体中,最终固体剩余最少的是( )
| A.在纯水中 | B.在0.1mol/L的MgCl2溶液中 |
| C.在0.1mol/L的NH3·H2O中 | D.在0.1mol/L的CH3COOH溶液中 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】化学用语是学习化学的工具和基础。下列化学用语错误的是
| A.钢铁的吸氧腐蚀电极总反应:2Fe +O2 +2H2O= 2Fe(OH)2 |
B.醋酸铵的水解反应:CH3COO- + + H2O + H2O CH3COOH + NH3·H2O CH3COOH + NH3·H2O |
C.AgCl沉淀溶解平衡:AgCl(s) AgCl(aq) = Ag+ (aq)+C1-(aq) AgCl(aq) = Ag+ (aq)+C1-(aq) |
D.氨在水中反应:NH3 + H2O NH3·H2O = NH3·H2O = +OH- +OH- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在一定温度下,一定量的水中石灰乳悬浊液存在下列平衡:
Ca(OH)2(s)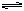 Ca2+(aq)+2OH-(aq)
Ca2+(aq)+2OH-(aq)
当向浑浊液中加入少量的生石灰,又恢复到原温度时,下列说法中正确的是
Ca(OH)2(s)
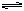 Ca2+(aq)+2OH-(aq)
Ca2+(aq)+2OH-(aq)当向浑浊液中加入少量的生石灰,又恢复到原温度时,下列说法中正确的是
| A.溶液中Ca2+数不变 | B.c(Ca2+)增大 |
| C.pH不变 | D.pH增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知Ksp(AgCl)=1.8×10-10。向盛有0.1 mol/L AgNO3溶液的试管中滴加等体积0.1 mol/L NaCl溶液,静置沉降,取上层清液和下层悬浊液分别进行实验。下列判断正确的是
| A.上层清液为AgCl的饱和溶液 |
| B.向清液中滴加0.1 mol/L AgNO3溶液,c(Cl-)不变 |
| C.向悬浊液中滴加0.1 mol/L KI溶液,不会有明显变化 |
| D.向悬浊液中加入适量浓氨水,混合液变澄清,说明AgCl可溶于强碱 |
您最近一年使用:0次





