回答下列关于铁元素及其化合物的知识:
(1)将 NaOH 溶液滴入 FeSO4溶液中,能观察到的现象是___ ,请写出产物颜色变化时发生的反应方程式___ 。
(2)实验室配制氯化铁溶液时,通常应将氯化铁固体溶解在加有少量___ 的水中; FeCl2溶液在空气中放置一段时间后,逐渐变成浅黄色,其原因是___ 。(用离子方程式表示)
(3)在常温下,铁与水并不起反应,但在高温下,铁与水蒸气可发生反应。该反应的化学方程式_________________ ,该反应中的还原剂是___ ,氧化剂是___ 。
(4)在 100mL18mol/L的浓硫酸中加入过量的铁片,加热使之充分反应,产生的气体在标准状况下的体积可能是___ 。
A.40.32L B.25.76L C.20.16L D.6.72L
(1)将 NaOH 溶液滴入 FeSO4溶液中,能观察到的现象是
(2)实验室配制氯化铁溶液时,通常应将氯化铁固体溶解在加有少量
(3)在常温下,铁与水并不起反应,但在高温下,铁与水蒸气可发生反应。该反应的化学方程式
(4)在 100mL18mol/L的浓硫酸中加入过量的铁片,加热使之充分反应,产生的气体在标准状况下的体积可能是
A.40.32L B.25.76L C.20.16L D.6.72L
更新时间:2019-11-07 18:35:37
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】国家规定,酿造食醋的总酸含量标准为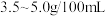 (总酸含量即
(总酸含量即 食醋中含醋酸的质量)。某兴趣小组为测定一市售食醋的总酸含量,进行了实验。实验后,得知
食醋中含醋酸的质量)。某兴趣小组为测定一市售食醋的总酸含量,进行了实验。实验后,得知 该食醋样品与
该食醋样品与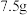 溶质的质量分数为
溶质的质量分数为 的氢氧化钠溶液恰好完全反应。计算该市售食醋样品中的总酸含量,并说明是否符合国家标准
的氢氧化钠溶液恰好完全反应。计算该市售食醋样品中的总酸含量,并说明是否符合国家标准______ 。(食醋和氢氧化钠反应的化学方程式: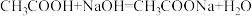 假设该市售食醋样品中其它物质不与氢氧化钠发生反应)
假设该市售食醋样品中其它物质不与氢氧化钠发生反应)
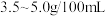 (总酸含量即
(总酸含量即 食醋中含醋酸的质量)。某兴趣小组为测定一市售食醋的总酸含量,进行了实验。实验后,得知
食醋中含醋酸的质量)。某兴趣小组为测定一市售食醋的总酸含量,进行了实验。实验后,得知 该食醋样品与
该食醋样品与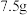 溶质的质量分数为
溶质的质量分数为 的氢氧化钠溶液恰好完全反应。计算该市售食醋样品中的总酸含量,并说明是否符合国家标准
的氢氧化钠溶液恰好完全反应。计算该市售食醋样品中的总酸含量,并说明是否符合国家标准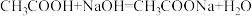 假设该市售食醋样品中其它物质不与氢氧化钠发生反应)
假设该市售食醋样品中其它物质不与氢氧化钠发生反应)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】为测定空气中SO2的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的100mL0.100mol/L的酸性KMnO4溶液(假定样品无其他还原性气体),已知SO2与该溶液反应的离子方程式为:5SO2+2 +2H2O=5
+2H2O=5 +2Mn2++4H+。若管道中空气流量为aL/min,经过bmin溶液恰好褪色,假定样品中的SO2可被溶液充分吸收。请计算:
+2Mn2++4H+。若管道中空气流量为aL/min,经过bmin溶液恰好褪色,假定样品中的SO2可被溶液充分吸收。请计算:
(1)题中消耗的KMnO4的物质的量为_____ mol。
(2)过程中转移的电子数为_____ (用NA表示)。
(3)则该空气样品中SO2的含量_____ g/L(用含a、b的代数式表示)。
 +2H2O=5
+2H2O=5 +2Mn2++4H+。若管道中空气流量为aL/min,经过bmin溶液恰好褪色,假定样品中的SO2可被溶液充分吸收。请计算:
+2Mn2++4H+。若管道中空气流量为aL/min,经过bmin溶液恰好褪色,假定样品中的SO2可被溶液充分吸收。请计算:(1)题中消耗的KMnO4的物质的量为
(2)过程中转移的电子数为
(3)则该空气样品中SO2的含量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】从下列提供的物质中选择合适的物质填空,并完成相应的问题。
①BaCl2②NaHCO3③KMnO4④CuCl2⑤稀H2SO4⑥KI⑦FeCl2⑧稀HNO3⑨NaOH⑩NH4Cl
(1)写出②在水中的电离方程式____ 。
(2)上述物质中能与⑨能发生反应的物质有____ 种,其中⑩与⑨在加热条件下发生反应的离子方程式为___ ,将⑨溶液滴入⑦中会观察到____ 现象。
(3)上述物质中常见的还原剂有______ 。
(4)写出③⑤⑥反应的离子方程式____ 。
①BaCl2②NaHCO3③KMnO4④CuCl2⑤稀H2SO4⑥KI⑦FeCl2⑧稀HNO3⑨NaOH⑩NH4Cl
(1)写出②在水中的电离方程式
(2)上述物质中能与⑨能发生反应的物质有
(3)上述物质中常见的还原剂有
(4)写出③⑤⑥反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知甲、乙、丙物质分别由H、C、Na、O、Cl、Fe元素中的一种或几种组成。
(1)若甲物质俗称为小苏打,则甲的化学式为_______ 。
(2)若乙物质在空气中迅速变成灰绿色,最后变成红褐色,,则该反应的化学方程式为_______ 。
(3)若丙物质在常温常压下为黄绿色气体,则实验室制取丙的化学方程式为:_______ 。
(4)2019年诺贝尔化学奖颁给锂离子电池领域,获奖科学家的重要贡献之一是研发出了电极材料——磷酸亚铁锂( )。
)。 的一种制备方法如下。
的一种制备方法如下。

① 中,铁元素的化合价为
中,铁元素的化合价为_______ 价。
②将反应Ⅰ的离子方程式配平:_______ 。
_______ _______
_______ _______
_______ _______
_______ _______
_______
(1)若甲物质俗称为小苏打,则甲的化学式为
(2)若乙物质在空气中迅速变成灰绿色,最后变成红褐色,,则该反应的化学方程式为
(3)若丙物质在常温常压下为黄绿色气体,则实验室制取丙的化学方程式为:
(4)2019年诺贝尔化学奖颁给锂离子电池领域,获奖科学家的重要贡献之一是研发出了电极材料——磷酸亚铁锂(
 )。
)。 的一种制备方法如下。
的一种制备方法如下。
①
 中,铁元素的化合价为
中,铁元素的化合价为②将反应Ⅰ的离子方程式配平:
_______
 _______
_______ _______
_______ _______
_______ _______
_______
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】铁元素在地壳中含量居于第四位。铁是目前产量最大,使用最广泛的金属。我国目前发现最早的人工冶铁制品是河南三门峡出土的西周晚期的玉柄铁剑。
(1)在钢铁厂的生产中,炽热的铁水或钢水注入模具之前必须进行充分的干燥处理,不得留有水,请用化学方程式解释___________ 。
(2)电子工业中常用FeCl3溶液作为“腐蚀液”腐蚀覆铜板,请用离子方程式解释该现象:___________ 。
(3)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,其一种制备原理如下:_______ClO- ___________
___________ ___________=___________
___________=___________ ___________
___________ ___________
___________ ,请将方程式补充完整并配平该方程式
,请将方程式补充完整并配平该方程式__________ 。
(4) 很不稳定,露置在空气中容易被氧化,该反应的化学方程式为
很不稳定,露置在空气中容易被氧化,该反应的化学方程式为___________ ,现象为___________ 。
(5)向一个金属铝的易拉罐内充满CO2,然后向罐内注入足量NaOH溶液,立即用胶布严封罐口,过一段时间后,罐壁内凹而瘪,再过一段时间后,瘪了的罐壁重新鼓起,请用离子方程式解释罐子重新鼓起的现象:___________ 。
(1)在钢铁厂的生产中,炽热的铁水或钢水注入模具之前必须进行充分的干燥处理,不得留有水,请用化学方程式解释
(2)电子工业中常用FeCl3溶液作为“腐蚀液”腐蚀覆铜板,请用离子方程式解释该现象:
(3)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,其一种制备原理如下:_______ClO-
 ___________
___________ ___________=___________
___________=___________ ___________
___________ ___________
___________ ,请将方程式补充完整并配平该方程式
,请将方程式补充完整并配平该方程式(4)
 很不稳定,露置在空气中容易被氧化,该反应的化学方程式为
很不稳定,露置在空气中容易被氧化,该反应的化学方程式为(5)向一个金属铝的易拉罐内充满CO2,然后向罐内注入足量NaOH溶液,立即用胶布严封罐口,过一段时间后,罐壁内凹而瘪,再过一段时间后,瘪了的罐壁重新鼓起,请用离子方程式解释罐子重新鼓起的现象:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】工业尾气中的氯气有多种处理方法。
(1)处理尾气中少量氯气的方法如图所示。
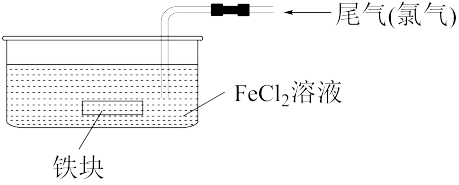
①处理过程中,发生反应的离子方程式为_______ 。
②为维持处理过程的持续进行,需要定期加入的物质是_______ 。
(2)大量氯气可用NaOH溶液处理,标准状况下,处理11.2L Cl2转移电子的物质的量为_______ mol。
(1)处理尾气中少量氯气的方法如图所示。

①处理过程中,发生反应的离子方程式为
②为维持处理过程的持续进行,需要定期加入的物质是
(2)大量氯气可用NaOH溶液处理,标准状况下,处理11.2L Cl2转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】写出下列有关反应的离子方程式
(1)碳酸氢钠与偏铝酸钠溶液混合_______ 。
(2)向Ba(OH)2溶液中滴加NaHSO4溶液至Ba2+沉淀完成_______ ,继续滴加NaHSO4溶液_______ 。
(3)足量氯气通入溴化亚铁溶液中_______ 。
(4)磁性氧化铁溶于氢碘酸中_______ 。
(5)过氧化钠与水反应_______ 。
(6)金属钠与硫酸铜溶液反应_______ 。
(1)碳酸氢钠与偏铝酸钠溶液混合
(2)向Ba(OH)2溶液中滴加NaHSO4溶液至Ba2+沉淀完成
(3)足量氯气通入溴化亚铁溶液中
(4)磁性氧化铁溶于氢碘酸中
(5)过氧化钠与水反应
(6)金属钠与硫酸铜溶液反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】铁是人类较早使用的金属之一,运用所学知识,回答下列问题。
I.某学习小组研究 腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
(1)从 腐蚀铜后的废液中回收铜,并获得
腐蚀铜后的废液中回收铜,并获得 溶液,设计如下方案:
溶液,设计如下方案:
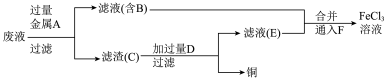
滤渣C中所含物质的化学式为___________ ;通入F发生反应的离子方程式为___________ 。
II.学习小组同学继续研究铁与水蒸气的反应,分别进行了如图实验。
请回答:
(2)实验I中反应的化学方程式是___________ 。
(3)甲同学观察到实验I中持续产生肥皂泡,但实验II中溶液B未呈现红色,则溶液B未呈现红色的原因是___________ 。(写出反应的离子方程式)
(4)实验室在制备 时必须隔绝空气,否则发生的现象是
时必须隔绝空气,否则发生的现象是___________ ;反应化学方程式为___________ 。
I.某学习小组研究
 腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
腐蚀铜后所得的废液成分并回收铜,进行了如下实验:(1)从
 腐蚀铜后的废液中回收铜,并获得
腐蚀铜后的废液中回收铜,并获得 溶液,设计如下方案:
溶液,设计如下方案:
滤渣C中所含物质的化学式为
II.学习小组同学继续研究铁与水蒸气的反应,分别进行了如图实验。
| 实验I | 实验II |
 | 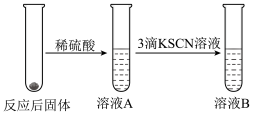 |
(2)实验I中反应的化学方程式是
(3)甲同学观察到实验I中持续产生肥皂泡,但实验II中溶液B未呈现红色,则溶液B未呈现红色的原因是
(4)实验室在制备
 时必须隔绝空气,否则发生的现象是
时必须隔绝空气,否则发生的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请回答下列问题:
(1)氯化铝水溶液呈________ (填“酸”、“中”或“碱”)性,原因是(用离子方程式表示)________________________________________ ;把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是___________ (填化学式)。
(2)在配制硫化钠溶液时,为了防止发生水解,可以加入少量的________________ (填化学式)。
(3)已知纯水在T℃时,pH=6,该温度下某NaOH溶液的浓度为1 mol·L-1,则该溶液由水电离出的c(OH-)=________ mol·L-1。
(4)常温下,向一定体积的0.1 mol/L的醋酸溶液中加水稀释后,溶液的pH将___________ (填“增大”、“不变”或“减小”)。关于该稀释过程下列说法正确的是_____ 。
A.溶液中导电粒子的数目减少 B.醋酸的电离程度增大,c(H+)也增大
C.溶液中 不变 D.溶液中
不变 D.溶液中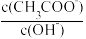 增大
增大
(5)常温下,浓度均为0.1 mol/L的五种溶液的pH如下表所示。
根据表中数据,回答问题:
①若分别稀释等浓度的下列四种酸溶液(稀释倍数相同),pH变化最小的是_________ ;
A.HCN B.HClO C.H2CO3 D.CH3COOH
②等体积等浓度的NaCN、NaClO两溶液中所含阴、阳离子总数的大小关系为_________ 。
A.前者大 B.相等 C.后者大 D.无法确定
(1)氯化铝水溶液呈
(2)在配制硫化钠溶液时,为了防止发生水解,可以加入少量的
(3)已知纯水在T℃时,pH=6,该温度下某NaOH溶液的浓度为1 mol·L-1,则该溶液由水电离出的c(OH-)=
(4)常温下,向一定体积的0.1 mol/L的醋酸溶液中加水稀释后,溶液的pH将
A.溶液中导电粒子的数目减少 B.醋酸的电离程度增大,c(H+)也增大
C.溶液中
 不变 D.溶液中
不变 D.溶液中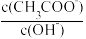 增大
增大(5)常温下,浓度均为0.1 mol/L的五种溶液的pH如下表所示。
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
根据表中数据,回答问题:
①若分别稀释等浓度的下列四种酸溶液(稀释倍数相同),pH变化最小的是
A.HCN B.HClO C.H2CO3 D.CH3COOH
②等体积等浓度的NaCN、NaClO两溶液中所含阴、阳离子总数的大小关系为
A.前者大 B.相等 C.后者大 D.无法确定
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有以下物质:①石墨;②氯化氢气体;③酒精;④氨水;⑤二氧化碳;⑥碳酸氢钠固体;⑦氯化铁溶液;⑧纯醋酸;⑨氧化钠固体;⑩铝。
(1)属于非电解质的是______________ ;属于强电解质的是__________ ;属于弱电解质的是___________ 。(用序号填空)
(2)写出物质⑥溶于水溶液显碱性的原因_______ (用离子方程式和简要文字说明作答)
(3)写出物质⑥和⑧在水中反应的离子方程式:_____________ 。
(4)配制溶液⑦时通常将⑦先溶于___________ ,然后再加水稀释,通过增加溶液中_______ 的浓度以防止其发生水解。
(5)浓度、体积相同的②和⑧的溶液,加入相同形状且足量的Zn粒,反应速率快的是___ (用序号填空);pH值、体积相同的②和⑧的溶液时,产生气体的量多的是________ 。(用序号填空)
(1)属于非电解质的是
(2)写出物质⑥溶于水溶液显碱性的原因
(3)写出物质⑥和⑧在水中反应的离子方程式:
(4)配制溶液⑦时通常将⑦先溶于
(5)浓度、体积相同的②和⑧的溶液,加入相同形状且足量的Zn粒,反应速率快的是
您最近一年使用:0次



