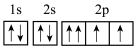
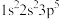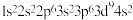写出下列原子或离子的核外电子排布式,并判断各元素在元素周期表中的位置。
(1)17Cl:____ ,第____ 周期____ 族。
(2)24Cr:____ ,第____ 周期____ 族。
(3)26Fe3+:____ ,第____ 周期____ 族。
(1)17Cl:
(2)24Cr:
(3)26Fe3+:
更新时间:2019-11-18 04:12:33
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】硅及其化合物在工业中有很多用处,一些硅的卤化物的熔点如表所示:
完成下列填空:
(1)硅原子核外电子共有______ 种形状不同的电子云,画出基态硅原子最外层电子的轨道表示式______ 。
(2)表中四种卤化物分子的空间结构均为______ ,由此推断 的键角为
的键角为______ , 属于
属于______ (填“极性”或“非极性”)分子。
(3)已知 (熔点为-56.6℃)和
(熔点为-56.6℃)和 (熔点为1713℃)熔点相差较大;原因是
(熔点为1713℃)熔点相差较大;原因是______ ,表中四种卤化硅熔点存在差异的原因是______ 。
完成下列填空:
卤化物 |
|
|
|
|
熔点/℃ | -90.2 | 70.4 | 5.2 | 120.5 |
(1)硅原子核外电子共有
(2)表中四种卤化物分子的空间结构均为
 的键角为
的键角为 属于
属于(3)已知
 (熔点为-56.6℃)和
(熔点为-56.6℃)和 (熔点为1713℃)熔点相差较大;原因是
(熔点为1713℃)熔点相差较大;原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】氮、磷、砷是同主族元素,均广泛用于农药、化肥等化工产品,请回答下列问题。
(1)画出基态砷原子价层电子的轨道表示式_______ 。
(2)NH3、PH3、AsH3的沸点由高到低的顺序为_______ (填化学式)。NH3、PH3、AsH3稳定性由强到弱的顺序为_______ (填化学式)。
(3)水和氨中心原子的杂化类型相同,但H2O的键角小于NH3的,其原因为_______ 。
(4)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态的磷原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的磷原子,其价电子自旋磁量子数的代数和为_______ 。
(5)已知有关氮、磷的单键和三键的键能(kJ·mol-1)如表:
请你预测键长:N—N_______ N≡N(填“>”或“<”),从N2、N4、P2、P4的能量角度看,氮气以N2而白磷以P4形式存在的原因是_______ 。
(6)2022年起,曾经的“天价药”诺西那生钠正式实施医保价格,一针直降几十万元人民币。诺西那生钠,用于治疗脊髓性肌肉菱缩症(SMA)。其结构片段如图所示。
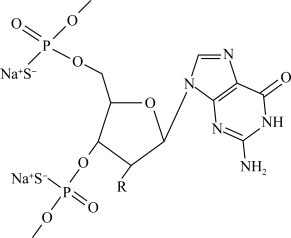 (R为OCH2CH2OCH3)
(R为OCH2CH2OCH3)
该结构片段中含有_______ 个手性碳原子。
(1)画出基态砷原子价层电子的轨道表示式
(2)NH3、PH3、AsH3的沸点由高到低的顺序为
(3)水和氨中心原子的杂化类型相同,但H2O的键角小于NH3的,其原因为
(4)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+
 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态的磷原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的磷原子,其价电子自旋磁量子数的代数和为(5)已知有关氮、磷的单键和三键的键能(kJ·mol-1)如表:
| N—N | N≡N | P—-P | P≡P |
| 193 | 946 | 197 | 489 |
请你预测键长:N—N
(6)2022年起,曾经的“天价药”诺西那生钠正式实施医保价格,一针直降几十万元人民币。诺西那生钠,用于治疗脊髓性肌肉菱缩症(SMA)。其结构片段如图所示。
 (R为OCH2CH2OCH3)
(R为OCH2CH2OCH3)该结构片段中含有
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】回答下列问题:
(1)基态钛原子的价层电子排布式为_______ ,其原子核外电子的空间运动状态有_______ 种,共有_______ 种运动状态不同的电子。
(2)基态Si原子,若其电子排布式表示为[Ne]3s23p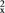 违背了
违背了_______ 。
(3)①基态Cu原子有_______ 种不同能级的电子。铜或铜盐的焰色试验为绿色,该光谱是_______ (填“吸收光谱”或“发射光谱”)。
②N原子中最高能级的电子的电子云轮廓图为_______ 。
③在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是_______ 。
(1)基态钛原子的价层电子排布式为
(2)基态Si原子,若其电子排布式表示为[Ne]3s23p
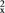 违背了
违背了(3)①基态Cu原子有
②N原子中最高能级的电子的电子云轮廓图为
③在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】按要求完成下列填空:
(1)核内有10个质子的原子的结构示意图_______ ;
(2)核外有10个电子的一价阴离子的结构示意图_______ ;
(3)核外有18个电子的二价阳离子的结构示意图_______ ;
(4)基态P原子核外电子排布式_______ ;
(5)基态As原子核外电子排布图_______ ;
(6)某元素基态原子N层只有2个电子,M层全充满,该元素名称是_______ ;
(7)某元素基态原子是第四周期未成对电子最多的,该元素符号是_______ 。
(1)核内有10个质子的原子的结构示意图
(2)核外有10个电子的一价阴离子的结构示意图
(3)核外有18个电子的二价阳离子的结构示意图
(4)基态P原子核外电子排布式
(5)基态As原子核外电子排布图
(6)某元素基态原子N层只有2个电子,M层全充满,该元素名称是
(7)某元素基态原子是第四周期未成对电子最多的,该元素符号是
您最近一年使用:0次
【推荐3】随着能源技术的发展,科学家们将目光聚焦于锂的开发与研究。
(1)基态Li原子中电子占据最高能级的符号是____ ,占据该能级电子的电子云轮廓图的形状为____ 形。
(2)在周期表中,与Li元素的化学性质最相似的邻族元素是____ (填元素符号)。
(3)部分元素的第一电离能(I1)如表所示。
①碱金属的第一电离能与碱金属的金属性的联系是____ 。
②Be的第一电离能比Li的大,从原子结构角度分析其原因是____ 。
(1)基态Li原子中电子占据最高能级的符号是
(2)在周期表中,与Li元素的化学性质最相似的邻族元素是
(3)部分元素的第一电离能(I1)如表所示。
| 元素 | Li | Be | Na | K |
| I1(kJ·mol-1) | 520 | 900 | 496 | 419 |
①碱金属的第一电离能与碱金属的金属性的联系是
②Be的第一电离能比Li的大,从原子结构角度分析其原因是
您最近一年使用:0次
【推荐1】我国科学家成功合成了世界上首个全氮阴离子盐,使氮原子簇化合物的研究有了新的突破。
(1)基态N原子中有___________ 个未成对电子,电子占据的最高能级的符号是___________ 。
(2)第二周期元素原子的第一电离能介于B、N之间的是___________ (填元素符号)。
(3)以氮化镓(GaN)等为代表的第三代半导体材料具有优异性能,基态 价层电子的轨道表示式
价层电子的轨道表示式___________ 。
(1)基态N原子中有
(2)第二周期元素原子的第一电离能介于B、N之间的是
(3)以氮化镓(GaN)等为代表的第三代半导体材料具有优异性能,基态
 价层电子的轨道表示式
价层电子的轨道表示式
您最近一年使用:0次
【推荐2】磷酸亚铁锂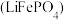 和锰酸锂
和锰酸锂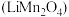 均可用作锂离子电池正极材料。回答下列问题:
均可用作锂离子电池正极材料。回答下列问题:
(1)基态O原子的价电子轨道表示式为___________ ;Mn的原子结构示意图为___________ 。
(2) 的熔、沸点
的熔、沸点___________ (填“高于”或“低于”) 。
。
(3) 分子中,与N原子相连的H呈正电性
分子中,与N原子相连的H呈正电性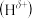 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性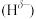 ,H、B、N电负性由小到大的顺序是
,H、B、N电负性由小到大的顺序是___________ 。
(4)已知: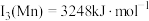 ,
,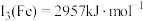 。Mn的第三电离能大于Fe的第三电离能,其主要原因是
。Mn的第三电离能大于Fe的第三电离能,其主要原因是___________ 。
(5)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种 配合物的结构如图所示,2mol该配合物中通过
配合物的结构如图所示,2mol该配合物中通过螯合作用 形成的配位键有___________ mol。
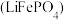 和锰酸锂
和锰酸锂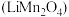 均可用作锂离子电池正极材料。回答下列问题:
均可用作锂离子电池正极材料。回答下列问题:(1)基态O原子的价电子轨道表示式为
(2)
 的熔、沸点
的熔、沸点 。
。(3)
 分子中,与N原子相连的H呈正电性
分子中,与N原子相连的H呈正电性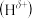 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性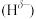 ,H、B、N电负性由小到大的顺序是
,H、B、N电负性由小到大的顺序是(4)已知:
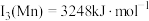 ,
,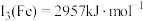 。Mn的第三电离能大于Fe的第三电离能,其主要原因是
。Mn的第三电离能大于Fe的第三电离能,其主要原因是(5)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种
 配合物的结构如图所示,2mol该配合物中通过
配合物的结构如图所示,2mol该配合物中通过
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】根据元素周期表中完整周期元素的性质,完成下列空格。
(1)在第三周期中,第一电离能最小的元素符号是_______ ,其原子的结构示意图为_______ ,第一电离能最大的元素符号是_______ ,其价电子排布式为_______ 。
(2)在元素周期表中,电负性最大的元素名称是_______ ,其价电子排布图为_______ 。
(3)第四周期元素中未成对电子数最多的元素符号是_______ ,其原子的简化电子排布式为_______ ,有_______ 个未成对电子。
(4)某元素的基态原子价电子排布式为3d104s1 ,该元素符号是_______ 。
(5)碳和氢形成的最简单碳正离子CH ,其中心原子碳原子的杂化类型为
,其中心原子碳原子的杂化类型为_______ ,该阳离子的空间构型为_______ 。
(6)向盛有CuSO4溶液的试管中滴加少量氨水,现象是_______ ,离子反应方程式为_______ ;继续滴加氨水至过量得到深蓝色溶液。经测定深蓝色是由于存在[Cu(NH3)4]SO4。其阳离子的结构式为_______ ,中心原子的配位数为_______ 。
(1)在第三周期中,第一电离能最小的元素符号是
(2)在元素周期表中,电负性最大的元素名称是
(3)第四周期元素中未成对电子数最多的元素符号是
(4)某元素的基态原子价电子排布式为3d104s1 ,该元素符号是
(5)碳和氢形成的最简单碳正离子CH
 ,其中心原子碳原子的杂化类型为
,其中心原子碳原子的杂化类型为(6)向盛有CuSO4溶液的试管中滴加少量氨水,现象是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】回答下列问题:
(1)醛基的电子式为___________ 。
(2)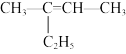 的系统命名是
的系统命名是___________ 。
(3)立方烷( )的二氯代物有
)的二氯代物有___________ 种。
(4)写出乙炔与水反应的化学方程式:___________ 。
(5)常温下,甲醇在水中的溶解度大于甲胺,原因是___________ 。
(1)醛基的电子式为
(2)
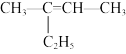 的系统命名是
的系统命名是(3)立方烷(
 )的二氯代物有
)的二氯代物有(4)写出乙炔与水反应的化学方程式:
(5)常温下,甲醇在水中的溶解度大于甲胺,原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】某元素原子序数为35,则
(1)此元素原子的电子总数是_______ ,有_______ 个未成对电子。
(2)有_______ 个电子层,有_______ 个原子轨道排布了电子。
(3)它的电子排布式为_______ 。
(4)该元素位于周期表第_______ 周期_______ 族。
(1)此元素原子的电子总数是
(2)有
(3)它的电子排布式为
(4)该元素位于周期表第
您最近一年使用:0次