工业废弃物的资源化回收再利用,可以更大限度地发挥原材料的价值。下图是工业生产纳米磁性氧化铁的流程:

下列说法不正确的是

下列说法不正确的是
| A.用Na2CO3溶液浸泡是为了除去废铁屑表面的油污 |
| B.若生产中不通入N2,暴露在空气中生产,将不能得到高纯度产品 |
| C.加适量的H2O2是为了将部分Fe2+氧化为Fe3+ ,涉及的反应:H2O2+2Fe2++2H+=2Fe3++2H2O |
| D.溶液A中Fe2+和Fe3+的浓度比为2∶1 |
更新时间:2019-11-19 18:13:24
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】以含镍废料(主要成分为NiO,含少量FeO、Fe2O3、CoO、BaO和SiO2)为原料制备NixOy和碳酸亚钴(CoCO3)的工艺流程如图。

下列说法正确的是

下列说法正确的是
| A.“滤渣1”的主要成分是H2SiO3、BaSO4 |
B.“氧化”时的离子反应为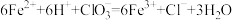 |
| C.“调pH"过程中形成黄钠铁矾渣,Na2CO3必须过量 |
D.“沉钴”过程发生的反应为 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】利用如下流程可从废光盘中回收金属层中的银(金属层中其他金属含量过低,对实验影响可忽略): 。下列说法正确的是
。下列说法正确的是

 。下列说法正确的是
。下列说法正确的是| A.若省略第一次过滤,会使氨水的用量增加 |
B.“氧化”时,发生的化学方程式: |
C.若“还原”工序利用原电池来实现,则 是正极产物 是正极产物 |
D.“还原”时,每生成1molAg,理论上消耗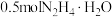 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】碲(52Te)被誉为“国防与尖端技术的维生素”;锡酸钠(Na2SnO3)可用于制造陶瓷电容器的基体。以锡碲渣(主要含Na2SnO3和Na2TeO3)为原料,回收锡酸钠并制备碲单质的流程图如下,下列说法错误的是
已知:锡酸钠(Na2SnO3)和亚碲酸钠(Na2TeO3)均易溶于碱。

已知:锡酸钠(Na2SnO3)和亚碲酸钠(Na2TeO3)均易溶于碱。

| A.在生产过程中,要将锡碲渣粉碎,其目的是增大锡碲渣的碱浸速率和浸出率 |
B.“氧化”时,反应的离子方程式为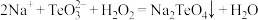 |
| C.“氧化”的温度应该越高越好,因为温度越高化学反应速率越快 |
D.以石墨为电极电解Na2TeO3溶液可获得Te,电解过程中阴极上的电极反应为: |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】CuBr是一种白色晶体,见光或潮湿时受热易分解,在空气中逐渐变为浅绿色。实验室制备CuBr的反应原理为:SO2+2CuSO4+2NaBr+ 2H2O=2CuBr↓+2H2SO4+Na2SO4,用下列装置进行实验,不能达到实验目的的是
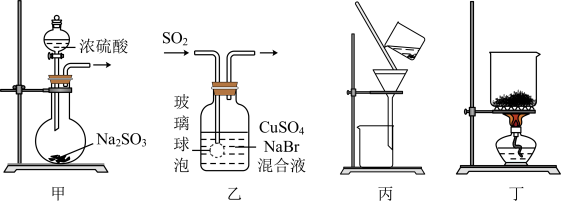

| A.用装置甲制取SO2 | B.用装置乙制取CuBr |
| C.用装置丙避光将CuBr与母液分离 | D.用装置丁干燥CuBr |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】类比(比较)是研究物质性质的常用方法之一,可预测许多物质的性质。但类比是相对的,不能违背客观实际。下列说法正确的是
| A.Fe能置换硫酸铜溶液的铜;则Na也能置换硫酸铜溶液的铜 |
| B.CaC2能水解:CaC2+2H2O=Ca(OH)2+C2H2↑;则Al4C3也能水解:Al4C3+12H2O =4Al(OH)3↓+3CH4↑ |
| C.工业上电解熔融MgCl2的制取金属镁;则也可以用电解熔融AlCl3的制取金属铝 |
| D.CO2与Na2O2反应生成Na2CO3和O2;则SO2与Na2O2反应生成Na2SO3和O2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下图所示装置可用来制取Fe(OH)2和观察Fe(OH)2在空气中被氧化时的颜色变化。实验提供的试剂:铁屑、6 mol/L硫酸溶液、NaOH溶液。下列说法错误的是( )
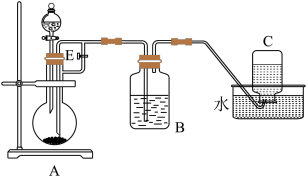
| A.B中盛有一定量的NaOH溶液,A中应预先加入的试剂是铁屑 |
| B.实验开始时应先将活塞E关闭 |
| C.生成Fe(OH)2的操作为:关闭E,使A中溶液压入B瓶中 |
| D.取下装置B中的橡皮塞,使空气进入,有关反应的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
您最近一年使用:0次

 是一种压电材料。以
是一种压电材料。以 为原料,采用下列路线可制备粉状
为原料,采用下列路线可制备粉状
 易溶于水的BaS和微溶于水的CaS;“沉淀”生成
易溶于水的BaS和微溶于水的CaS;“沉淀”生成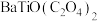 。下列说法正确的是
。下列说法正确的是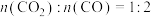

 ;
;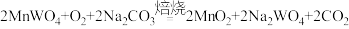 。
。
 离子结合质子的能力比SiO
离子结合质子的能力比SiO 离子强
离子强

