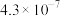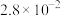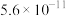已知19.2gCu与过量的200mL5mol/L 稀硝酸充分反应,反应方程式如下:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(1)写出该反应的离子方程式:________ ;
(2)标准状况下,产生NO气体的体积为:________ ;转移电子的物质的量为______ ;反应后NO3-的物质的量浓度为:______ 。(忽略反应前后溶液体积的变化)
(1)写出该反应的离子方程式:
(2)标准状况下,产生NO气体的体积为:
更新时间:2019-11-22 19:44:20
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】向一定量的Fe、FeO、Fe2O3的混合物中,加入100 mLl.0 mol·L-1的盐酸,恰好使混合物完全溶解并放出约224 mL(标准状况)气体,假设溶液体积不变,所得溶液中加入KSCN溶液无血红色出现。请回答下列问题:
(1)生成气体的物质的量为___ mol。
(2)所得溶液中溶质为___ (填化学式),物质的量浓度为___ mol·L-1。
(3)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量为___ g。
(4)原混合物的总质量为___ g。
(1)生成气体的物质的量为
(2)所得溶液中溶质为
(3)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量为
(4)原混合物的总质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某溶液中只含有Ba2+、Mg2+、Ag+三种阳离子,现用适量的NaOH溶液、稀盐酸和Na2SO4溶液将这三种离子逐一沉淀分离,其流程如图所示:
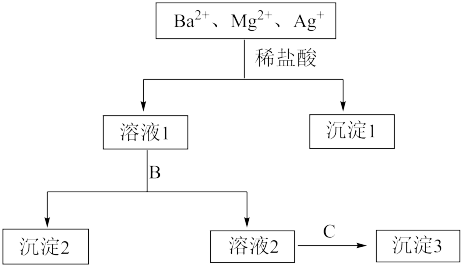
(1)沉淀1的化学式为_________ ,
(2)若试剂B为Na2SO4溶液,则沉淀2化学式为______________ 。
(3)若试剂B为NaOH溶液,则生成沉淀2的离子方程式为______________ 。
(4)如果原溶液中Ba2+、Mg2+、Ag+的浓度均为0.1mol·L-1,且溶液中含有的阴离子只有 ,则溶液中
,则溶液中 浓度为
浓度为_______ mol·L-1。

(1)沉淀1的化学式为
(2)若试剂B为Na2SO4溶液,则沉淀2化学式为
(3)若试剂B为NaOH溶液,则生成沉淀2的离子方程式为
(4)如果原溶液中Ba2+、Mg2+、Ag+的浓度均为0.1mol·L-1,且溶液中含有的阴离子只有
 ,则溶液中
,则溶液中 浓度为
浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为__________ mol•L-1。
(2)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.200mol•L-1的稀盐酸。可供选用的仪器有:A胶头滴管;B量筒;C烧杯;D天平;E玻璃棒。
①配制稀盐酸时,上述仪器中不需要使用的有 (选填字母),还缺少的仪器有__________ 。
②该学生需要用__________ mL量筒量取__________ mL上述浓盐酸进行配制。
③配制稀盐酸时,在洗涤操作中,将洗涤液全部移入容量瓶,其目的是__________ 。
④配制稀盐酸时,在定容操作中,应在距刻度线__________ 处,改用胶头滴管滴加蒸馏水至液面与__________ 。
⑤若出现如下情况,对所配溶液浓度将有何影响?(填“偏高”、“偏低”或“无影响”)定容时俯视刻度线__________ ;定容后经振荡、摇匀、静置,发现液面下降,再加适合的蒸馏水__________ 。
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:1.19g/cm3 质量分数:36.5% |
(1)该浓盐酸中HCl的物质的量浓度为
(2)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.200mol•L-1的稀盐酸。可供选用的仪器有:A胶头滴管;B量筒;C烧杯;D天平;E玻璃棒。
①配制稀盐酸时,上述仪器中不需要使用的有 (选填字母),还缺少的仪器有
②该学生需要用
③配制稀盐酸时,在洗涤操作中,将洗涤液全部移入容量瓶,其目的是
④配制稀盐酸时,在定容操作中,应在距刻度线
⑤若出现如下情况,对所配溶液浓度将有何影响?(填“偏高”、“偏低”或“无影响”)定容时俯视刻度线
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氧化还原反应、离子反应在生产生活中应用广泛。
(1) 和
和 都是大气污染物。利用氨水可以将
都是大气污染物。利用氨水可以将 和
和 吸收,原理如下图所示:
吸收,原理如下图所示:
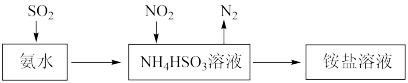
 被吸收的离子方程式是
被吸收的离子方程式是_____ 。
(2)用高能电子束激活烟气(主要成分是 等),会产生
等),会产生 等强氧化性微粒。烟气经下列过程可获得化肥。该化肥中含有的离子是
等强氧化性微粒。烟气经下列过程可获得化肥。该化肥中含有的离子是 、
、_____ (填离子符号)。

(3)SCR(选择性催化还原)工作原理

①尿素 水溶液热解为
水溶液热解为 和
和 ,该反应化学方程式
,该反应化学方程式_____
②反应器中 还原
还原 的化学方程式是
的化学方程式是_____
(4)NSR( 储存还原)的工作原理如下图所示,柴油发动机工作时在稀燃(
储存还原)的工作原理如下图所示,柴油发动机工作时在稀燃( 充足、柴油较少)和富燃(
充足、柴油较少)和富燃( 不足、柴油较多)条件下交替进行,通过
不足、柴油较多)条件下交替进行,通过 和
和 的相互转化实现
的相互转化实现 的储存和还原。
的储存和还原。
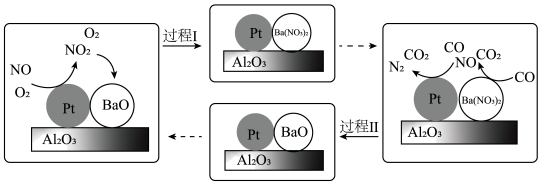
① 吸收
吸收 的反应中氧化剂与还原剂的粒子个数之比是
的反应中氧化剂与还原剂的粒子个数之比是_____ 。
②富燃条件下 表面反应的化学方程式是
表面反应的化学方程式是_____ 。
③若柴油中硫含量较高,在稀燃过程中, 吸收氮氧化物的能力下降至很低水平,结合化学方程式解释原因
吸收氮氧化物的能力下降至很低水平,结合化学方程式解释原因_____ 。
④研究 对
对 吸收氮氧化物的影响,一定温度下,测得气体中
吸收氮氧化物的影响,一定温度下,测得气体中 的体积分数与氮氧化物吸收率的关系如图所示。下列相关分析中正确的是
的体积分数与氮氧化物吸收率的关系如图所示。下列相关分析中正确的是_____ 。
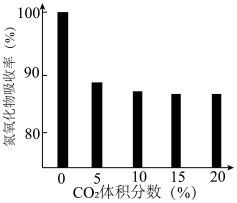
A.一定范围内,氮氧化物吸收率随 体积分数的增大而下降,原因可能是
体积分数的增大而下降,原因可能是 与
与 反应生成
反应生成 ,覆盖在
,覆盖在 表面
表面
B.当 体积分数达到
体积分数达到 时,氮氧化物吸收率依然
时,氮氧化物吸收率依然 体积分数
体积分数 较高,其原因可能是
较高,其原因可能是 在一定程度上也能吸收
在一定程度上也能吸收
C.以上分析均不对
(1)
 和
和 都是大气污染物。利用氨水可以将
都是大气污染物。利用氨水可以将 和
和 吸收,原理如下图所示:
吸收,原理如下图所示: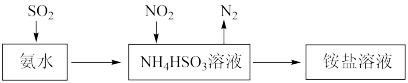
 被吸收的离子方程式是
被吸收的离子方程式是(2)用高能电子束激活烟气(主要成分是
 等),会产生
等),会产生 等强氧化性微粒。烟气经下列过程可获得化肥。该化肥中含有的离子是
等强氧化性微粒。烟气经下列过程可获得化肥。该化肥中含有的离子是 、
、
(3)SCR(选择性催化还原)工作原理

①尿素
 水溶液热解为
水溶液热解为 和
和 ,该反应化学方程式
,该反应化学方程式②反应器中
 还原
还原 的化学方程式是
的化学方程式是(4)NSR(
 储存还原)的工作原理如下图所示,柴油发动机工作时在稀燃(
储存还原)的工作原理如下图所示,柴油发动机工作时在稀燃( 充足、柴油较少)和富燃(
充足、柴油较少)和富燃( 不足、柴油较多)条件下交替进行,通过
不足、柴油较多)条件下交替进行,通过 和
和 的相互转化实现
的相互转化实现 的储存和还原。
的储存和还原。
①
 吸收
吸收 的反应中氧化剂与还原剂的粒子个数之比是
的反应中氧化剂与还原剂的粒子个数之比是②富燃条件下
 表面反应的化学方程式是
表面反应的化学方程式是③若柴油中硫含量较高,在稀燃过程中,
 吸收氮氧化物的能力下降至很低水平,结合化学方程式解释原因
吸收氮氧化物的能力下降至很低水平,结合化学方程式解释原因④研究
 对
对 吸收氮氧化物的影响,一定温度下,测得气体中
吸收氮氧化物的影响,一定温度下,测得气体中 的体积分数与氮氧化物吸收率的关系如图所示。下列相关分析中正确的是
的体积分数与氮氧化物吸收率的关系如图所示。下列相关分析中正确的是
A.一定范围内,氮氧化物吸收率随
 体积分数的增大而下降,原因可能是
体积分数的增大而下降,原因可能是 与
与 反应生成
反应生成 ,覆盖在
,覆盖在 表面
表面B.当
 体积分数达到
体积分数达到 时,氮氧化物吸收率依然
时,氮氧化物吸收率依然 体积分数
体积分数 较高,其原因可能是
较高,其原因可能是 在一定程度上也能吸收
在一定程度上也能吸收
C.以上分析均不对
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】如图是目前我国城市饮用水的生产流程,生活饮用水水质的标准主要有:色度、浑浊度、pH、细菌总数、气味等。

(1)目前我国规定一、二类水质的饮用水中铝含量不得高于0.2mg/L。已知常温下Al(OH)3的Ksp=3.2×10-34,如果某城市的出厂饮用水的pH为6,则水中Al3+含量为_______ mg/L,_______ (填“符合”或“不符合”)标准。
(2)流程中②的分离方式相当于化学基本操作中的_______ 操作,①、③中加氯气的作用是_______ 。氯气和水反应的离子方程式是_______ 。
(3)在污水处理分析时,常用双硫腙(H2Dz,二元弱酸)把金属离子络合成电中性的物质[如:Bi3++3H2Dz Bi(HDz)3+3H+],再经萃取把金属离子从水溶液中分离出来。设常温时该反应的化学平衡常数为K,则当pH=2时(此时,Bi3+以络合物形式被萃取分离的百分率为40%),废水中c(H2Dz)等于
Bi(HDz)3+3H+],再经萃取把金属离子从水溶液中分离出来。设常温时该反应的化学平衡常数为K,则当pH=2时(此时,Bi3+以络合物形式被萃取分离的百分率为40%),废水中c(H2Dz)等于_______ mol/L(用K表示)。

(1)目前我国规定一、二类水质的饮用水中铝含量不得高于0.2mg/L。已知常温下Al(OH)3的Ksp=3.2×10-34,如果某城市的出厂饮用水的pH为6,则水中Al3+含量为
(2)流程中②的分离方式相当于化学基本操作中的
(3)在污水处理分析时,常用双硫腙(H2Dz,二元弱酸)把金属离子络合成电中性的物质[如:Bi3++3H2Dz
 Bi(HDz)3+3H+],再经萃取把金属离子从水溶液中分离出来。设常温时该反应的化学平衡常数为K,则当pH=2时(此时,Bi3+以络合物形式被萃取分离的百分率为40%),废水中c(H2Dz)等于
Bi(HDz)3+3H+],再经萃取把金属离子从水溶液中分离出来。设常温时该反应的化学平衡常数为K,则当pH=2时(此时,Bi3+以络合物形式被萃取分离的百分率为40%),废水中c(H2Dz)等于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知25℃时,五种酸的电离平衡常数如下:
请回答下列问题:
(1)等物质的量浓度的 、
、 、HCOOH、HClO、
、HCOOH、HClO、 溶液中,
溶液中, 的大小顺序为
的大小顺序为_______ (填化学式),浓度分别为 、
、 ,
, 、
、 混合溶液中
混合溶液中
________ 。
(2)写出下列反应的离子方程式。
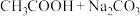 (少量):
(少量):_______________ ;
 (少量):
(少量):_________________ 。
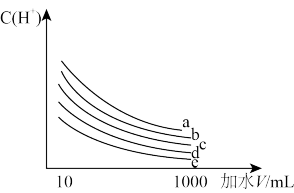
(3)体积均为10mL、浓度均为 的上述五种酸溶液分别加水稀释至1000mL,稀释过程中溶液
的上述五种酸溶液分别加水稀释至1000mL,稀释过程中溶液 的变化如图所示,则曲线b代表
的变化如图所示,则曲线b代表______________ 。
化学式 |
|
| HClO | HCOOH |
|
|
|
|
|
|
|
|
|
|
(1)等物质的量浓度的
 、
、 、HCOOH、HClO、
、HCOOH、HClO、 溶液中,
溶液中, 的大小顺序为
的大小顺序为 、
、 ,
, 、
、 混合溶液中
混合溶液中
(2)写出下列反应的离子方程式。
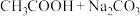 (少量):
(少量): (少量):
(少量):(3)体积均为10mL、浓度均为
 的上述五种酸溶液分别加水稀释至1000mL,稀释过程中溶液
的上述五种酸溶液分别加水稀释至1000mL,稀释过程中溶液 的变化如图所示,则曲线b代表
的变化如图所示,则曲线b代表
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3 → Cu(NO3)2+NO↑+NO2↑+H2O (方程式未配平)
(1)硝酸在该反应中的作用是______ ,该反应的还原产物是______ 。
(2)0.3mol Cu被硝酸完全溶解后,Cu失去的电子数是______ 个,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是______ ,若用排水法收集这些气体,可得标准状况下的气体体积______ 。
(3) 如果参加反应的Cu和HNO3的物质的量之比是3:10,写出并配平该反应的离子方程式______ 。
(4) 如果没有对该反应中的某些物质的比例作限定,则方程式可能的配平系数有许多组。原因是______ 。
(1)硝酸在该反应中的作用是
(2)0.3mol Cu被硝酸完全溶解后,Cu失去的电子数是
(3) 如果参加反应的Cu和HNO3的物质的量之比是3:10,写出并配平该反应的离子方程式
(4) 如果没有对该反应中的某些物质的比例作限定,则方程式可能的配平系数有许多组。原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】过硫酸(H2S2O8)是一种强酸,为无色晶体,易溶于水,在热水中易水解。过硫酸和过硫酸盐在工业上均可用作氧化剂。
(1)根据硫酸和过硫酸的结构式,可判断下列说法正确的是___________ (填标号)。
A.硫酸和过硫酸均为共价化合物
B.过硫酸分子中含有的化学键与过氧化钠的相同
C.过硫酸分子可看作2个硫酸分子脱去1个水分子
D.过硫酸可用于工业漂白、外科消毒等领域
(2)工业上利用过硫酸铵制备过氧化氢的一种方法如图。
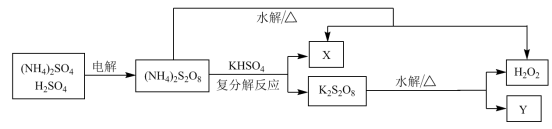
①Y为___________ (填化学式)。
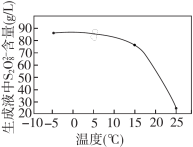
②其他条件一定,电解相同时间后,测得生成液中 的含量随温度变化的关系如图。电解时通常控制温度在15℃,不用更低温度的原因是
的含量随温度变化的关系如图。电解时通常控制温度在15℃,不用更低温度的原因是___________ 。
(3)氮氧化物是大气主要污染物,可采用强氧化剂氧化脱除、热分解等方法处理。

①“反应1”的离子方程式为___________ 。
②“反应2”为 +
+ +2OH-
+2OH-
 +2
+2 +H2O。不同温度下,达到平衡时
+H2O。不同温度下,达到平衡时 的脱除率与过硫酸钠(Na2S2O8)初始浓度的关系如图所示。(NO2的初始浓度相同)
的脱除率与过硫酸钠(Na2S2O8)初始浓度的关系如图所示。(NO2的初始浓度相同)
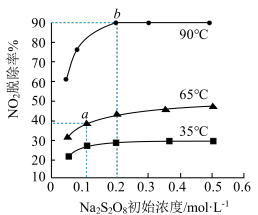
比较a、b点的反应速率: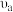
___________ (填“>”“<”或“一”) 。
。
(4)过硫酸钾氧化法可用于分析锰钢中Mn元素的含量:取锰钢样品ag,加入过量浓硝酸,在加热条件下将Mn溶出,再用bL过硫酸钾溶液将溶出的Mn2+全部转化为 ,检测
,检测 浓度,计算得出样品中Mn元素的质量分数为
浓度,计算得出样品中Mn元素的质量分数为 。
。
①该实验条件下氧化性:
___________ (填“>”或“<”) 。
。
②该过程中过硫酸钾溶液的浓度至少是___________ (用含a、b、 的代数式表示)mol·L-1。
的代数式表示)mol·L-1。
| 物质 | 硫酸 | 过硫酸 |
| 结构式 | 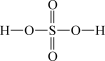 | 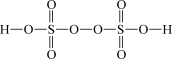 |
A.硫酸和过硫酸均为共价化合物
B.过硫酸分子中含有的化学键与过氧化钠的相同
C.过硫酸分子可看作2个硫酸分子脱去1个水分子
D.过硫酸可用于工业漂白、外科消毒等领域
(2)工业上利用过硫酸铵制备过氧化氢的一种方法如图。

①Y为
②其他条件一定,电解相同时间后,测得生成液中
 的含量随温度变化的关系如图。电解时通常控制温度在15℃,不用更低温度的原因是
的含量随温度变化的关系如图。电解时通常控制温度在15℃,不用更低温度的原因是
(3)氮氧化物是大气主要污染物,可采用强氧化剂氧化脱除、热分解等方法处理。

①“反应1”的离子方程式为
②“反应2”为
 +
+ +2OH-
+2OH-
 +2
+2 +H2O。不同温度下,达到平衡时
+H2O。不同温度下,达到平衡时 的脱除率与过硫酸钠(Na2S2O8)初始浓度的关系如图所示。(NO2的初始浓度相同)
的脱除率与过硫酸钠(Na2S2O8)初始浓度的关系如图所示。(NO2的初始浓度相同)
比较a、b点的反应速率:
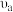
 。
。(4)过硫酸钾氧化法可用于分析锰钢中Mn元素的含量:取锰钢样品ag,加入过量浓硝酸,在加热条件下将Mn溶出,再用bL过硫酸钾溶液将溶出的Mn2+全部转化为
 ,检测
,检测 浓度,计算得出样品中Mn元素的质量分数为
浓度,计算得出样品中Mn元素的质量分数为 。
。①该实验条件下氧化性:

 。
。②该过程中过硫酸钾溶液的浓度至少是
 的代数式表示)mol·L-1。
的代数式表示)mol·L-1。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求完成下列内容
(1)生产硫化钠大多采用无水芒硝(Na2SO4)-碳粉还原法,若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生反应的化学方程式:_______ 。
(2)NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2(已知HCN、HOCN中N元素的化合价相同)则反应的离子方程式:_______ 。
(3)FeO·Cr2O3+Na2CO3+NaNO3 Na2CrO4+Fe2O3+CO2+NaNO2;上述反应配平后FeO·Cr2O3与NaNO3的系数比为
Na2CrO4+Fe2O3+CO2+NaNO2;上述反应配平后FeO·Cr2O3与NaNO3的系数比为_______ 。该步骤不能使用陶瓷容器,原因是_______ 。
(4)将废钒催化剂(主要成分V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应,所得溶液显酸性,含VO2+、K+、SO 等。写出该反应的化学方程式:
等。写出该反应的化学方程式:_______ 。
(1)生产硫化钠大多采用无水芒硝(Na2SO4)-碳粉还原法,若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生反应的化学方程式:
(2)NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2(已知HCN、HOCN中N元素的化合价相同)则反应的离子方程式:
(3)FeO·Cr2O3+Na2CO3+NaNO3
 Na2CrO4+Fe2O3+CO2+NaNO2;上述反应配平后FeO·Cr2O3与NaNO3的系数比为
Na2CrO4+Fe2O3+CO2+NaNO2;上述反应配平后FeO·Cr2O3与NaNO3的系数比为(4)将废钒催化剂(主要成分V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应,所得溶液显酸性,含VO2+、K+、SO
 等。写出该反应的化学方程式:
等。写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】“三酸两碱”是最重要的无机化工产品,广泛用于化学、国防、石油、纺织、冶金、食品等工业。“三酸”是指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。回答下列问题:
(1)浓硝酸不稳定,易分解,需要保存在_____________ 色细口瓶,并用________ 塞盖好,该分解的方程式为_______________________ 。
(2)将红热的木炭,投入热的浓硝酸中,看到的现象是______________________ 。写出该反应的化学方程式______________________________ 。
(3)等物质的量的氯气与二氧化硫通入水中,溶液中存在的主要离子为_______________ ,往反应后溶液中滴入紫色石蕊试液,现象是_______________________________ ,往反应后溶液中BaCl2溶液后的离子方程式为__________________________________ 。
(4)写出氨水与稀盐酸反应的离子方程式___________________________ 。
(1)浓硝酸不稳定,易分解,需要保存在
(2)将红热的木炭,投入热的浓硝酸中,看到的现象是
(3)等物质的量的氯气与二氧化硫通入水中,溶液中存在的主要离子为
(4)写出氨水与稀盐酸反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】强氧化性
①和金属(Cu)反应的实验探究
写出上述反应的化学方程式:______ ;_______ 。
②与Fe、Al反应
常温下浓硝酸可使铁、铝表面形成致密的氧化膜而______ ,保护内部金属不再与酸反应,所以可以用______ 制容器或____ 制容器盛放浓硝酸。加热时,铁、铝可以与浓硝酸反应。
③与非金属反应
写出碳与浓硝酸在加热时反应的化学方程式:______ 。
①和金属(Cu)反应的实验探究
| 实验操作 | 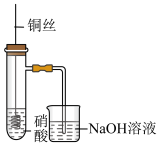 两支试管中分别加入2mL浓硝酸和稀硝酸 |
| 实验现象 | 浓硝酸反应比较 |
| 实验结论 | 硝酸无论浓、稀都有 |
②与Fe、Al反应
常温下浓硝酸可使铁、铝表面形成致密的氧化膜而
③与非金属反应
写出碳与浓硝酸在加热时反应的化学方程式:
您最近一年使用:0次