等物质的量浓度、等体积的下列溶液中(1)H2CO3 (2)Na2CO3 (3)NaHCO3 (4)NH4HCO3 (5)(NH4)2CO3。下列关系或者说法正确的是( )
| A.c(HCO3-)的大小关系为:(4)>(3)>(5)>(2)>(1) |
| B.c(CO32-)的大小关系为:(1)<(4)<(3)<(5)<(2) |
| C.将溶液蒸干后灼烧后只有(1)不能得到对应的固体物质 |
| D.(2)(3)(4)(5)既能与盐酸反应,又能与NaOH溶液反应 |
15-16高三上·河北石家庄·阶段练习 查看更多[12]
第3课时 溶液中粒子浓度的大小比较江西省吉安市2020-2021学年高二上学期期中统考化学试题江西省吉安市省重点中学2020-2021学年高二上学期期中联合考试化学试题河南省鲁山县第一高级中学2019-2020学年高二11月月考化学试题山东省枣庄市第八中学南校区2017-2018学年高二上学期第二次月考(12月)化学试题福建省闽侯第六中学2017-2018学年高二12月月考化学试题2016-2017学年山东省桓台二中高二上学期期中化学试卷2016-2017学年河北省邢台一中高二上月考二化学卷2016-2017学年吉林省长春市第十一高中高二上学期期初考试化学试卷2017届河北省定州中学高三上学期第二次月考化学卷2016届河北省行唐启明中学高三上学期12月月考化学试卷苏教版高三单元精练检测八化学试题
更新时间:2019-11-24 13:10:42
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】对于0.1mol·L-1Na2CO3溶液,下列说法正确的是
| A.升高温度,溶液中c(OH-)增大 |
| B.稀释溶液,溶液中c(H+)减少 |
| C.加入NaOH固体,溶液pH减小 |
D.C(Na+)+c(H+)=C(HCO )+c(CO )+c(CO )+c(OH-) )+c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列说法正确的是
| A.升高NH4Cl溶液的温度,其水的离子积常数和pH均增大 |
| B.在有AgI沉淀的上层清液中滴加一定浓度的NaCl溶液,不可能产生白色沉淀 |
| C.pH=3的盐酸与pH=11的氨水等体积混合后,溶液中:c(NH4+>c(Cl-)>c(OH-)>c(H+) |
D.室温下,稀释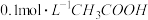 溶液,溶液的导电能力增强 溶液,溶液的导电能力增强 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】已知 是难溶于水、可溶于酸的盐。常温下,用盐酸调节
是难溶于水、可溶于酸的盐。常温下,用盐酸调节 浊液的pH,测得在不同pH条件下,体系中
浊液的pH,测得在不同pH条件下,体系中 与
与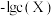 (X为
(X为 或
或 )的关系如图所示。下列说法错误的是
)的关系如图所示。下列说法错误的是
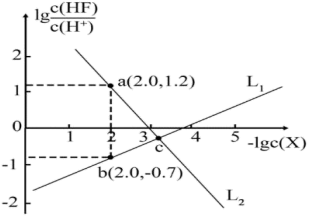
 是难溶于水、可溶于酸的盐。常温下,用盐酸调节
是难溶于水、可溶于酸的盐。常温下,用盐酸调节 浊液的pH,测得在不同pH条件下,体系中
浊液的pH,测得在不同pH条件下,体系中 与
与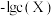 (X为
(X为 或
或 )的关系如图所示。下列说法错误的是
)的关系如图所示。下列说法错误的是
A. 表示 表示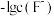 与 与 的变化曲线 的变化曲线 |
B.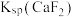 的数量级为 的数量级为 |
C.a、b两点的溶液中均存在: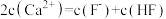 |
D.c点的溶液中: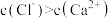 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】常温下, 相等的氨水、氯化铵、硫酸铵、硫酸氢铵四种溶液,溶液浓度最大的是( )
相等的氨水、氯化铵、硫酸铵、硫酸氢铵四种溶液,溶液浓度最大的是( )
 相等的氨水、氯化铵、硫酸铵、硫酸氢铵四种溶液,溶液浓度最大的是( )
相等的氨水、氯化铵、硫酸铵、硫酸氢铵四种溶液,溶液浓度最大的是( )| A.氨水 | B.氯化铵 | C.硫酸铵 | D.硫酸氢铵 |
您最近一年使用:0次

 HCO3-+OH-。下列说法正确的是
HCO3-+OH-。下列说法正确的是 溶液蒸干并灼烧可得到
溶液蒸干并灼烧可得到
 加入大量水中并加热,可得到
加入大量水中并加热,可得到
 溶液,常将
溶液,常将 固体溶于2~3mL蒸馏水会产生SbOCl白色沉淀,则所得溶液显酸性
固体溶于2~3mL蒸馏水会产生SbOCl白色沉淀,则所得溶液显酸性

