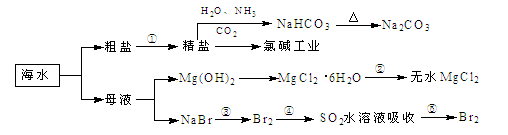
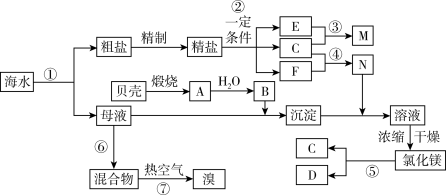
如图是某化工厂对海水资源综合利用的示意图。根据以上信息,判断下列相关分析不正确的是

| A.富集溴元素过程中,热空气吹出法利用了溴易挥发的性质 |
| B.因氮气的化学性质相对稳定,冷却电解无水氯化镁所得的镁蒸气时,可选择氮气 |
| C.反应⑥所用的气态氧化剂可从本厂生产烧碱处理循环利用或从本厂生产镁单质处理循环利用 |
| D.MgCl2·6H2O必须在氯化氢氛围条件下加热制得无水氯化镁 |
18-19高一·浙江·期末 查看更多[1]
(已下线)【新东方】高中化学085
更新时间:2019-11-08 22:31:01
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】硫代硫酸钠晶体( )不溶于乙醇,可用作纸浆漂白时的脱氯剂等。用工业硫化钠(主要成分
)不溶于乙醇,可用作纸浆漂白时的脱氯剂等。用工业硫化钠(主要成分 ,含少量
,含少量 )及纯碱等为原料制备
)及纯碱等为原料制备 的流程如下:
的流程如下:
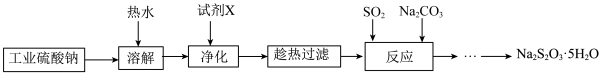
下列说法正确的是
 )不溶于乙醇,可用作纸浆漂白时的脱氯剂等。用工业硫化钠(主要成分
)不溶于乙醇,可用作纸浆漂白时的脱氯剂等。用工业硫化钠(主要成分 ,含少量
,含少量 )及纯碱等为原料制备
)及纯碱等为原料制备 的流程如下:
的流程如下:
下列说法正确的是
A. 作脱氯剂时主要利用其还原性 作脱氯剂时主要利用其还原性 |
| B.“净化”时加入的试剂X可选用CaCl2溶液 |
| C.“反应”过程中体系pH大小对产品产率无影响 |
D.提纯 时,应先用乙醇,再用水洗涤 时,应先用乙醇,再用水洗涤 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】为除去括号内的杂质,所选用的试剂或方法正确的是
| A.Na2SO4溶液(Na2CO3),加入适量的盐酸 |
| B.NaHCO3溶液(Na2CO3),通入过量的CO2气体 |
| C.镁粉(铝),加入足量的盐酸,过滤 |
| D.FeCl2溶液(FeCl3),加入足量的烧碱溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】海洋中有丰富的资源,如图为海水利用的部分过程。下列有关说法正确的是
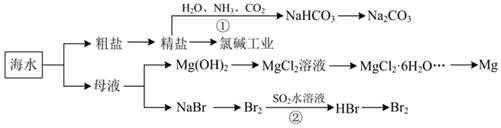

| A.由反应①可知:相同温度下,NaHCO3的溶解度大于Na2CO3 |
| B.通过电解MgCl2溶液可以获得Mg单质 |
C.反应②的离子方程式为:Br2+SO2+2H2O=SO +2Br—+4H+ +2Br—+4H+ |
| D.工业上沉淀Mg2+为Mg(OH)2时常选用NaOH作为沉淀剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】从海带中提取碘有如下步骤:①通入足量的Cl2,②将海带焙烧成灰后加水搅拌,③加CCl4振荡,④用分液漏斗分液,⑤过滤。合理的操作顺序是( )
| A.①②③④⑤ | B.②⑤①③④ | C.①③⑤②④ | D.②①③⑤④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】海水是重要的资源,可以制备一系列物质。下列说法正确的是( )
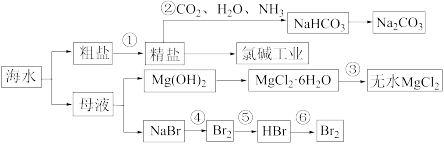

| A.步骤②中,应先通CO2,再通NH3 |
B.第⑤步是向溴水中通SO2,该反应的离子方程式为Br2+SO2+2H2O=2HBr+2H++SO |
| C.步骤④、⑤、⑥反应中,溴元素均被氧化 |
| D.步骤③在HCl气流中加热固体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】由溴化钠溶液制取单质溴可采用的方法是
| A.蒸发结晶,灼烧固体 | B.通入氯气,用汽油萃取 |
| C.通入氯气,用酒精萃取 | D.加入碘水,用四氯化碳萃取 |
您最近一年使用:0次
【推荐3】根据下图海水综合利用的工业流程图,判断下列说法正确的是
已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
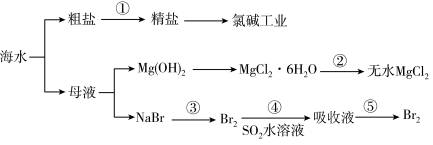
A.除去粗盐中杂质(Mg2+、SO 、Ca2+),加入的药品顺序为: NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 、Ca2+),加入的药品顺序为: NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 |
| B.在过程②中将MgCl2·6H2O灼烧即可制得无水MgCl2 |
| C.从能量转换角度来看,氯碱工业中的电解饱和食盐水是一个将化学能转化为电能的过程 |
| D.过程④与⑤的目的是为了提纯Br2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】工业上60%的镁来自海水,从海水中提取镁工艺流程如图所示,下列说法正确的是( )
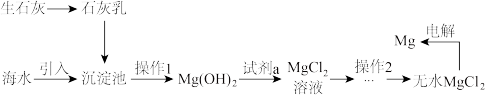
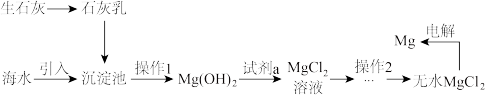
| A.该工艺流程涉及的反应有分解反应、化合反应和置换反应 |
| B.操作1为过滤,实验室里为加快过滤速度应用玻璃棒搅拌液体 |
C.操作2实验室可用装置甲对MgCl2溶液进行蒸发浓缩,再冷却结晶获得无水MgCl2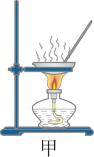 |
| D.该工艺的优点是原料来源广泛,同时获得重要的化工原料 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】从海水的母液中(主要含NaCl和MgSO4)提取金属镁的一种工艺流程如图,下列说法中错误的是
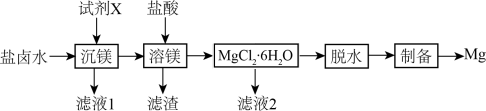

| A.试剂X可以为石灰乳 |
| B.“脱水”时采用直接灼烧的方法,得到MgCl2固体 |
| C.“制备”采取电解熔融MgCl2的方法,Mg在阴极生成 |
| D.“溶镁”的离子方程式为:Mg(OH)2+2H+=Mg2++2H2O |
您最近一年使用:0次

 和
和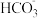
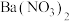 溶液、
溶液、 溶液
溶液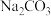 溶液,观察现象
溶液,观察现象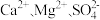
 溶液, 最后加
溶液, 最后加 溶液
溶液