氧化还原反应是一类重要的反应,请按要求完成下列题目。
(1)对反应NH3+O2——NO+H2O(未配平)作分析,该反应中,________ 是还原剂,________ 是还原产物,被还原的物质是________ 。
(2)在一定条件下,反应2NH3+3CuO 3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是
3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是________ 。
①该反应是置换反应
②反应中NH3被氧化为N2
③在反应中体现了金属铜的还原性
④该反应中CuO作为氧化剂参与反应
(3) 配平反应:____ H2S+___ SO2=____ S+____ H2O。
其中,氧化产物为________ ,还原剂为________ ,氧化剂为______ 。
(1)对反应NH3+O2——NO+H2O(未配平)作分析,该反应中,
(2)在一定条件下,反应2NH3+3CuO
 3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是
3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是①该反应是置换反应
②反应中NH3被氧化为N2
③在反应中体现了金属铜的还原性
④该反应中CuO作为氧化剂参与反应
(3) 配平反应:
其中,氧化产物为
更新时间:2019-11-29 16:40:02
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】用双线桥法标出下列反应的电子转移情况和化合价升降情况
Fe+H2SO4=FeSO4+H2↑_____________________________________
Fe+H2SO4=FeSO4+H2↑
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知电子工业上常用FeCl3溶液来溶解电路板中的铜。某一反应体系有反应物和生成物共三种物质:FeCl3、FeCl2、Fe。完成下列问题:
(1)该反应中的还原产物的化学式是____________ ,氧化产物的化学式是____________ 。
(2)该反应中,发生还原反应的过程是(填化学式)_______ →__________ 。
(3)该反应的离子方程式为:_____________________________ 。
(4)标出该反应电子转移的方向和数目______________________________
(5)如反应转移了0.3mol电子,则_______ (填“溶解”或“生成”)的铁的质量为_________ 。
(1)该反应中的还原产物的化学式是
(2)该反应中,发生还原反应的过程是(填化学式)
(3)该反应的离子方程式为:
(4)标出该反应电子转移的方向和数目
(5)如反应转移了0.3mol电子,则
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.纯过氧化氢是淡蓝色的黏稠液体,可与水以任意比混合,水溶液俗称双氧水,为无色透明液体。实验室常用过氧化氢制取氧气,工业上过氧化氢是重要的氧化剂和还原剂,常用于消毒、杀菌、漂白等。某化学兴趣小组的同学围绕过氧化氢开展了调查研究与实验,请你参与其中一起完成下列学习任务:
(1)写出过氧化氢的电子式:____________ 。
(2)实验室中用过氧化氢制取氧气的化学方程式为_______________ ,当生成标准状况下2.24L O2时,转移电子为______ mol。
(3)该兴趣小组的同学查阅资料后发现H2O2为二元弱酸,其酸性比碳酸弱。请写出H2O2在其水溶液中的电离方程式:______ 。(只写第一步)
(4)同学们发现向滴加了酚酞的NaOH溶液中加入H2O2后,溶液中红色消失。关于褪色原因:甲同学认为H2O2是二元弱酸,消耗了OH-使红色消失;乙同学认为H2O2具有漂白性使溶液褪色。请设计一个简单的实验方案来判断甲、乙两位同学的说法是否正确:___________
Ⅱ.工业尾气中含有大量的氮氧化物,NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:
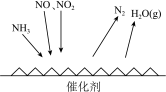
(1)由上图可知SCR技术中的氧化剂为________ 。
(2)用Fe作催化剂加热时,在氨气足量的情况下,当NO2与NO的物质的量之比为1∶1时,写出该反应的化学方程式:________________________________
Ⅲ.研究减少CO2排放是一项重要课题。CO2经催化加氢可以生成低碳有机物,主要有以下反应:
反应①:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1= -49.6 kJ/mol
CH3OH(g)+H2O(g) △H1= -49.6 kJ/mol
反应②:CH3OCH3(g)+H2O(g) 2CH3OH(g) △H2= +23.4 kJ/mol
2CH3OH(g) △H2= +23.4 kJ/mol
反应③:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) △H3=
CH3OCH3(g)+3H2O(g) △H3=___________ kJ/mol。
(1)写出过氧化氢的电子式:
(2)实验室中用过氧化氢制取氧气的化学方程式为
(3)该兴趣小组的同学查阅资料后发现H2O2为二元弱酸,其酸性比碳酸弱。请写出H2O2在其水溶液中的电离方程式:
(4)同学们发现向滴加了酚酞的NaOH溶液中加入H2O2后,溶液中红色消失。关于褪色原因:甲同学认为H2O2是二元弱酸,消耗了OH-使红色消失;乙同学认为H2O2具有漂白性使溶液褪色。请设计一个简单的实验方案来判断甲、乙两位同学的说法是否正确:
Ⅱ.工业尾气中含有大量的氮氧化物,NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:

(1)由上图可知SCR技术中的氧化剂为
(2)用Fe作催化剂加热时,在氨气足量的情况下,当NO2与NO的物质的量之比为1∶1时,写出该反应的化学方程式:
Ⅲ.研究减少CO2排放是一项重要课题。CO2经催化加氢可以生成低碳有机物,主要有以下反应:
反应①:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1= -49.6 kJ/mol
CH3OH(g)+H2O(g) △H1= -49.6 kJ/mol反应②:CH3OCH3(g)+H2O(g)
 2CH3OH(g) △H2= +23.4 kJ/mol
2CH3OH(g) △H2= +23.4 kJ/mol反应③:2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g) △H3=
CH3OCH3(g)+3H2O(g) △H3=
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】I.现有下列物质:
①铁、②硫酸溶液、③ 、④熔融的
、④熔融的 、⑤
、⑤ 固体、⑥蔗糖、⑦
固体、⑥蔗糖、⑦ 晶体、⑧氧气、⑨氨水、⑩稀硝酸。
晶体、⑧氧气、⑨氨水、⑩稀硝酸。
(1)上述物质中属于电解质的有___________ (填编号,下同),属于非电解质的有___________ ,能导电的有___________ 。
(2) 电离方程式为
电离方程式为___________ 。
II.利用氧化还原反应原理可处理污水。
(3)高铁酸钠 是一种新型的净水剂,其中一种制备方法如下:
是一种新型的净水剂,其中一种制备方法如下:
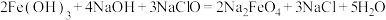 。
。
用单线桥标出该反应电子转移的方向和数目___________ 。
(4)电镀废水中含有剧毒的 (C为
(C为 价),加入
价),加入 溶液处理该碱性废水时生成
溶液处理该碱性废水时生成 、
、 和
和 。该反应的离子方程式为
。该反应的离子方程式为___________ 。
①铁、②硫酸溶液、③
 、④熔融的
、④熔融的 、⑤
、⑤ 固体、⑥蔗糖、⑦
固体、⑥蔗糖、⑦ 晶体、⑧氧气、⑨氨水、⑩稀硝酸。
晶体、⑧氧气、⑨氨水、⑩稀硝酸。(1)上述物质中属于电解质的有
(2)
 电离方程式为
电离方程式为II.利用氧化还原反应原理可处理污水。
(3)高铁酸钠
 是一种新型的净水剂,其中一种制备方法如下:
是一种新型的净水剂,其中一种制备方法如下: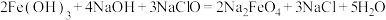 。
。用单线桥标出该反应电子转移的方向和数目
(4)电镀废水中含有剧毒的
 (C为
(C为 价),加入
价),加入 溶液处理该碱性废水时生成
溶液处理该碱性废水时生成 、
、 和
和 。该反应的离子方程式为
。该反应的离子方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】利用Al-CO2电池(工作原理如下图所示)能有效地将CO2转化成化工原料草酸铝。
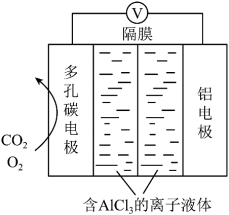
(1)电池的总反应式为_______ 。
(2)电池的正极反应式:2CO2+2e-=C2O (草酸根),正极反应过程中,O2是催化剂,催化过程可表示为:
(草酸根),正极反应过程中,O2是催化剂,催化过程可表示为:
①6O2+6e-=6O
②……
写出反应②的离子方程式:_______ 。

(1)电池的总反应式为
(2)电池的正极反应式:2CO2+2e-=C2O
 (草酸根),正极反应过程中,O2是催化剂,催化过程可表示为:
(草酸根),正极反应过程中,O2是催化剂,催化过程可表示为:①6O2+6e-=6O

②……
写出反应②的离子方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】氮、磷、硫、氯等非金属元素的单质和化合物在工农业生产中有重要应用。回答下列问题:
(1)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为___________ 。某厂废液中含有2%∼5%的 ,直接排放会造成污染,下列物质能使
,直接排放会造成污染,下列物质能使 转化为
转化为 的是
的是___________ (填标号)。
A. B.
B. C.
C.
(2) 及正盐
及正盐 均可将溶液中的
均可将溶液中的 还原为银,从而可用于化学镀银。
还原为银,从而可用于化学镀银。
① 为
为___________ 元酸(填“一”二”或“三”),磷原子的杂化方式为___________ 。
②利用 进行化学镀银,反应中氧化剂与还原剂的物质的量之比为
进行化学镀银,反应中氧化剂与还原剂的物质的量之比为 ,则氧化产物为
,则氧化产物为___________ (填化学式)。
(3)硫代硫酸钠晶体( ),又名大苏打、海波,是一种用途非常广泛的化学试剂,遇酸立即分解,生成淡黄色沉淀,放出的气体能使品红溶液褪色,试写出硫代硫酸钠溶液与稀硫酸反应的离子方程式:
),又名大苏打、海波,是一种用途非常广泛的化学试剂,遇酸立即分解,生成淡黄色沉淀,放出的气体能使品红溶液褪色,试写出硫代硫酸钠溶液与稀硫酸反应的离子方程式:___________ 。
(4)氯气与氢氧化钠在70℃时反应,生成物中 和
和 的物质的量之比为
的物质的量之比为 ,其离子方程式为
,其离子方程式为___________ 。
(1)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为
 ,直接排放会造成污染,下列物质能使
,直接排放会造成污染,下列物质能使 转化为
转化为 的是
的是A.
 B.
B. C.
C.
(2)
 及正盐
及正盐 均可将溶液中的
均可将溶液中的 还原为银,从而可用于化学镀银。
还原为银,从而可用于化学镀银。①
 为
为②利用
 进行化学镀银,反应中氧化剂与还原剂的物质的量之比为
进行化学镀银,反应中氧化剂与还原剂的物质的量之比为 ,则氧化产物为
,则氧化产物为(3)硫代硫酸钠晶体(
 ),又名大苏打、海波,是一种用途非常广泛的化学试剂,遇酸立即分解,生成淡黄色沉淀,放出的气体能使品红溶液褪色,试写出硫代硫酸钠溶液与稀硫酸反应的离子方程式:
),又名大苏打、海波,是一种用途非常广泛的化学试剂,遇酸立即分解,生成淡黄色沉淀,放出的气体能使品红溶液褪色,试写出硫代硫酸钠溶液与稀硫酸反应的离子方程式:(4)氯气与氢氧化钠在70℃时反应,生成物中
 和
和 的物质的量之比为
的物质的量之比为 ,其离子方程式为
,其离子方程式为
您最近半年使用:0次



