氮、磷、硫、氯等非金属元素的单质和化合物在工农业生产中有重要应用。回答下列问题:
(1)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为___________ 。某厂废液中含有2%∼5%的 ,直接排放会造成污染,下列物质能使
,直接排放会造成污染,下列物质能使 转化为
转化为 的是
的是___________ (填标号)。
A. B.
B. C.
C.
(2) 及正盐
及正盐 均可将溶液中的
均可将溶液中的 还原为银,从而可用于化学镀银。
还原为银,从而可用于化学镀银。
① 为
为___________ 元酸(填“一”二”或“三”),磷原子的杂化方式为___________ 。
②利用 进行化学镀银,反应中氧化剂与还原剂的物质的量之比为
进行化学镀银,反应中氧化剂与还原剂的物质的量之比为 ,则氧化产物为
,则氧化产物为___________ (填化学式)。
(3)硫代硫酸钠晶体( ),又名大苏打、海波,是一种用途非常广泛的化学试剂,遇酸立即分解,生成淡黄色沉淀,放出的气体能使品红溶液褪色,试写出硫代硫酸钠溶液与稀硫酸反应的离子方程式:
),又名大苏打、海波,是一种用途非常广泛的化学试剂,遇酸立即分解,生成淡黄色沉淀,放出的气体能使品红溶液褪色,试写出硫代硫酸钠溶液与稀硫酸反应的离子方程式:___________ 。
(4)氯气与氢氧化钠在70℃时反应,生成物中 和
和 的物质的量之比为
的物质的量之比为 ,其离子方程式为
,其离子方程式为___________ 。
(1)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为
 ,直接排放会造成污染,下列物质能使
,直接排放会造成污染,下列物质能使 转化为
转化为 的是
的是A.
 B.
B. C.
C.
(2)
 及正盐
及正盐 均可将溶液中的
均可将溶液中的 还原为银,从而可用于化学镀银。
还原为银,从而可用于化学镀银。①
 为
为②利用
 进行化学镀银,反应中氧化剂与还原剂的物质的量之比为
进行化学镀银,反应中氧化剂与还原剂的物质的量之比为 ,则氧化产物为
,则氧化产物为(3)硫代硫酸钠晶体(
 ),又名大苏打、海波,是一种用途非常广泛的化学试剂,遇酸立即分解,生成淡黄色沉淀,放出的气体能使品红溶液褪色,试写出硫代硫酸钠溶液与稀硫酸反应的离子方程式:
),又名大苏打、海波,是一种用途非常广泛的化学试剂,遇酸立即分解,生成淡黄色沉淀,放出的气体能使品红溶液褪色,试写出硫代硫酸钠溶液与稀硫酸反应的离子方程式:(4)氯气与氢氧化钠在70℃时反应,生成物中
 和
和 的物质的量之比为
的物质的量之比为 ,其离子方程式为
,其离子方程式为
更新时间:2024-03-06 09:39:35
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】用电弧法合成碳纳米管,常伴有大量杂质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为2K2C2O7+3C+8H2SO4=2Cr2(SO4)3+2K2SO4+8H2O+3CO2↑。
(1)用双线桥法表示出电子转移方向和数目___ 。
2K2C2O7+3C+8H2SO4=2Cr2(SO4)3+2K2SO4+8H2O+3CO2↑
(2)此反应的氧化产物和还原产物的物质的量之比为___ 。
(3)要使10mL1.0mol•L-1K2C2O7溶液被还原至少要加入___ mL2.0mol•L-1的H2SO4溶液,消耗C的质量为__ g。
(4)若产生6.72LCO2(标准状况下)气体,该反应转移电子的物质的量为___ mol。
(5)H2SO4在上述反应中表现出来的性质是___ 。
A.酸性B.氧化性C.吸水性
(1)用双线桥法表示出电子转移方向和数目
2K2C2O7+3C+8H2SO4=2Cr2(SO4)3+2K2SO4+8H2O+3CO2↑
(2)此反应的氧化产物和还原产物的物质的量之比为
(3)要使10mL1.0mol•L-1K2C2O7溶液被还原至少要加入
(4)若产生6.72LCO2(标准状况下)气体,该反应转移电子的物质的量为
(5)H2SO4在上述反应中表现出来的性质是
A.酸性B.氧化性C.吸水性
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】突如其来的新冠肺炎使人们认识到日常杀菌消毒的重要性。氯气、“84”消毒液、漂白粉都是生活中常用的含氯消毒剂,回答下列问题:
(1)工业生产漂白粉的化学方程式为___________ 。
(2)取一滴“84”消毒液滴在pH试纸上,可观察到先变蓝后褪色的现象,证明“84”消毒液具有___________ 性和___________ 性。
(3)日常生活中“84”消毒液若与洁厕灵(含盐酸)混用,发生反应:NaClO+2HCl=NaCl+Cl2↑+H2O,该反应的氧化剂为_________ ,若反应中转移1.5mol电子,则生成的氯气在标准状况下体积为_________ L。
(4)“84”消毒液需要避光密封保存,否则容易变质而失效,用化学方程式解释其原因:①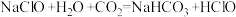 ;②
;②___________ 。
(1)工业生产漂白粉的化学方程式为
(2)取一滴“84”消毒液滴在pH试纸上,可观察到先变蓝后褪色的现象,证明“84”消毒液具有
(3)日常生活中“84”消毒液若与洁厕灵(含盐酸)混用,发生反应:NaClO+2HCl=NaCl+Cl2↑+H2O,该反应的氧化剂为
(4)“84”消毒液需要避光密封保存,否则容易变质而失效,用化学方程式解释其原因:①
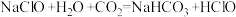 ;②
;②
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】水体中的六价铬[Cr(Ⅵ)]对生态环境和人体健康威胁很大。工业废水中[Cr(Ⅵ)]常用还原沉淀法、微生物法等进行处理。
(1)“还原沉淀法”常用Na2SO3、FeSO4等处理Cr(Ⅵ)得到Cr(Ⅲ)。已知溶液中含Cr(Ⅵ)的微粒(H2CrO4、Cr2O 和CrO
和CrO )的物质的量分数随pH的关系如图所示。
)的物质的量分数随pH的关系如图所示。
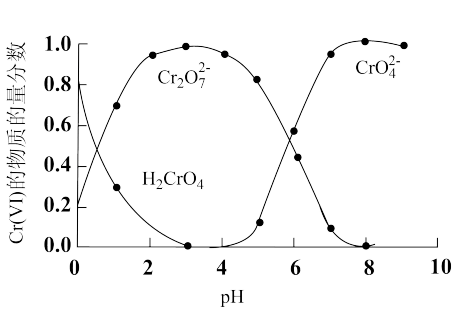
①某含Cr(Ⅵ)废水的pH约为8,写出用Na2SO3处理该废水的主要离子方程式:_______ 。[已知pH=3时,Cr(Ⅲ)以Cr3+形式存在,pH=7.5时,Cr(Ⅲ)开始沉淀]。
②其他条件相同,用Na2SO3处理不同pH含Cr(Ⅵ)的废水,反应相同时间,Cr(Ⅵ)的去除率与pH的关系如图所示。已知酸性条件下Cr(Ⅵ)对Na2SO3具有很强的氧化能力,pH<2时,Cr(Ⅵ)的去除率随pH降低而降低的原因是_______ 。
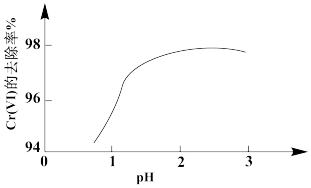
③研究发现,用FeSO4处理pH=3的含Cr(Ⅵ)废水,Cr(Ⅵ)的去除率大于其被FeSO4还原的理论值。Cr(Ⅵ)的去除率大于理论值的原因是_______ 。
(2)“微生物法”处理含Cr(Ⅵ)废水具有效率高、选择性强、吸附容量大等优点。一种微生物法是用硫酸盐还原菌(SRB)处理含Cr(Ⅵ)废水。
①硫酸盐还原菌能将水中的SO 转化为S2-,S2-与CrO
转化为S2-,S2-与CrO 可反应生成Cr2S3和S两种沉淀。写出S2-与CrO
可反应生成Cr2S3和S两种沉淀。写出S2-与CrO 反应的离子方程式:
反应的离子方程式:_______ 。
②用硫酸盐还原菌(SRB)处理含铬废水时,温度常控制在30℃左右,温度过高,Cr(Ⅵ)的去除率低的原因是_______ 。
③硫酸盐还原菌(SRB)常存在于水体中,会腐蚀许多金属及合金。一种Fe合金在硫酸盐还原菌存在条件下腐蚀的机理如图所示。已知溶液中的S2-会完全转化为FeS,则Fe腐蚀后生成Fe(OH)2和FeS的物质的量之比为_______ 。

(1)“还原沉淀法”常用Na2SO3、FeSO4等处理Cr(Ⅵ)得到Cr(Ⅲ)。已知溶液中含Cr(Ⅵ)的微粒(H2CrO4、Cr2O
 和CrO
和CrO )的物质的量分数随pH的关系如图所示。
)的物质的量分数随pH的关系如图所示。
①某含Cr(Ⅵ)废水的pH约为8,写出用Na2SO3处理该废水的主要离子方程式:
②其他条件相同,用Na2SO3处理不同pH含Cr(Ⅵ)的废水,反应相同时间,Cr(Ⅵ)的去除率与pH的关系如图所示。已知酸性条件下Cr(Ⅵ)对Na2SO3具有很强的氧化能力,pH<2时,Cr(Ⅵ)的去除率随pH降低而降低的原因是

③研究发现,用FeSO4处理pH=3的含Cr(Ⅵ)废水,Cr(Ⅵ)的去除率大于其被FeSO4还原的理论值。Cr(Ⅵ)的去除率大于理论值的原因是
(2)“微生物法”处理含Cr(Ⅵ)废水具有效率高、选择性强、吸附容量大等优点。一种微生物法是用硫酸盐还原菌(SRB)处理含Cr(Ⅵ)废水。
①硫酸盐还原菌能将水中的SO
 转化为S2-,S2-与CrO
转化为S2-,S2-与CrO 可反应生成Cr2S3和S两种沉淀。写出S2-与CrO
可反应生成Cr2S3和S两种沉淀。写出S2-与CrO 反应的离子方程式:
反应的离子方程式:②用硫酸盐还原菌(SRB)处理含铬废水时,温度常控制在30℃左右,温度过高,Cr(Ⅵ)的去除率低的原因是
③硫酸盐还原菌(SRB)常存在于水体中,会腐蚀许多金属及合金。一种Fe合金在硫酸盐还原菌存在条件下腐蚀的机理如图所示。已知溶液中的S2-会完全转化为FeS,则Fe腐蚀后生成Fe(OH)2和FeS的物质的量之比为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】磷元素能形成多种含氧酸。回答下列问题:
(1)次磷酸(H3PO2)是一元弱酸,其在水溶液中的电离方程式为__ 。
(2)亚磷酸(H3PO3)是二元弱酸。已知25℃时,Ka1=1×10-2,Ka2=2.6×10-7.
①Na2HPO3属于__ (填“酸式盐”或“正盐”);NaH2PO3溶液显__ (填“酸性”“碱性”或“中性”)。
②已知25℃时,CH3COOH的Ka=1.75×10-5,则CH3COOH溶液和Na2HPO3溶液反应的化学方程式为__ 。
(3)测定亚磷酸溶液的浓度。
取25.00mL亚磷酸溶液放入锥形瓶中,用0.10mol·L-1酸性高锰酸钾溶液进行滴定,反应的离子方程式为__ 。
(1)次磷酸(H3PO2)是一元弱酸,其在水溶液中的电离方程式为
(2)亚磷酸(H3PO3)是二元弱酸。已知25℃时,Ka1=1×10-2,Ka2=2.6×10-7.
①Na2HPO3属于
②已知25℃时,CH3COOH的Ka=1.75×10-5,则CH3COOH溶液和Na2HPO3溶液反应的化学方程式为
(3)测定亚磷酸溶液的浓度。
取25.00mL亚磷酸溶液放入锥形瓶中,用0.10mol·L-1酸性高锰酸钾溶液进行滴定,反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列填空
(1)某Fe2(SO4)3样品含有少量FeSO4杂质,将其配成溶液。
①若要检验溶液中的Fe3+,可加入___________ 试剂(填化学式),观察溶液呈血红色。
②若要检验溶液中的Fe2+,下列方法可行的是:___________ 。
A.取少量溶液于试管中,滴入几滴酸性高锰酸钾溶液,若紫红色褪去,则含有Fe2+
B.取少量溶液于试管中,加入新制氯水,再滴入硫氰化钾,若呈血红色,则含有Fe2+
C.取少量溶液于试管中,滴入NaOH溶液,看到白色沉淀迅速变为灰绿再变为红褐色,则含有Fe2+
(2)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,某学习小组设计如图方案制备高铁酸钾:
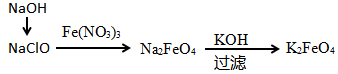
①高铁酸钾中铁元素的化合价为___________ ,据此推测它具有的化学性质是___________ 。
②其中第一步操作是:在NaClO溶液中加入烧碱固体形成强碱性环境,将研磨过的硝酸铁少量多次地加入上述溶液中,温度保持0℃反应1h,则采用的合适控温方式是___________ 。发生的离子反应为:___________ 。
③高铁酸钾和水发生反应,生成一种胶体能吸附杂质净水,同时还产生气体,写出反应的离子方程式:___________ 。
(1)某Fe2(SO4)3样品含有少量FeSO4杂质,将其配成溶液。
①若要检验溶液中的Fe3+,可加入
②若要检验溶液中的Fe2+,下列方法可行的是:
A.取少量溶液于试管中,滴入几滴酸性高锰酸钾溶液,若紫红色褪去,则含有Fe2+
B.取少量溶液于试管中,加入新制氯水,再滴入硫氰化钾,若呈血红色,则含有Fe2+
C.取少量溶液于试管中,滴入NaOH溶液,看到白色沉淀迅速变为灰绿再变为红褐色,则含有Fe2+
(2)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,某学习小组设计如图方案制备高铁酸钾:
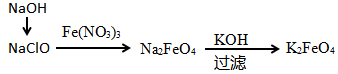
①高铁酸钾中铁元素的化合价为
②其中第一步操作是:在NaClO溶液中加入烧碱固体形成强碱性环境,将研磨过的硝酸铁少量多次地加入上述溶液中,温度保持0℃反应1h,则采用的合适控温方式是
③高铁酸钾和水发生反应,生成一种胶体能吸附杂质净水,同时还产生气体,写出反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】高铁酸盐(K2FeO4)在能源、环保等方面有着广泛的用途.湿法、干法制备高铁酸盐的原理如下表所示.
(1)写出干法制备K2FeO4的化学方程式为,_____________________________________ ,该
反应中氧化剂与还原剂的物质的量之比为_______________________________ 。
(2)高铁酸钾在水中既能消毒杀菌,又能净水,是一种理想的水处理剂.它能消毒杀菌是因为_______________________________ ,它能净水的原因是_____________________________________ 。
(3)在实验室配制Fe(NO3)3溶液时,若用蒸馏水直接配制,所得溶液往往较浑浊,其原因是(用离子方程式表示)____________________________ ,因此,正确的配制操作是在溶液中加入少量的(填试剂名称)_____________ ,其目的是__________________________ 。
(4)Fe2O3是一种____________ 色的氧化物,写出它和盐酸反应的离子方程式___________ 。
(5)检验Fe3+的方法很多,写出其中的一种检验方法_______________________________ 。
| 湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
反应中氧化剂与还原剂的物质的量之比为
(2)高铁酸钾在水中既能消毒杀菌,又能净水,是一种理想的水处理剂.它能消毒杀菌是因为
(3)在实验室配制Fe(NO3)3溶液时,若用蒸馏水直接配制,所得溶液往往较浑浊,其原因是(用离子方程式表示)
(4)Fe2O3是一种
(5)检验Fe3+的方法很多,写出其中的一种检验方法
您最近一年使用:0次
【推荐1】CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。
已知:①CuCl可以由CuCl2用适当的还原剂如SO2,SnCl2等还原制得:
2Cu2++2Cl-+SO2+2H2O 2CuCl↓+4H++SO42-
2CuCl↓+4H++SO42-
2CuCl2+SnCl2=2CuCl↓+SnCl4
②CuCl2溶液与乙二胺(H2N—CH2—CH2—NH2)可形成配离子:

请回答下列问题:
(1)基态Cu原子的核外电子排布式为_________ ;H、N、O三种元素的电负性由大到小的顺序是_____________
(2)SO2分子的空间构型为_____________
(3)乙二胺分子中氮原子轨道的杂化类型为_________ 乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是_____________
(4)②中所形成的配离子中含有的化学键类型有______ (填字母)。
A.配位键 B.极性键 C.离子键 D.非极性键
已知:①CuCl可以由CuCl2用适当的还原剂如SO2,SnCl2等还原制得:
2Cu2++2Cl-+SO2+2H2O
 2CuCl↓+4H++SO42-
2CuCl↓+4H++SO42-2CuCl2+SnCl2=2CuCl↓+SnCl4
②CuCl2溶液与乙二胺(H2N—CH2—CH2—NH2)可形成配离子:

请回答下列问题:
(1)基态Cu原子的核外电子排布式为
(2)SO2分子的空间构型为
(3)乙二胺分子中氮原子轨道的杂化类型为
(4)②中所形成的配离子中含有的化学键类型有
A.配位键 B.极性键 C.离子键 D.非极性键
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】硼及其化合物在新材料、工农业生产等方面用途很广。请回答下列问题:
 元素的基态原子的价电子排布图为
元素的基态原子的价电子排布图为______ ,B、N、O元素的第一电离能由大到小的顺序为______ 。
 三氟化硼在常温常压下为具有刺鼻恶臭和强刺激性气味的无色有毒腐蚀性气体,其分子的立体构型为
三氟化硼在常温常压下为具有刺鼻恶臭和强刺激性气味的无色有毒腐蚀性气体,其分子的立体构型为______ ,B原子的杂化类型为______ 。
 自然界中,含B的钠盐是一种天然矿藏,其化学式写作
自然界中,含B的钠盐是一种天然矿藏,其化学式写作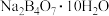 ,实际上它的阴离子结构单元是由两个
,实际上它的阴离子结构单元是由两个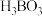 和两个
和两个 缩合而成的双六元环,应该写成
缩合而成的双六元环,应该写成 ,其结构式如图1,它的阴离子可形成链状结构。该阴离子由极性键和配位键构成,请在答题卷中抄上图1结构式后用“
,其结构式如图1,它的阴离子可形成链状结构。该阴离子由极性键和配位键构成,请在答题卷中抄上图1结构式后用“ ”标出其中的配位键,该阴离子通过
”标出其中的配位键,该阴离子通过______ 相互结合形成链状结构。

 科学家发现硼化镁在39K时有超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列。图2是该晶体微观结构中取出的部分原子沿z轴方向的投影,白球是镁原子投影,黑球是硼原子投影。则硼化镁的化学式为
科学家发现硼化镁在39K时有超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列。图2是该晶体微观结构中取出的部分原子沿z轴方向的投影,白球是镁原子投影,黑球是硼原子投影。则硼化镁的化学式为______ 。
 磷化硼
磷化硼 是一种有价值的超硬耐磨涂层材料,这种陶瓷材料可作为金属表面的保护薄膜。磷化硼晶胞如图3所示,在BP晶胞中B的堆积方式为
是一种有价值的超硬耐磨涂层材料,这种陶瓷材料可作为金属表面的保护薄膜。磷化硼晶胞如图3所示,在BP晶胞中B的堆积方式为______ ,当晶胞晶格参数为478pm时,磷化硼中硼原子和磷原子之间的最近距离为______ cm。
 元素的基态原子的价电子排布图为
元素的基态原子的价电子排布图为 三氟化硼在常温常压下为具有刺鼻恶臭和强刺激性气味的无色有毒腐蚀性气体,其分子的立体构型为
三氟化硼在常温常压下为具有刺鼻恶臭和强刺激性气味的无色有毒腐蚀性气体,其分子的立体构型为 自然界中,含B的钠盐是一种天然矿藏,其化学式写作
自然界中,含B的钠盐是一种天然矿藏,其化学式写作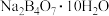 ,实际上它的阴离子结构单元是由两个
,实际上它的阴离子结构单元是由两个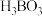 和两个
和两个 缩合而成的双六元环,应该写成
缩合而成的双六元环,应该写成 ,其结构式如图1,它的阴离子可形成链状结构。该阴离子由极性键和配位键构成,请在答题卷中抄上图1结构式后用“
,其结构式如图1,它的阴离子可形成链状结构。该阴离子由极性键和配位键构成,请在答题卷中抄上图1结构式后用“ ”标出其中的配位键,该阴离子通过
”标出其中的配位键,该阴离子通过
 科学家发现硼化镁在39K时有超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列。图2是该晶体微观结构中取出的部分原子沿z轴方向的投影,白球是镁原子投影,黑球是硼原子投影。则硼化镁的化学式为
科学家发现硼化镁在39K时有超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列。图2是该晶体微观结构中取出的部分原子沿z轴方向的投影,白球是镁原子投影,黑球是硼原子投影。则硼化镁的化学式为 磷化硼
磷化硼 是一种有价值的超硬耐磨涂层材料,这种陶瓷材料可作为金属表面的保护薄膜。磷化硼晶胞如图3所示,在BP晶胞中B的堆积方式为
是一种有价值的超硬耐磨涂层材料,这种陶瓷材料可作为金属表面的保护薄膜。磷化硼晶胞如图3所示,在BP晶胞中B的堆积方式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
(1)氟原子在不同状态下的电子排布式有以下几种,其中处于激发态且能量较高的是___________ 。(填标号)
a. b.
b. c.
c. d.
d.
(2)①一氯乙烯(C2H3Cl)分子中,C的一个___________ 杂化轨道与Cl的3px轨道形成C-Cl___________ 键,并且Cl的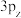 轨道与C的
轨道与C的 轨道形成3中心4电子的大π键
轨道形成3中心4电子的大π键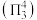 。
。
②一氯乙烷(C2H5Cl)、一氯乙烯(C2H3Cl)、一氯乙炔(C2HCl)分子中,C-Cl键长的顺序是___________ ,理由:(ⅰ)C的杂化轨道中s成分越多,形成的C-Cl键越强;(ⅱ)___________ 。
(1)氟原子在不同状态下的电子排布式有以下几种,其中处于激发态且能量较高的是
a.
 b.
b. c.
c. d.
d.
(2)①一氯乙烯(C2H3Cl)分子中,C的一个
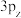 轨道与C的
轨道与C的 轨道形成3中心4电子的大π键
轨道形成3中心4电子的大π键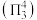 。
。②一氯乙烷(C2H5Cl)、一氯乙烯(C2H3Cl)、一氯乙炔(C2HCl)分子中,C-Cl键长的顺序是
您最近一年使用:0次



