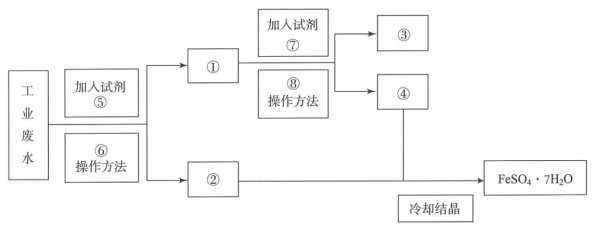
实验室需纯净的NaCl晶体,但现有的NaCl晶体中混有少量的Na2SO4和NH4HCO3,为除去杂质,甲同学设计了如下实验:(已知NH4HCO3 NH3↑+H2O+CO2↑)
NH3↑+H2O+CO2↑)
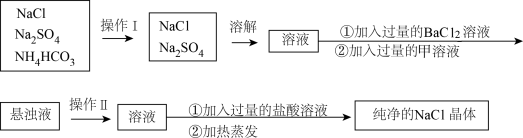
(1)上述操作I、Ⅱ的名称分别为______ 、_______
(2)进行操作“加入过量的BaCl2溶液”时,如何判断BaCl2溶液已过量,其方法是______________________________________________________
(3)操作“加入过量的甲溶液”,甲溶液为______ 溶液,此操作的目的是________________________ 。
(4)操作“加入过量的盐酸溶液”的目的是________________________ 。
 NH3↑+H2O+CO2↑)
NH3↑+H2O+CO2↑)
(1)上述操作I、Ⅱ的名称分别为
(2)进行操作“加入过量的BaCl2溶液”时,如何判断BaCl2溶液已过量,其方法是
(3)操作“加入过量的甲溶液”,甲溶液为
(4)操作“加入过量的盐酸溶液”的目的是
更新时间:2019-11-26 12:54:43
|
相似题推荐
解答题-工业流程题
|
容易
(0.94)
名校
【推荐1】现有含少量NaCl、Na2SO4、Na2CO3杂质的NaNO3溶液,选择适当的试剂除去杂质,得到纯净的NaNO3固体,实验流程如下图所示。
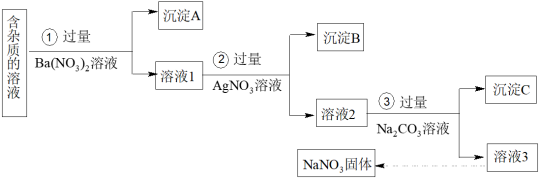
(1)沉淀A的成分是_______ (填化学式)。
(2)②中反应的离子方程式是_______ 。
(3)溶液3中肯定含有的杂质离子是_______ ,为除去杂质可向溶液3中加入适量的_______ 。

(1)沉淀A的成分是
(2)②中反应的离子方程式是
(3)溶液3中肯定含有的杂质离子是
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
【推荐2】为除去粗盐中的Ca2+、Mg2+、SO 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:(用于沉淀的试剂稍过量)
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:(用于沉淀的试剂稍过量)

(1)第⑤步中,操作B是___________ 。
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2)___________ 。
(3)判断BaCl2已过量的方法是________ 。
(4)下列是某学生设计操作A后混合液中Cl-、SO 的检验步骤请根据内容填空:
的检验步骤请根据内容填空:
①首先检验___ 离子, 需要的试剂是____________ 。
②将所得混合物___ (填操作名称) ,然后在溶液中加入试剂______ 检验另一离子。
 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:(用于沉淀的试剂稍过量)
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:(用于沉淀的试剂稍过量)
(1)第⑤步中,操作B是
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2)
(3)判断BaCl2已过量的方法是
(4)下列是某学生设计操作A后混合液中Cl-、SO
 的检验步骤请根据内容填空:
的检验步骤请根据内容填空:①首先检验
②将所得混合物
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
解题方法
【推荐3】为除去粗盐中的Mg2+、Ca2+、SO 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图:
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图:
粗盐



 滤液
滤液
 精盐
精盐
已知可选择的试剂有:BaCl2溶液、Ba(NO3)2溶液、Na2CO3溶液、K2CO3溶液、盐酸、NaOH溶液。
请回答下列问题:
(1)检验粗盐中是否含有SO 的方法是:取少量溶解后的澄清粗盐水于试管中,先加足量的
的方法是:取少量溶解后的澄清粗盐水于试管中,先加足量的____ (填试剂名称),然后再加几滴___ (填试剂名称)。
(2)加入“试剂2”发生反应的离子方程式为___ 。
(3)过滤时,所需玻璃仪器有___ 。过滤后,滤渣要用蒸馏水洗涤2~3次,并将洗涤液转入到滤液中,这样做的目的为___ 。
(4)加盐酸时发生反应的离子方程式为___ ,判断盐酸适量的现象为___ 。
 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图:
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图:粗盐




 滤液
滤液
 精盐
精盐已知可选择的试剂有:BaCl2溶液、Ba(NO3)2溶液、Na2CO3溶液、K2CO3溶液、盐酸、NaOH溶液。
请回答下列问题:
(1)检验粗盐中是否含有SO
 的方法是:取少量溶解后的澄清粗盐水于试管中,先加足量的
的方法是:取少量溶解后的澄清粗盐水于试管中,先加足量的(2)加入“试剂2”发生反应的离子方程式为
(3)过滤时,所需玻璃仪器有
(4)加盐酸时发生反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
容易
(0.94)
解题方法
【推荐1】某工厂生产废液中含有大量的( 、
、 、
、 、
、 某兴趣小组设计了以下方案,对废液加以综合利用获得了Cu和绿矾。
某兴趣小组设计了以下方案,对废液加以综合利用获得了Cu和绿矾。

请回答以下问题:
(1)废液中加过量铁时发生反应的离子方程式为_______ 、_______ ;
(2)合并溶液1和溶液2后,系列操作3包含_______ 、_______ 、过滤等操作;
(3)若使用得到的绿矾晶体制备净水剂溶液,除在绿矾中加入适量稀硫酸外,还需要加入_______ (填标号)。
①稀 ②
② ③
③ ④Fe粉
④Fe粉
 、
、 、
、 、
、 某兴趣小组设计了以下方案,对废液加以综合利用获得了Cu和绿矾。
某兴趣小组设计了以下方案,对废液加以综合利用获得了Cu和绿矾。
请回答以下问题:
(1)废液中加过量铁时发生反应的离子方程式为
(2)合并溶液1和溶液2后,系列操作3包含
(3)若使用得到的绿矾晶体制备净水剂溶液,除在绿矾中加入适量稀硫酸外,还需要加入
①稀
 ②
② ③
③ ④Fe粉
④Fe粉
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
解题方法
【推荐2】某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性和强挥发性。他们参观生产过程后,绘制了如图装置简图。
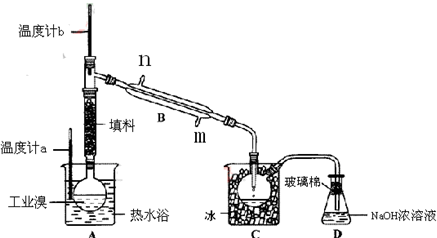
请你参与分析讨论:
(1)图中仪器B的名称:_____ ,冷却水从_____ 进,_____ 出。
(2)烧杯A的作用_____________ ,C中冰的作用是_____ 。

请你参与分析讨论:
(1)图中仪器B的名称:
(2)烧杯A的作用
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
【推荐1】实验室中用浓盐酸与MnO2制取Cl2,再用Cl2和Ca(OH)2反应制少量漂白粉。已知Cl2和Ca(OH)2制漂白粉是放热反应,温度稍高易发生副反应:
6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2O。现有三位同学分别设计的三套实验装置如下(U形管中放有玻璃纤维,气体能顺利通过):
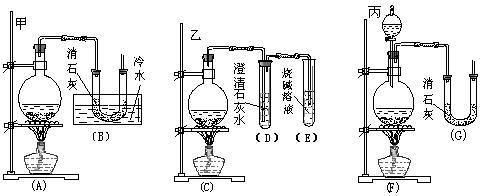
(1)请从以下六方面对上述甲、乙、丙三套装置的优缺点进行评价,将适当的选项序号填于下表内:
a.不易控制反应速率 b.容易控制反应速率 c.有副反应发生
d.可防止副反应发生 e.容易污染环境 f.可防止污染环境
(2)请从甲、乙、丙三套装置中,选取合理的组成部分(A、B、C、D、E、F、G),组装一套你认为更完善的实验装置,连接顺序(按气流从左到右的方向)为___________ ;在此装置及甲、乙、丙三装置中,你认为是否还缺少必要的装置,并说明原因_________________________________________________________________________________________________________________________________________ 。
(3)如果反应前加入了mg Ca(OH)2,反应结束并冷却后倒出固体物质称量为ng(设反应中产生的水仍留在固体物质中)。则该固体物质中Ca(ClO)2的质量分数的表达式为(不必化简):__________________________________________________ 。
6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2O。现有三位同学分别设计的三套实验装置如下(U形管中放有玻璃纤维,气体能顺利通过):

(1)请从以下六方面对上述甲、乙、丙三套装置的优缺点进行评价,将适当的选项序号填于下表内:
a.不易控制反应速率 b.容易控制反应速率 c.有副反应发生
d.可防止副反应发生 e.容易污染环境 f.可防止污染环境
| 优点 | 缺点 | |
| 甲装置 | ||
| 乙装置 | ||
| 丙装置 |
(3)如果反应前加入了mg Ca(OH)2,反应结束并冷却后倒出固体物质称量为ng(设反应中产生的水仍留在固体物质中)。则该固体物质中Ca(ClO)2的质量分数的表达式为(不必化简):
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
【推荐2】碘化钠可用作甲状腺肿瘤防治剂、祛痰剂和利尿剂等,实验室用NaOH、单质碘和水合肼(N2H4·H2O)为原料制备碘化钠。已知:水合肼易被空气氧化。回答下列问题:
(1)水合肼的制备
①制取次氯酸钠和氢氧化钠的混合液。盛装氢氧化钠溶液的仪器名称是__ ,正确的连接顺序为__ (按气流方向,用小写字母表示)。
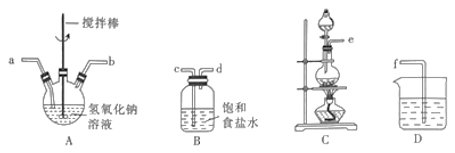
②将尿素滴入次氯酸钠和氢氧化钠的混合液中,发生反应CO(NH2)2+NaClO+2NaOH=N2H4·H2O+NaCl+Na2CO3,反应中作氧化剂的是__ [填“NaClO”或“CO(NH2)2”]。
(2)碘化钠的制备
I.向锥形瓶中加入40mL6mol·L-1NaOH溶液,搅拌、冷却,加入25.4g单质碘,打开恒温磁力搅拌器,保持60~70℃至反应完全;
II.继续加入稍过量的N2H4·H2O,还原生成的NaIO和NaIO3,得到NaI溶液,同时释放出一种空气中主要成分的气体;
III.将溶液蒸发浓缩、冷却结晶过滤、洗涤、干燥,得产品25.5g。
①步骤I反应完全的现象是__ 。
②步骤II中IO-参与反应的离子方程式为__ 。
③实验发现,水合肼实际用量比理论值偏高,可能的原因是__ 。
④测定产品中NaI含量的实验步骤如下:
a.称取10.00g产品并溶解,在500mL容量瓶中定容;
b.量取25.00mL待测液于锥形瓶中,然后加入足量FeCl3溶液,充分反应后,再加入M溶液作指示剂;
c.用0.2100mol·L-1的Na2S2O3标准溶液滴定至终点(化学方程式为2Na2S2O3+I2=Na2S4O6+2NaI),重复实验多次.测得平均消耗Na2S2O3标准溶液的体积为15.00mL。则M为__ (写名称);该产品中NI的质量分数为__ 。
⑤工业上也可用硫化钠或铁屑还原碘酸钠来制备碘化钠,但水合肼还原法制得的产品纯度更高,其原因__ 。
(1)水合肼的制备
①制取次氯酸钠和氢氧化钠的混合液。盛装氢氧化钠溶液的仪器名称是

②将尿素滴入次氯酸钠和氢氧化钠的混合液中,发生反应CO(NH2)2+NaClO+2NaOH=N2H4·H2O+NaCl+Na2CO3,反应中作氧化剂的是
(2)碘化钠的制备
I.向锥形瓶中加入40mL6mol·L-1NaOH溶液,搅拌、冷却,加入25.4g单质碘,打开恒温磁力搅拌器,保持60~70℃至反应完全;
II.继续加入稍过量的N2H4·H2O,还原生成的NaIO和NaIO3,得到NaI溶液,同时释放出一种空气中主要成分的气体;
III.将溶液蒸发浓缩、冷却结晶过滤、洗涤、干燥,得产品25.5g。
①步骤I反应完全的现象是
②步骤II中IO-参与反应的离子方程式为
③实验发现,水合肼实际用量比理论值偏高,可能的原因是
④测定产品中NaI含量的实验步骤如下:
a.称取10.00g产品并溶解,在500mL容量瓶中定容;
b.量取25.00mL待测液于锥形瓶中,然后加入足量FeCl3溶液,充分反应后,再加入M溶液作指示剂;
c.用0.2100mol·L-1的Na2S2O3标准溶液滴定至终点(化学方程式为2Na2S2O3+I2=Na2S4O6+2NaI),重复实验多次.测得平均消耗Na2S2O3标准溶液的体积为15.00mL。则M为
⑤工业上也可用硫化钠或铁屑还原碘酸钠来制备碘化钠,但水合肼还原法制得的产品纯度更高,其原因
您最近一年使用:0次
解答题-工业流程题
|
容易
(0.94)
【推荐3】为了从海带中制取碘,某学习小组将海带灼烧后,加水溶解配成海带浸取原液(浸取原液中的碘元素主要以I-形式存在),并设计了如下甲、乙两种实验方案:
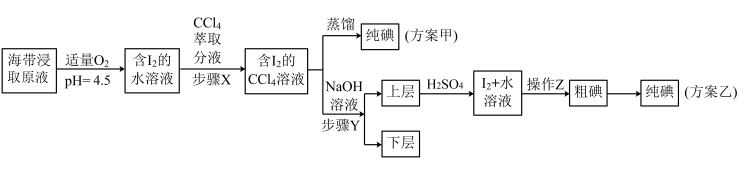
已知:①步骤Y中加NaOH时发生反应:3I2+6NaOH=5NaI+NaIO3+3H2O;
②碘单质常温为紫黑色固体,在通常状况下,100g水中约溶解0.02g碘单质。
请回答:
(1)灼烧海带应该在___________ (填仪器名称)中进行。
(2)分液漏斗使用前须先___________ ;步骤X中,萃取后分液漏斗内观察到的现象是___________ 。
(3)步骤Y中需要控制加入的NaOH溶液的量不宜过多,原因是___________ 。
(4)操作Z的名称是___________ 。
(5)方案甲中采用蒸馏不合理,理由是___________ 。

已知:①步骤Y中加NaOH时发生反应:3I2+6NaOH=5NaI+NaIO3+3H2O;
②碘单质常温为紫黑色固体,在通常状况下,100g水中约溶解0.02g碘单质。
请回答:
(1)灼烧海带应该在
(2)分液漏斗使用前须先
(3)步骤Y中需要控制加入的NaOH溶液的量不宜过多,原因是
(4)操作Z的名称是
(5)方案甲中采用蒸馏不合理,理由是
您最近一年使用:0次