某混合物浆液含有Al(OH)3、MnO2和少量Na2CrO4.考虑到胶体的吸附作用使Na2CrO4不易完全被水浸出,某研究小组利用设计的电解分离装置(见图),使浆液分离成固体混合物和含铬元素溶液,并回收利用。回答Ⅰ和Ⅱ中的问题。

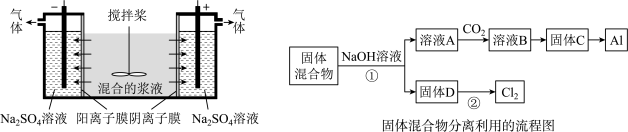
Ⅰ.固体混合物的分离和利用(流程图中的部分分离操作和反应条件未标明)
(1)C→Al的制备方法称为电解法,请写出阳极反应方程式_____________________ .
(2)该小组探究反应②发生的条件.D与浓盐酸混合,不加热无变化;加热有Cl2生成,当反应停止后,固体有剩余,此时滴加硫酸,又产生Cl2.由此判断影响该反应有效进行的因素有(填序号)_____ 。
A.温度 B.溶液的pH值 C.Cl-和 -的浓度
-的浓度
(3)固体D是碱性锌锰电池的正极,请写出该电池的负极反应方程式_____________ 。
(4)0.2molCl2与焦炭、TiO2完全反应,生成CO和TiCl4(熔点-25℃,沸点136.4℃)放热8.56kJ,该反应的热化学方程式为______________________________________ .
Ⅱ.含铬元素溶液的分离和利用
(5)用惰性电极电解时, 能从浆液中分离出来的原因是
能从浆液中分离出来的原因是_________________ ,
分离后得到的含铬元素的粒子有 ﹣和
﹣和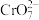 ﹣,原因是
﹣,原因是__________________________ (用离子反应方程式表示),阴极室生成的物质为_____________ (写化学式);


Ⅰ.固体混合物的分离和利用(流程图中的部分分离操作和反应条件未标明)
(1)C→Al的制备方法称为电解法,请写出阳极反应方程式
(2)该小组探究反应②发生的条件.D与浓盐酸混合,不加热无变化;加热有Cl2生成,当反应停止后,固体有剩余,此时滴加硫酸,又产生Cl2.由此判断影响该反应有效进行的因素有(填序号)
A.温度 B.溶液的pH值 C.Cl-和
 -的浓度
-的浓度 (3)固体D是碱性锌锰电池的正极,请写出该电池的负极反应方程式
(4)0.2molCl2与焦炭、TiO2完全反应,生成CO和TiCl4(熔点-25℃,沸点136.4℃)放热8.56kJ,该反应的热化学方程式为
Ⅱ.含铬元素溶液的分离和利用
(5)用惰性电极电解时,
 能从浆液中分离出来的原因是
能从浆液中分离出来的原因是分离后得到的含铬元素的粒子有
 ﹣和
﹣和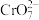 ﹣,原因是
﹣,原因是
更新时间:2019-12-04 23:04:06
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
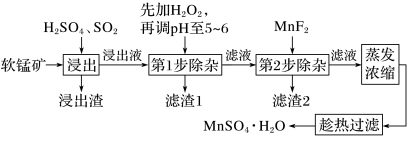
【推荐1】软锰矿的主要成分为MnO2,还含有Fe2O3、MgO、Al2O3、CaO、SiO2等杂质,工业上用软锰矿制取MnSO4·H2O的流程如图:
已知:①部分金属阳离子完全沉淀时的pH如表
②温度高于27℃时,MnSO4晶体的溶解度随温度的升高而逐渐降低。
(1)“浸出”过程中MnO2转化为Mn2+的离子方程式为___________ ;
(2)第1步除杂中加入H2O2的目的是___________ ;
(3)第1步除杂中形成滤渣1的主要成分为___________ (填化学式),调pH至5~6所加的试剂,可选择___________ (填字母)。
a.CaO b.MgO c.Al2O3 d.氨水
(4)第2步除杂,主要是将Ca2+、Mg2+转化为相应氟化物沉淀除去,写出MnF2除去Mg2+的离子方程式:___________ ,该反应的平衡常数数值为___________ ;(已知:MnF2的Ksp=5.3×10-3;CaF2的Ksp=1.5×10-10;MgF2的Ksp=7.4×10-11)
(5)采用“趁热过滤”操作的原因是___________ ;
(6)取少量MnSO4·H2O溶于水,配成溶液,测其pH发现该溶液显酸性,原因是_______ (用离子方程式表示)。

已知:①部分金属阳离子完全沉淀时的pH如表
| 金属阳离子 | Fe3+ | Al3+ | Mn2+ | Mg2+ |
| 完全沉淀时的pH | 3.2 | 5.2 | 10.4 | 12.4 |
②温度高于27℃时,MnSO4晶体的溶解度随温度的升高而逐渐降低。
(1)“浸出”过程中MnO2转化为Mn2+的离子方程式为
(2)第1步除杂中加入H2O2的目的是
(3)第1步除杂中形成滤渣1的主要成分为
a.CaO b.MgO c.Al2O3 d.氨水
(4)第2步除杂,主要是将Ca2+、Mg2+转化为相应氟化物沉淀除去,写出MnF2除去Mg2+的离子方程式:
(5)采用“趁热过滤”操作的原因是
(6)取少量MnSO4·H2O溶于水,配成溶液,测其pH发现该溶液显酸性,原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】某混合物甲中含有明矾KAl(SO4)2·12H2O、Al2O3和Fe2O3。在一定条件下由甲可实现下图所示的物质之间的转化。
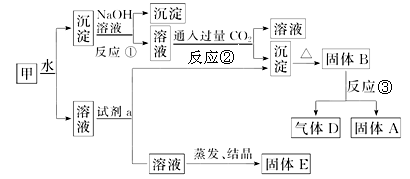
请回答下列问题:
(1)写出A、B的化学式:A______ ;B_____ 。
试剂a最好选用______________ (填序号),写出反应的离子方程式:_________ 。
(2)除去固体A中混有的镁选用__________ (填序号),写出反应的化学方程式:___________ 。
a.NaOH溶液 b.稀盐酸 c.二氧化碳 d.氨水
(3)写出反应②的离子方程式:_______________________________________________ 。

请回答下列问题:
(1)写出A、B的化学式:A
试剂a最好选用
(2)除去固体A中混有的镁选用
a.NaOH溶液 b.稀盐酸 c.二氧化碳 d.氨水
(3)写出反应②的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备金属铝的主要原料.工业上提取铝的工艺流程如下:
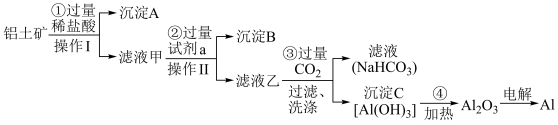
(1)沉淀A的化学式是____ ,沉淀B的化学式是____ ,滤液甲中所含金属离子是___ 、____ ,试剂a的化学式为__________ ;
(2)步骤③中通入过量CO2,产生沉淀C的离子方程式为___________________________________ ;
(3)Al2O3中所含的化学键的类型为________________ ;
(4)工业上用电解熔融Al2O3的方法制备金属铝,其反应方程式为_____________________________ ;
(5)在生活中,常利用Al与Fe2O3间的铝热反应来进行焊接钢轨。除了Fe2O3,铝粉还可以与很多金属氧化物组成铝热剂,下列氧化物中不能与铝粉组成铝热剂的是( )
a.MgO b.V2O5 c.Fe3O4 d.MnO2

(1)沉淀A的化学式是
(2)步骤③中通入过量CO2,产生沉淀C的离子方程式为
(3)Al2O3中所含的化学键的类型为
(4)工业上用电解熔融Al2O3的方法制备金属铝,其反应方程式为
(5)在生活中,常利用Al与Fe2O3间的铝热反应来进行焊接钢轨。除了Fe2O3,铝粉还可以与很多金属氧化物组成铝热剂,下列氧化物中不能与铝粉组成铝热剂的是
a.MgO b.V2O5 c.Fe3O4 d.MnO2
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】下图是中学化学中常用于化合物的分离和提纯装置,请根据装置回答问题:
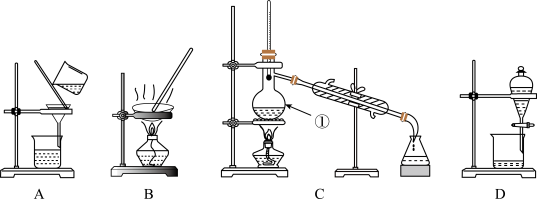
下图是中学化学中常用于化合物的分离和提纯装置,请根据装置回答问题:
(1)装置B中被加热仪器的名称是_____ ,装置C中①的名称是_________ 。
(2)某硝酸钠固体中混有少量硫酸钠杂质,现设计一实验方案,既除去杂质,又配成硝酸钠溶液。
实验方案:先将固体溶于蒸馏水配成溶液,选择合适的试剂和操作完成表格中各步实验。
所加入的试剂①可以是_____ (填化学式),证明溶液中SO42-已经除尽的操作是__________ 。加入Na2CO3溶液的目的是__________ ,所加入的试剂④是____________ (填化学式)。
(3)青蒿素是高效的抗疟疾药,为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156-157℃,热稳定性差。已知:乙醚沸点为35℃。提取青蒿素的主要工艺为:
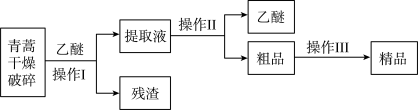
若要在实验室模拟上述工艺,操作I选择的实验操作是_____ ,操作Ⅱ选择的实验操作是_________ 。

下图是中学化学中常用于化合物的分离和提纯装置,请根据装置回答问题:
(1)装置B中被加热仪器的名称是
(2)某硝酸钠固体中混有少量硫酸钠杂质,现设计一实验方案,既除去杂质,又配成硝酸钠溶液。
实验方案:先将固体溶于蒸馏水配成溶液,选择合适的试剂和操作完成表格中各步实验。
| 选择试剂 | ① | Na2CO3溶液 | ④ |
| 实验操作 | ② | ③ | 加热 |
(3)青蒿素是高效的抗疟疾药,为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156-157℃,热稳定性差。已知:乙醚沸点为35℃。提取青蒿素的主要工艺为:

若要在实验室模拟上述工艺,操作I选择的实验操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】对叔丁基邻苯二酚是一种无色晶体,有毒,是工业上的一种阻聚剂,实验室可用邻苯二酚和甲基叔丁基醚在硫酸的催化下反应制备,反应原理和装置图如图所示。实验中会生成 二叔丁基邻苯二酚、磺化产物等副产物。
二叔丁基邻苯二酚、磺化产物等副产物。
(1)该反应的反应类型为___________ 。
(2)可在如图装置中进行,仪器 的名称是
的名称是___________ ;比起蒸馏实验中的直形冷凝管,球形冷凝管A冷凝效果更好,原因是___________ 。
(3)反应中硫酸不宜过多过浓的原因是___________ 。
(4)实验的流程图如图所示: 溶液的目的主要是除去混合液中的硫酸,调节
溶液的目的主要是除去混合液中的硫酸,调节 ,操作2的名称是
,操作2的名称是___________ 。
②操作3的目的是___________ 。
③若要进一步提纯粗产品对叔丁基邻苯二酚可进行的实验操作是___________ 。
 二叔丁基邻苯二酚、磺化产物等副产物。
二叔丁基邻苯二酚、磺化产物等副产物。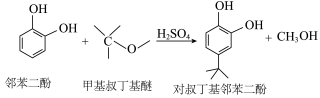
 装置图(部分)
装置图(部分)
| 物质 | 沸点 | 熔点 | 溶解性 |
| 对叔丁基邻苯二酚 | 57 | 285 | 溶于甲醇、乙醚、四氯化碳等,难溶于冷水 |
(1)该反应的反应类型为
(2)可在如图装置中进行,仪器
 的名称是
的名称是(3)反应中硫酸不宜过多过浓的原因是
(4)实验的流程图如图所示:

 溶液的目的主要是除去混合液中的硫酸,调节
溶液的目的主要是除去混合液中的硫酸,调节 ,操作2的名称是
,操作2的名称是②操作3的目的是
③若要进一步提纯粗产品对叔丁基邻苯二酚可进行的实验操作是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】硫酸铅(PbSO4)广泛应用于制造铅蓄电池、白色颜料等。工业生产中利用方铅矿(主要成分为PbS,含有FeS2等杂质)和软锰矿(主要成分为MnO2)制备PbSO4的工艺流程如图:
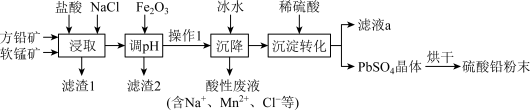
已知:i.PbCl2难溶于冷水,易溶于热水。
ii.PbCl2(s)+2Cl-(aq) PbCl42-(aq) ΔH>0
PbCl42-(aq) ΔH>0
iii.Ksp(PbSO4)=1.08×10-8,Ksp(PbCl2)=1.6×10-5。
(1)“浸取”时需要加热,此时盐酸与MnO2、PbS发生反应生成PbCl2和S的化学方程式为__ 。
(2)“调pH”的目的是__ 。
(3)“沉降”操作时加入冰水的作用是__ 。
(4) 时,PbCl2(s)在不同浓度的盐酸中的最大溶解量(g·L-1)如图所示。下列叙述正确的是
时,PbCl2(s)在不同浓度的盐酸中的最大溶解量(g·L-1)如图所示。下列叙述正确的是__ (填字母)。
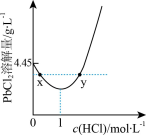
A.盐酸浓度越小,Ksp(PbCl2)越小
B.x、y两点对应的溶液中c(Pb2+)不相等
C.当盐酸浓度为1mol·L-1时,溶液中c(Pb2+)一定最小
D.当盐酸浓度小于1mol·L-1时,随着HCl浓度的增大,PbCl2溶解量减小是因为Cl-浓度增大使PbCl2溶解平衡逆向移动
(5)PbCl2经“沉淀转化”后得到PbSO4,当c(Cl-)=0.1mol·L-1时,c(SO42-)=__ 。
(6)“滤液a”经过处理后可以返回到__ 工序循环使用。利用制备的硫酸铅与氢氧化钠反应制备目前用量最大的热稳定剂三盐基硫酸铅(3PbO·PbSO4·H2O),该反应的化学方程式为__ 。

已知:i.PbCl2难溶于冷水,易溶于热水。
ii.PbCl2(s)+2Cl-(aq)
 PbCl42-(aq) ΔH>0
PbCl42-(aq) ΔH>0iii.Ksp(PbSO4)=1.08×10-8,Ksp(PbCl2)=1.6×10-5。
(1)“浸取”时需要加热,此时盐酸与MnO2、PbS发生反应生成PbCl2和S的化学方程式为
(2)“调pH”的目的是
(3)“沉降”操作时加入冰水的作用是
(4)
 时,PbCl2(s)在不同浓度的盐酸中的最大溶解量(g·L-1)如图所示。下列叙述正确的是
时,PbCl2(s)在不同浓度的盐酸中的最大溶解量(g·L-1)如图所示。下列叙述正确的是
A.盐酸浓度越小,Ksp(PbCl2)越小
B.x、y两点对应的溶液中c(Pb2+)不相等
C.当盐酸浓度为1mol·L-1时,溶液中c(Pb2+)一定最小
D.当盐酸浓度小于1mol·L-1时,随着HCl浓度的增大,PbCl2溶解量减小是因为Cl-浓度增大使PbCl2溶解平衡逆向移动
(5)PbCl2经“沉淀转化”后得到PbSO4,当c(Cl-)=0.1mol·L-1时,c(SO42-)=
(6)“滤液a”经过处理后可以返回到
您最近一年使用:0次



